方案详情
文
为实时分析和高通量性能而设计Octet互作分析系统能够大幅缩短研发时间,简化了最佳候选药物的选择流程,为下游开发的成功提供了最佳机会。
方案详情

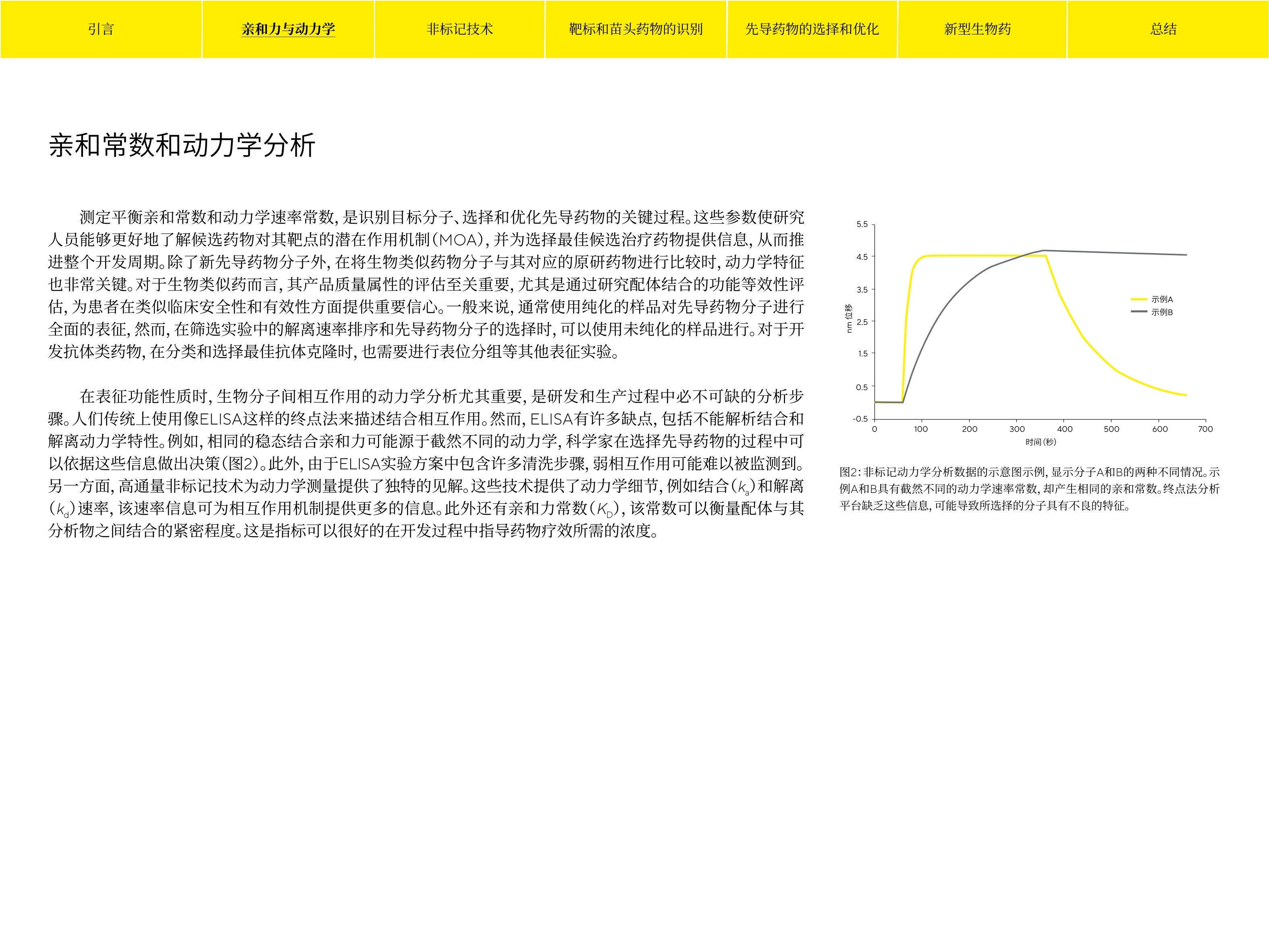
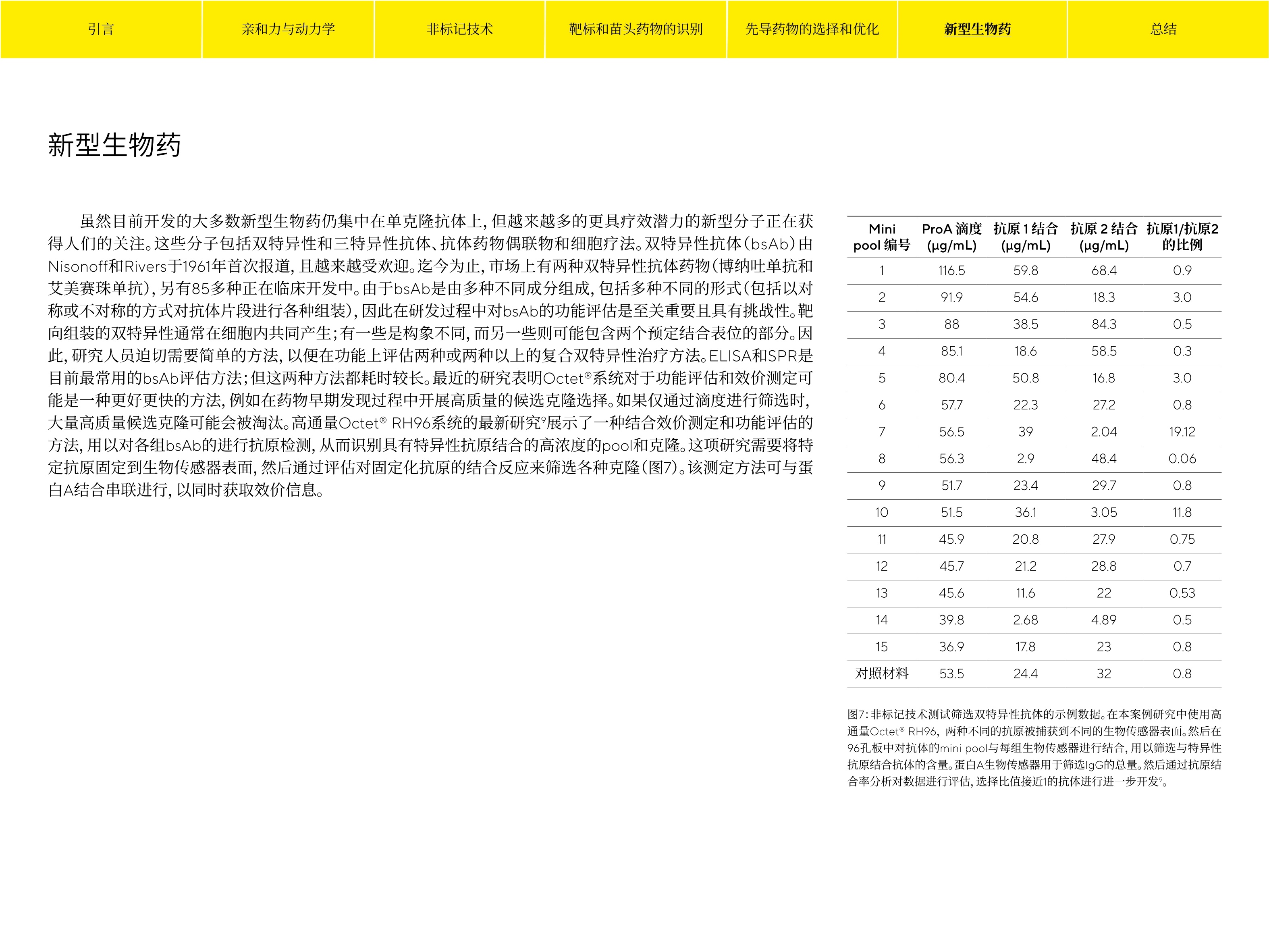
非标记技术 服务热线 400 920 9889|800 820 9889邮箱 lab.cn@sartorius.com销售与服务联系方式 非标记技术在药物早期发现中的应用 Simplifying Progress 大多数小分子药物和生物药(包括单克隆抗体)可以作用于治疗靶点,从而改变其功能。药物开发的前提是通过对这些靶点的鉴别,通常是蛋白质或核酸,明确它们在疾病中所起到的因果作用以及具有一定的“成药性”,例如药物有适当的药理作用1。药物开发过程往往是耗时长,风险高且花费巨大。一种新药从发现到被批准上市,尽管精确的时间表各不相同,但通常需要10年以上的时间。此外,在每年开发的许多候选药物中,只有很少一部分能够获得监管机构的批准进入临床试验研究。筛选靶点特异性结合的候选药物,验证与靶点的相互作用,需要多种工艺和表征技术,而这些工艺和表征技术的局限性又是药物研发耗时冗长的诸多原因之一。具备实时分析和高通量性能的现代分析技术大大缩短了药物研发时间,并运用简化的方式选择最佳候选药物,为下游开发的成功提供了最佳机会。 苗头药物的高通量 先导药物的选择 靶点鉴别和验证 筛选 和优化 图1:药物早期发现的关键阶段,即从靶点的鉴别和验证到先导药物的选择和优化。整个过程可能需要5年的时间,才能进入临床研究。 传统的分析技术,例如基于荧光的方法,都需要对分析物或二抗分子标记上荧光信号。标记位点通常不具备特异性,因此可能会导致结构改变,从而影响其活性。需要标记的分析方法往往包含多个特定的步骤,每个步骤都需要进行优化,最终导致研发时间的增加。此外,由于荧光标记的干扰而产生的假阳性结果可能对数据质量产生不利影响。近20年来,非标记分析技术在药物早期发现中展现出明显的优势。由于不需要标记试剂,非标记分析平台能够大幅加快实验开发过程。非标记技术在药物发现中的关键应用包括通过平衡解离常数(K),结合速率常数(k),解离速率常数(k)等动力学参数,评估结合药物与靶点的结合活性。图1展示了药物早期发现阶段常规工作流程中的关键步骤。 引言 亲和力与动力学 非标记技术 靶标和苗头药物的识别 先导药物的选择和优化 新型生物药 总结 亲和常数和动力学分析 测定平衡亲和常数和动力学速率常数,是识别目标分子、选择和优化先导药物的关键过程。这此参数使研究人员能够更好地了解候选药物对其靶点的潜在作用机制(MOA),并为选择最佳候选治疗药物提供信息,从而推进整个开发周期。除了新先导药物分子外,在将生物类似药物分子与其对应的原研药物进行比较时,动力学特征也非常关键。对于生物类似药而言,其产品质量属性的评估至关重要,尤其是通过研究配体结合的功能等效性评估,为患者在类似临床安全性和有效性方面提供重要信心。一般来说,通常使用纯化的样品对先导药物分子进行全面的表征,然而,在筛选实验中的解离速率排序和先导药物分子的选择时,可以使用未纯化的样品进行。对于开发抗体类药物,在分类和选择最佳抗体克隆时,也需要进行表位分组等其他表征实验。 在表征功能性质时,生物分子间相互作用的动力学分析尤其重要,是研发和生产过程中必不可缺的分析步骤。人们传统上使用像ELISA这样的终点法来描述结合相互作用。然而, ELISA有许多缺点,包括不能解析结合和解离动力学特性。例如,相同的稳态结合亲和力可能源于截然不同的动力学,科学家在选择先导药物的过程中可以依据这些信息做出决策(图2)。此外,由于ELISA实验方案中包含许多清洗步骤,弱相互作用可能难以被监测到。另一方面,高通量非标记技术为动力学测量提供了独特的见解。这些技术提供了动力学细节,例如结合(k)和解离(k)速率,该速率信息可为相互作用机制提供更多的信息。此外还有亲和力常数(K),该常数可以衡量配体与其分析物之间结合的紧密程度。这是指标可以很好的在开发过程中指导药物疗效所需的浓度。 图2:非标记动力学分析数据的示意图示例,显示分子A和B的两种不同情况。示例A和B具有截然不同的动力学速率常数,却产生相同的亲和常数。终点法分析平台缺乏这些信息,可能导致所选择的分子具有不良的特征。 虽然在药物研发中仍然会使用诸如ELISA和Western Blots等传统生化分析方法,但是越来越多的科学家在他们的工作流程中开始采用非标记分析技术。基于这些技术的系统可以将生物分子间的相互作用转化为响应信号(通常是实时信号),为研究人员提供研究表征结合机制的工具。除此之外,这些系统可用于动力学表征、浓度测定和生物分子相互作用筛选等。非标记技术可在动力学表征实验中提供结合/解离速率信息,这是和亲和力常数息息相关的重要因素,也是终点法分析技术(如ELISA)所无法提供的。常用的非标记技术有:等温滴定量热技术(ITC)、表面等离子共振技术(SPR)和生物层干涉技术(BLI),每种技术都有其独特的优点。面对如此多的选择,研究人员应用所需的技术,在药物研发过程的各个阶段推动候选药物快速准确地进行。在这些常用的非标记技术中,ITC所提供的丰富的热力学数据具有广泛的用途;但在相互作用研究中, ITC无法提供动力学信息,如k和k值。SPR和BLI虽然无法获取丰富的热力学数据,但它们都可提供带有丰富信息的亲和力表征数据,例如k和k值(请在此处阅读有关非标记技术的更多信息)。基于BLI技术的Octet@平台具有独特的优势,使其成为加速药物早期发现的理想技术。 Octet@平台采用96孔或384孔样品板,仪器的读取探头可直接移动到样品板中。与SPR技术明显不同的是,Octet采用非流路设计,可以更好的耐受不同样品的基质。与SPR仪器相比, Octet@系统也相对易于使用,其对使用者的操作和分析技能要求相对更低,并且不需要在样品装载或样品运行时的清洗环节上浪费大量时间。这些特性,加上其一次可同时分析多达96个样品(Octet@RH96)的能力,使得Octet成为药物早期发现阶段中理想的先导药物选择系统。 Octet系统用于药物早期发现的优势: ·无流路;不堵塞样品,系统可兼容多种类型的粗样品 ·易于使用,用途广泛;与其他技术相比,使用者的技能门槛较低 ·高通量;能够快速筛选主要生物制药的靶点 ·低维护;与SPR技术相比,维护时间大幅减少 靶点和苗头药物的识别 新治疗药物的发现始于靶标识别;即识别与疾病病理生理学相关的生物学靶点的过程4。非标记实验可以监测不同类型的生物分子之间的相互作用,包括蛋白质、DNA/RNA、抗体、病毒和细胞。现有丰富的人类遗传信息可用于识别药物靶点、验证治疗方案并预测针对分子靶点的抑制性化合物的潜在安全性。一旦确定了靶点,下一步就是开发一个分子库来筛选有希望的先导候选药物。这个过程通常包括筛选数以万计的小分子或生物药,用以确定可与细胞疾病的靶点蛋白相结合并引起变化的少数最佳候选药物(通常3-5个)。 在药物发现项目中,基于片段的药物发现(FBDD)是一个用于识别小分子候选药物的热门平台。片段结合可以使用灵敏的生物物理技术来检测和表征,该技术能够检测小分子化合物的弱亲和力相互作用。诸如核磁共振(NMR)、X射线晶体衍射、差示扫描荧光法(DSF)、SPR和BLI等技术是许多制药和生物技术实验室用于识别目标靶点的核心技术。然而,片段筛段往往受到样品量大、分子量低(<300 Da)、亲和力弱(K=10pM-10mM)和溶解度低等诸多限制。微弱的亲和力和有限的溶解度就需要使用高于相互作用K,值的样品浓度来测试结合,但这个条件往往又不切实际,并且经常导致最终做出决策是基于不适当的实验设置条件。Pioneer FE是新一代的SPR仪器,可凭借其独有的一步进样(OneStep)功能做出更好的决策5。OneStep进样功能可通过在进样管道中生成样品或分析物的梯度浓度来增加样品通量和数据信息量,从而显著改善基于SPR技术的片段筛选。Pioneer FE旨在通过在单次样品进样中测试全浓度梯度来简化结合分析。这不仅节省了样品制备时间和材料,而且免除了制备多浓度样品稀释液的需求,也减少人为误差。OneStep进样功能还通过简化工作流程的效率,显着改善SPR生物传感器芯片检测的运作方式(在此处了解更多信息)。当候选片段选择在初步筛选过程中就完成优化,则完全没有必要再进行二次筛选(图3和图4)。 图3:在Pioneer FE上进行化合物片段筛选的工作流程。首先将蛋白靶点固定在生物传感器表面,然后使用OneStep进样功能,在单次进样中对逐渐增加的分析物浓度进行评估,从而实现对片段库的筛选。 图4:使用赛多利斯的Pioneer-FE系统进行一步法初步筛选的结果。阳性对照化合物重复运行了16次,图中以蓝色显示。插图显示每个片段的终点反应与对应的分析周期数,以及蓝色标识的对照化合物的16个重复数据。OneStep进样法可通过单一分析物浓度测定亲和力和动力学(k、k、K)值,免除对多个分析物浓度的需求。 在选择具有最佳药物特性的候选药物时,通常要对靶向特异性、可生产性和可开发性等指标对生物制药候选库(如杂交瘤或噬菌体展示)开展筛选。筛选工作通常从分析主要目标靶点的结合开始,然后再进行动力学表征。必须在发现过程的早期就把那些靶点结合亲和力较弱、靶点选择性低、生化或生物物理特性差的不良苗头药物都剔除掉。然而,如果需要在分析前对大量的杂交瘤或噬菌体展示样品进行纯化,那么先导药物的选择和优化就会成为一个瓶颈问题。由于非特异性结合高和检测分辨率低,大多数分析技术无法在粗样品中实现准确的测量。由于粗样品通常会导致微流路管道的堵塞,因此与使用微流路设计的系统相比,应用非标记技术(如Octet@)的系统是分析这些类型样品的理想选择。 生物制药通常都是大分子,需要具有高通量能力的技术来同时快速筛选多个样品。更关键的是能够在其原液中直接筛选出这些分子,从而节省纯化样品所需的时间和资源。 治疗性抗体发现中的杂交瘤 杂交瘤是由抗原免疫小鼠的脾脏B细胞和骨髓瘤细胞系融合而成。杂杂瘤是产生抗体的克隆细胞系,可被用于抗原特异性结合的筛选。迄今为止,有一半以上的商业化抗体药物来自杂交瘤细胞系,并且杂交瘤已被用于生产双特异性单克隆抗体。在开发单克隆抗体疗法时,筛选融合杂交瘤以及亚克隆候选杂交瘤,是一个非常耗时的步骤。这一挑战不仅体现于先导药物在基于体内疗效和表位作图的选择,也体现于先导药物优化过程中的人源化、亲和力成熟、药物安全性研究和生物标记物开发等方面。传统上,在将杂交瘤细胞转移到多孔分析板之前,需要使用细胞分选法将杂交瘤分离成单个细胞,然后使用单点结合实验筛选杂交瘤上清液,用以评估抗原结合。之后可以分离一部分阳性克隆用以抗体鉴别,这些抗体将被表达和纯化,以作进一步的表征。因此,筛选杂交瘤上清液用于抗原结合抗体是发现过程中的关键步骤。高通量技术可以大幅缩短选择最佳抗体的时间,有效促进这一过程。 虽然ELISA已被用于筛选先导药物,但在应用ELISA对抗体进行抗体库筛选时,无法根据靶点开展排序。Octet@系统可识别具有高亲和力和低解离速率的克隆,以便进一步表征。目前解离速率分析非常流行,因为无需知道抗体浓度就能对粗样品实现快速筛选和评估,如细菌裂解液等(图5)。与非标记技术(如Octet系统)一起使用时,该过程只需简单地将目标抗原固定在生物传感器表面,然后将生物传感器浸入样品库中,从而监测抗原和抗体的解离。与亲和力较低的候选先导药物相比,结合力强的候选先导药物会表现出较慢的解离速率。 图5:在Octet@系统上评估裂解液的传感图。(A)将药物A或药物B固化在传感器上,并监测粗裂解液中Fab抗体的K值。根据K值对Fab进行排序。 噬菌体展示 特定抗体的基因序列通常被整合到丝状噬菌体的DNA序列中。噬菌体在其衣壳表面表达单链抗体scFv,通过感染大肠杆菌并利用其复制系统连续展示新噬菌体,这导致了大量scFv的快速生成。此外,噬菌体淘选是一种将噬菌体展示与所需靶标结合的过程,可以用多个抗原按顺序进行,以富集靶向保守表位的抗体8。杂交瘤与噬菌体展示技术存在根本性的差异。与杂交瘤技术相比,噬菌体展示技术被认为更为通用、强大且快速。它也被广泛应用于体外方法,使得候选药物的亲和力成熟更容易控制。利用这两种技术都可以进行解离速率排序,以便加快先导药物的选择过程。 表位分组 杂交瘤和噬菌体展示方法旨在针对每个靶点产生大量抗体。根据结合靶点表位的相似性,这些抗体通常需要归类到不同的“组”中,因为相似的表位会表现为相似的功能。因此,表位分组是一种被广泛应用的先导药物选择技术。在这一过程中,单克隆抗体以成对的方式或组合的方式相互竞争,以便与特定抗原结合。表位组是指在被测试的单克隆抗体组中代表的单个表位。因此,如果两个单克隆抗体具有相同的阻断效应,则它们同属于一个组。由于用计算机预测B细胞表位极具挑战,表位分组技术仍然是一个依赖经验的过程6,其中非标记分析技术发挥着至关重要的作用。表位分组主要使用三种形式(图6);预混法、夹心法、以及串联法。在这三种方法中,最常用的是传统的夹心分析法,即将一种抗体固定在固体表面(生物传感器或芯片表面),然后结合上目标分子(抗原),最后通过检测第二个抗体组的结合来进行筛选。串联法也很常见,该方法是首先固定抗原,然后结合第一个抗体,再筛选另一组抗体。预混法使用较少,主要是因为预混合的样品之间需要较高的比率,这使得该方法的成本相对更高。所有这些方法的目的都是通过评估每个连续结合步骤,并根据结合图谱的相似性将筛选出的抗体进行分组。虽然有许多非标记技术能够进行表位分组,但考虑到需要筛选的候选物数量,高通量仪器往往更适合这种应用。由于经常需要尝试使用多种方法,特别是当一种方法的结合响应不甚明确时,像Octet@RH96这样的系统无疑是一个最理想的选择。它具有前所未有的高通量,并可以灵活的运行所有三种分析方法。 图6:非标记技术中的表位分组测定方法(A-C)以及方法设置中的重要注意事项(D)。 虽然目前开发的大多数新型生物药仍集中在单克隆抗体上,但越来越多的更具疗效潜力的新型分子正在获得人们的关注。这些分子包括双特异性和三特异性抗体、抗体药物偶联物和细胞疗法。双特异性抗体(bsAb)由Nisonoff和Rivers于1961年首次报道,且越来越受欢迎。迄今为止,市场上有两种双特异性抗体药物(博纳吐单抗和艾美赛珠单抗),另有85多种正在临床开发中。由于bsAb是由多种不同成分组成,包括多种不同的形式(包括以对称或不对称的方式对抗体片段进行各种组装),因此在研发过程中对bsAb的功能评估是至关重要且具有挑战性。靶向组装的双特异性通常在细胞内共同产生;有一些是构象不同,而另一些则可能包含两个预定结合表位的部分。因此,研究人员迫切需要简单的方法,以便在功能上评估两种或两种以上的复合双特异性治疗方法。ELISA和SPR是目前最常用的bsAb评估方法;但这两种方法都耗时较长。最近的研究表明Octet@系统对于功能评估和效价测定可能是一种更好更快的方法,例如在药物早期发现过程中开展高质量的候选克隆选择。如果仅通过滴度进行筛选时,大量高质量候选克隆可能会被淘汰。高通量Octet@RH96系统的最新研究?展示了一种结合效价测定和功能评估的方法,用以对各组bsAb的进行抗原检测,从而识别具有特异性抗原结合的高浓度的pool和克隆。这项研究需要将特定抗原固定到生物传感器表面,然后通过评估对固定化抗原的结合反应来筛选各种克隆(图7)。该测定方法可与蛋白A结合串联进行,以同时获取效价信息。 Mini ProA滴度:3抗原1结合 抗原2结合抗原1/抗原2 pool编号 (ug/mL) (ug/mL) (ug/mL) 的比例 116.5 59.8 68.4 0.9 2 91.9 54.6 18.3 3.0 3 88 38.5 84.3 0.5 4 85.1 18.6 58.5 0.3 5 80.4 50.8 16.8 3.0 6 57.7 22.3 27.2 0.8 7 56.5 39 2.04 19.12 8 56.3 2.9 48.4 0.06 9 51.7 23.4 29.7 0.8 10 51.5 36.1 3.05 11.8 11 45.9 20.8 27.9 0.75 12 45.7 21.2 28.8 0.7 13 45.6 11.6 22 0.53 14 39.8 2.68 4.89 0.5 15 36.9 17.8 23 0.8 对照材料 53.5 24.4 32 0.8 图7:非标记技术测试筛选双特异性抗体的示例数据。在本案例研究中使用高通量Octet@RH96,两种不同的抗原被捕获到不同的生物传感器表面。然后在96孔板中对抗体的mini pool与每组生物传感器进行结合,用以筛选与特异性抗原结合抗体的含量。蛋白A生物传感器用于筛选IgG的总量。然后通过抗原结合率分析对数据进行评估,选择比值接近1的抗体进行进一步开发。 引言 亲和力与动力学 非标记技术 靶标和苗头药物的识别 先导药物的选择和优化 新型生物药 总结 总结 在候选治疗药物的早期发现阶段中有几个关键步骤;其中,目标靶点识别、验证和先导候选药物选择都至关重要。如果处理得不好,药物开发的时间可能会面临多次挫折,并且成本也变得令人难以承受。虽然已有许多分析技术被用于药物早期发现,但能够快速筛选所需特性的技术无疑可以大幅缩短研发周期。从技术上来讲,如果一个技术在满足粗样品和微量样品检测的同时,也能够得到准确的相关信息,则可以快速筛选和验证最佳的候选药物进入到下游开发。在常用的非标记技术中,BLI技术为研究人员提供了最大最价值。采用BLI技术沐Octet系统是一个多应用平台,它可以对库中的克隆进行高通量靶向特异性分析、解离速率排序和其他关键质量属性(如糖基化)筛选,这些应用都有助于候选克隆在下游工艺中提高成功的可能性。另外,Octet系统能够大幅缩短识别、选择和优化候选治疗药物所需的时间。 引言 亲和力与动力学 靶标和苗头药物的识别 先导药物的选择和优化 新型生物药 总结 ( 参考文献 ) ( 1. Hingorani, AD et al., Improving the Odds of Drug Development Success Through Human Genomics: ModellingStudy. Scientific reports, 2019 Dec 11;9(1):18911. ) ( 2. Kalimuthu, S et al., Drug Discovery by Molecular Imaging a nd Monitoring Therapy Response in Lymphoma.Int JMol Sci., 2017 Jul 27;18(8):1639. ) ( 3 . Hughes, JP et al., Principles of Early Drug Discovery. Br J Pharmacol., 2011 Mar;162(6):1239-49. ) ( 4. Floris , M et al., Genetic-Driven Druggable Target I dentification and Validation. Trends Genet., 2018 Jul;34(7):558-570. ) ( 5. Giannetti, AM et al., Getting the Most Value From Your Screens: Advances in Hardware, Software andMethodologies to Enhance Surface Resonance Based Fragment Screening and Heat to Lead Support. RSCDrug Discovery series. 2015:19-48. ) ( 6. Abdiche, YN et al., High-Throughput Epitope Binning Assays on Label-Free Array-Based Biosensors Can Y ieldExquisite Epitope Discrimination T h at F a cilitates the S election o f M onoclonal Antibodies With Fun c tionalActivity . P L oS One, 2014 Mar 20;9(3):e92451. ) ( 7. Bazan, J et al. , Phage Display-A Powerful Technique for Im m unotherapy: 1. Int r oduction and P otential ofTherapeutic Applications. Hum Vaccin Immunother., 2012 Dec1;8 ( 12):1817-28. ) ( 8.VVarkey, R et al., Discovery and Characterization of Potent IL-21 Neutralizing Antibodies via a Novel AlternatingAntigen Immunization and Humanization Strategy. PLoS One, 2019 Jan 25;14 ( 1):e0211236. ) ( 9. Rubio-Marerro, E e t al., A Rapid Method to Quantitatively Screen Bi s pecific Antibody Using Pro t ein A a n dHIS1K Biosensors. S a rtorius Application Note 29. ) 更多联系信息,请访问www.sartorius.com.cn 赛多利斯(上海)贸易有限公司上海市浦东新新盛荣路 388 弄百佳通产业园3号楼,7-11层, 200120电话 +86 21 6066 6100 技木规格如有变更,恕不另行通知。 ( 赛多利斯保留最终解释权和修改权。 ) SARTORILS 了解关于非标记技术的更多信息下载非标记技术电子书 药物研发过程通常是漫长的,风险高且花费巨大。一种新药从发现到临床试验再到批准上市,通常需要10年以上的时间。此外,每年开发的许多候选药物中,只有很少一部分能够最终进入临床试验,并获得监管机构的批准。识别和分离一个治疗靶点,并表征其性质及靶向相互作用,需要多种工艺和表征技术,这些工艺和表征技术的局限性又往往导致了漫长的开发时间表。为实时分析和高通量性能而设计Octet互作分析系统能够大幅缩短研发时间,简化了最佳候选药物的选择流程,为下游开发的成功提供了理想机会。请下载并阅读赛多利斯公司最新推出的《非标记技术在药物早期发现中的应用》电子书。点击下载查看全文有人又会觉得陈老湿在自吹自擂了吧?那么我们就来看看那些监管机构已经批准,并在申报资料中用到BLI数据的药物吧。引用Octet数据的药物评估资料汇总欧盟医药管理局(EMA)的药物评估资料(assessment report)包含了已经被EMA批准上市的药物的质量研究、药理、药代动力学和毒理等非临床研究,以及临床研究的研究资料,并且可以免费下载。这些已上市药物(包含众多大名鼎鼎的药物,比如K药,T药,辉瑞的新冠疫苗等)的研发中应用了Octet的BLI技术。当然,没有提到Octet也并不代表没有用到, 一般药物评估资料中只会列举一些该药物研发的核心技术。从数据可以发现,Octet在药物早期研发的应用非常广泛,是名副其实的生物制药研发工具中的多面手,也是生物制药公司研发必备的利器之一。Octet是生物药物研发中的“多面手”Octet的应用能够贯穿在抗体研发和生产的各个环节中,涵盖药物研发前期抗体库构建后的大规模筛选、亲和力的成熟,研发后期的免疫原性测定、细胞株的筛选,以及生产阶段的残留物监控和抗体活性检测。详情可前往【赛多利斯实验室】微信公众号阅读陈老湿的往期内容- 杂交瘤筛选:一个都不能少——杂交瘤筛选不只有ELISA- pH依赖性抗体筛选:给药周期从14天延长到56天——ForteBio助力新型孤儿药物研发- 抗体表位分组:诺奖获得者教你做分子互作竞争实验 有的放矢,事半功倍 ——表位分组实验设计与分析线上培训- 抗体药物表征:中检院教你如何评价原研药与类似药的相似性- 抗体粘性:别和自己过不去--用生物膜干涉技术检测蛋白自身相互作用- 免疫原性:结论很冷门-BLI,SPR,ECL(MSD)三种方法检测抗药性抗体(ADA)灵敏度的比较应用Octet加快药物研发周期Octet产品可以凭借较低的运营成本来获取比传统方法更丰富的数据和更广泛的应用,缩短研发周期,其面世后受到广大抗体研发生产企业的欢迎。自从去年新冠病毒在全球范围内肆虐,在各国应急发开的新冠病毒中和抗体或者疫苗的研发过程中,Octet系统的诸多优点被体现的淋漓尽致。最新可升级型Octet R系列已闪亮登场总 结在候选治疗药物的早期发现阶段中有几个关键步骤;其中,目标靶点识别、验证和先导候选药物选择都至关重要。如果处理得不好,药物开发的时间可能会面临多次挫折,并且成本也变得令人难以承受。虽然已有许多分析技术被用于药物早期发现,但能够快速筛选所需特性的技术无疑可以大幅缩短发现时间。从技术上来讲,如果在满足处理粗样品及微量体积样品的同时,也能够得到准确和相关的信息,这将使得早期阶段的快速筛选以及候选药物选择能够协助药物在下游阶段获取成功。采用BLI技术的Octet系统是一个多应用平台,它可以对库中的克隆进行高通量靶向特异性分析、解离速率排序和其他关键质量属性(如糖基化)筛选,这些应用都有助于候选克隆在下游工艺中提高成功的可能性。同时,Octet系统能够大幅缩短识别、选择和优化候选治疗药物所需的时间。在2020年末,Octet的生物层干涉技术(BLI)技术被正式列入《美国药典》,表明广大药物研发企业和科研工作者对该BLI技术的认可。请看“15年的等待!BLI技术正式列入《美国药典》(USP-NF)”
确定







还剩9页未读,是否继续阅读?
德国赛多利斯集团为您提供《蛋白样品中病毒检测方案(大分子作用仪)》,该方案主要用于其他中微生物相关及生化特性检测,参考标准--,《蛋白样品中病毒检测方案(大分子作用仪)》用到的仪器有赛多利斯 Octet® R2 生物分子相互作用分析系统、赛多利斯 Octet® R4 生物分子相互作用分析系统
该厂商其他方案
更多











