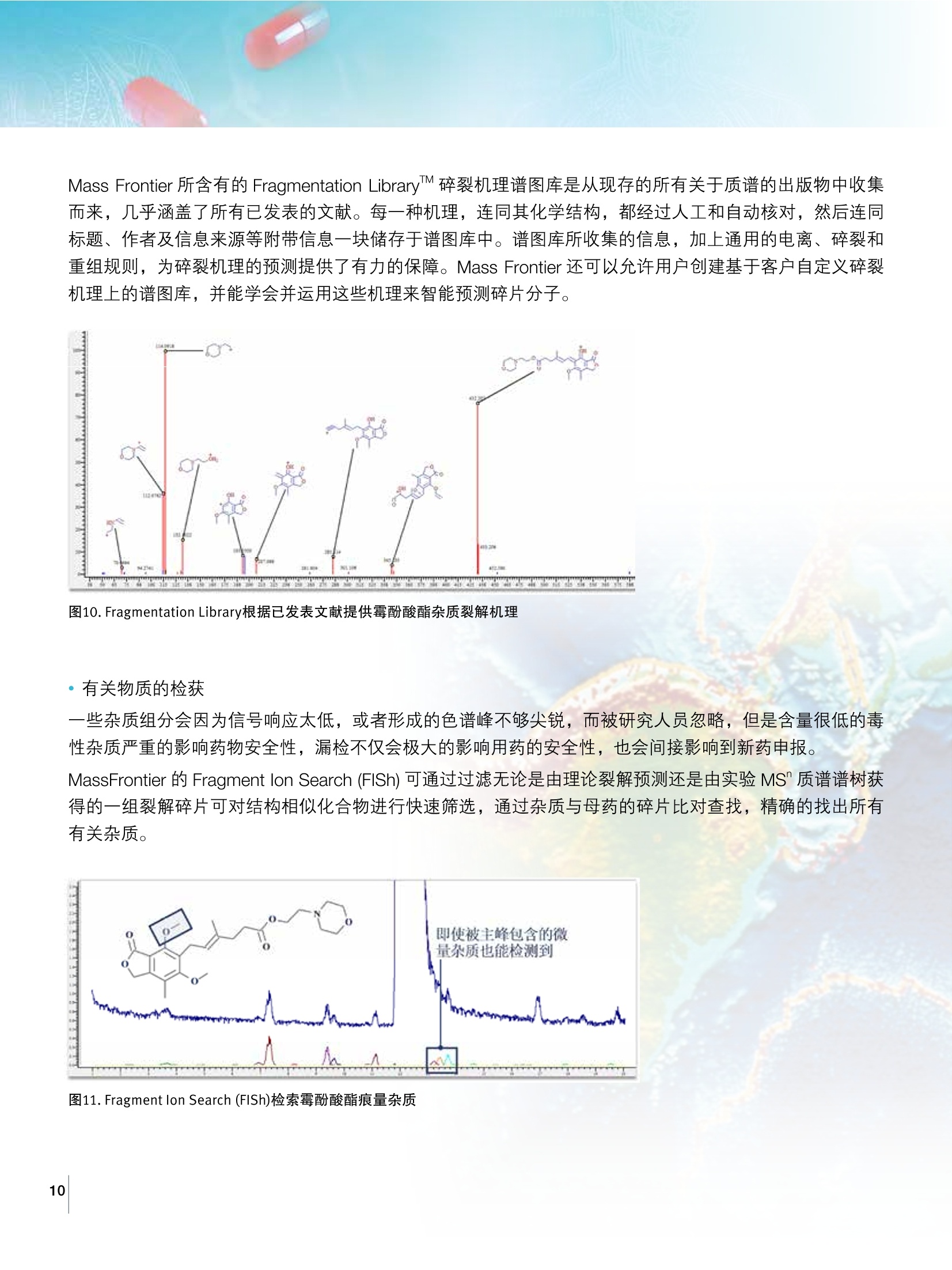
方案详情
文
赛默飞的离子阱技术有效解决了药物杂质研究难题,其高灵敏度和宽广的动态范围能够采集到药物中微量杂质的有效质谱信息;离子阱的多级质谱能力可以获得杂质的“指纹图谱”-- 离子树,结合强大的结构解析软件可以对工艺杂质或降解产物的结构进行深入有效的剖析;结合高效的色谱分离、深入的多级质谱分析和智能化的解析软件,赛默飞建立了基于离子阱质谱技术的药物杂质分析解决方案。
方案详情

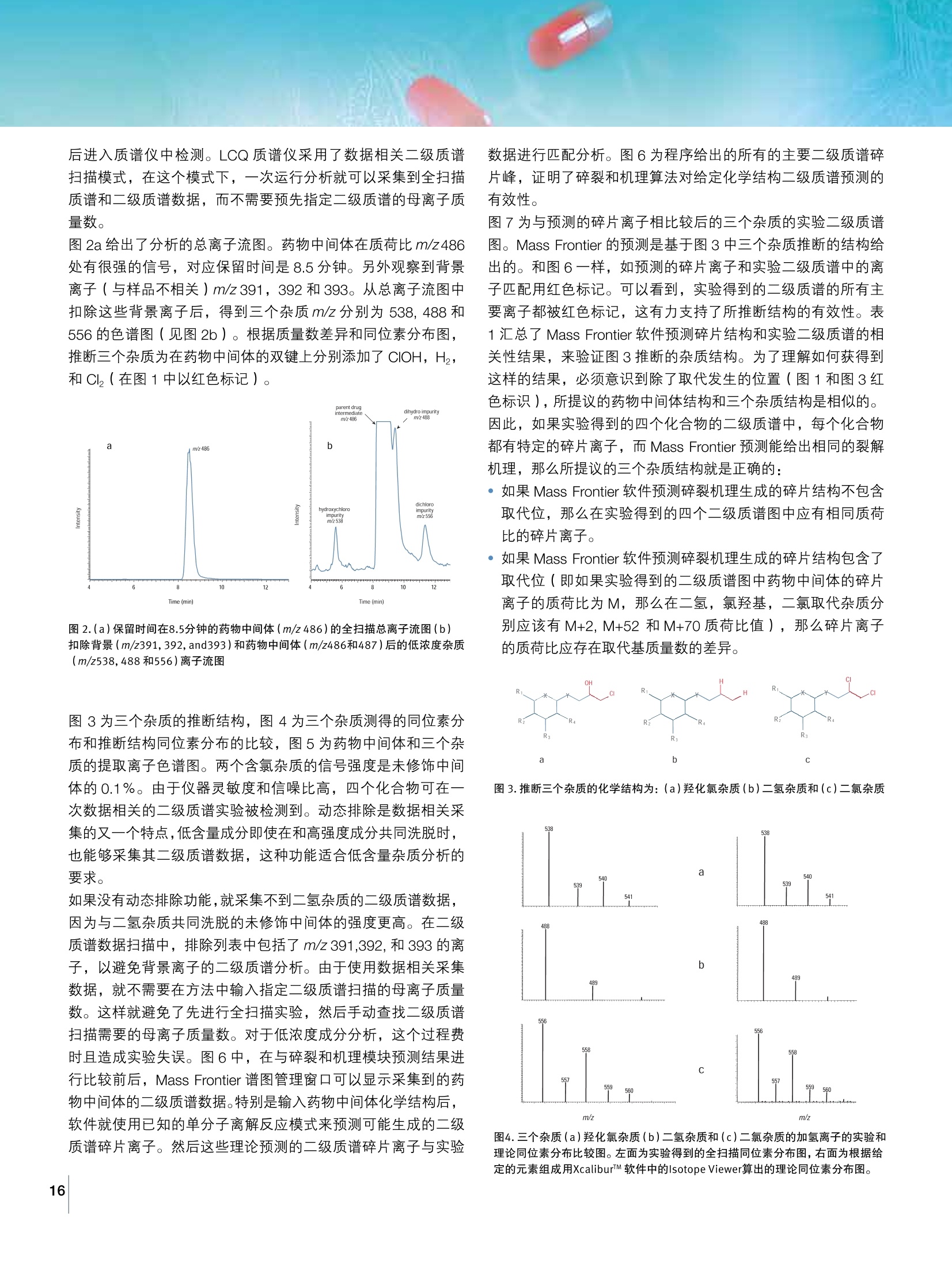
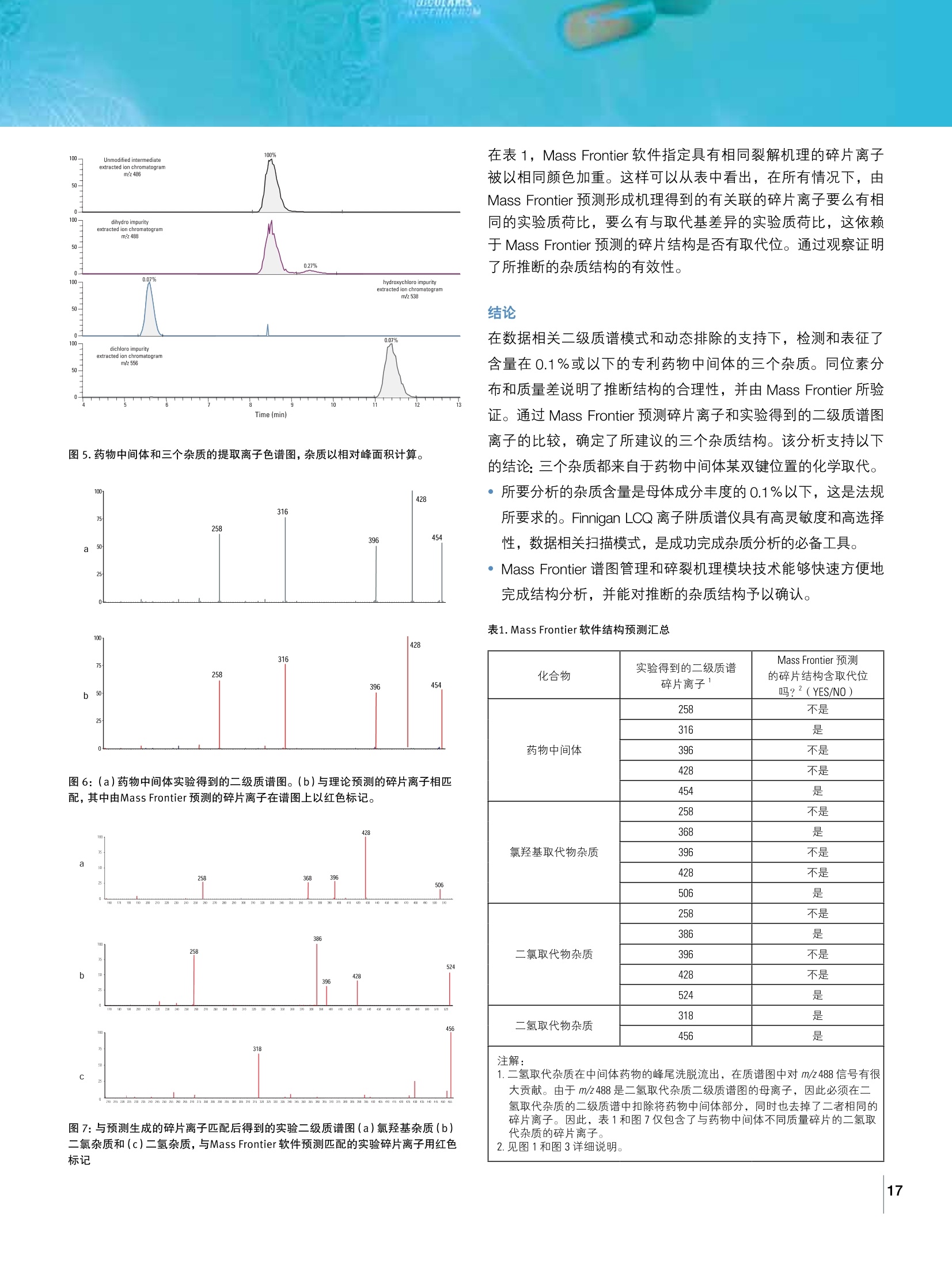
ALPEBNARUM 未知杂质分析 多级质谱技术深入剖析化合物结构 离子阱多级液质药物杂质分析解决方案 目录 序言…. 3 杂质分析工作流程….·...... 4 离子阱质谱技术介绍· 5 离子阱质谱原理…... 5 Thermo 专利的线性离子阱质谱 6 数据采集·. ....... .7 多种扫描方式…..... …7 目标杂质分析· 7 未矢杂质分析…… 8 数据分析….... .9 MassFrontier 专业结构解析软件 .9 离子阱质谱在药物杂质分析中的应用…...... 11 线性离子阱多种解离技术对阿德福韦酯杂质谱的全面鉴定· 11 应用 LCQ 离子阱质谱仪和 Mass Frontier 软件分析药物中间体的痕量杂质成分 …15 药物杂质分析部分客户文章列表·....... 18 附录…. ·19 药物杂质研究相关官方网站......... ..20 药物杂质因其可能对药品质量、安全性和有效性产生影响,目前成为国内外药品监管机构的重点关注内容之一。随着我国医药产品出口规模的扩大,了解国外法规市场的药物杂质控制要求、加强对药物杂质的分析与控制已成为国内药品生产企业共同关注的话题。 任何影响药物纯度的物质统称为杂质,人用药物注册技术要求国际协调会(简称ICH)对杂质的定义为药物中存在的,化学结构与该药物不一致的任何成分。药物中含有杂质会降低疗效,影响药物的稳定性,有的甚至对人体健康有害或产生其他毒副作用。因此,检测有关物质,控制纯度对确保用药安全有效,对保证药物质量非常重要。 杂质谱分析是指研究药物中存在的已知和未知的杂质的分布情况,分析药物中杂质的来源和去向,通过杂质谱的研究,可以全面的评估药物的安全性。对于药物生产阶段,杂质谱研究可以在工艺过程中建立完整可靠的杂质分析方法,对工艺的关键步骤 监控杂质的变化情况,验证杂质分析方法并转移到QA/QC,对于药物研发阶段,需要对艺研发过程中的杂质进行鉴定和表征并进一步确认杂质的来源,研发人员根据分析结果可以评价药物的安全性和与原研药的一致性,并根据杂质来源进一步优化工艺,降低或消除杂质的产生。 有机杂质主要起源于起始原料及其本身所含杂质、生产过程中带入的合成中间体与副反应产物、成品在储存过程中产生的降解产物,辅料带入的杂质或辅料相互作用降解产生的杂质,及药物与包材相互作用产生的杂质。有机杂质在成品药物中含量通常很低,制备纯化需要消耗大量人力物力,常规分析方法难以应对多组分、低含量的杂质结构解析工作。离子阱质谱仪,因其灵敏的MS"能力,复杂样品的高通量常规分析,高质量的结构信息,快速正负离子切换技术,快速正负离子切换技术,稳定、、可靠、便于操作,被广泛的应用于药物杂质研究,临床和法医鉴定,天然化合物鉴定,代谢物鉴定等领域。 杂质分析工作流程 药物中的杂质往往含量很小,在大量的母药存在下,检测到微量的杂质是对质谱技术的一大挑战,采集到杂质的质谱信息后,对这些工艺杂质或降解产物的结构进行有效的解析是另一大挑战。Thermo 的离子阱技术有效地解决了以上杂质研究难题,其高灵敏度和宽广的动态范围能够采集到微量杂质的有效质谱信息,离子阱的多级质谱能力和强大的解析软件可以对杂质结构进行深入的剖析,同时结合色谱高效的分离能力和专业的结构解析软件, Thermo 建立了专门针对杂质分析的解决方案。 图1.基于离子阱的杂质解析流程 离子阱质谱原理 离子阱是时间串联的质谱技术,化合物离子的捕获,隔离,激发和抛射都在阱中完成,正因如此,离子阱重复此扫描过程即可完成多级碎裂(MS")。 图2.离子阱时间串联扫描 离子阱中的稳定区域可以通过马绍方程计算出来,化合物离子在特定的射频电压下按照特定频率移动,增力 RF电压,,离子的频率(q值)将会增加,逐渐提高射频,使离子从低 m/z 到高 m/z逐渐依次离开,完成扫描。 图3.离子阱扫描原理 Thermo 专利的线性离子阱质谱 作为离子阱质谱的领导者, Thermo 专利的线性离子阱提供最快的速度同时保证优异的灵敏度 .离子沿着中心线方向聚集,同时也减少了空间电荷效应,极大提高离子容量; 离子捕获效率更高,获得更高的灵敏度,进行更多级数的碎裂; 双径向检测器设计同时检测离子,离子检测速度更快,响应强度更高,信号更加稳定; 蛋白质组学 法医和临床分析 ·最大序列覆盖率,源自卓越的循环时间和灵敏度自动MS" 触发数据依赖中性丢失扫描 ·灵活的离子化模式、进样口和色谱解决方案 药物研发定量 .优异的离子统计学使定量稳定可靠 ..碰撞能量归一化获得最高工作效率为规范实验室提供同时定性和定量数据 ·持久稳定性适应复杂基质样品可靠定量 .正、负离子模式下同时定量和定性简便地操作提高实验室效率 代谢物鉴定 .·出色的 MS" 谱图质量和全扫描采集技术 低浓度代谢物结构确认,无需了解 MRM信息 数据依赖和动态排除技术可以从复杂样品中获得最多信息 数据采集 多种扫描方式 Thermo 离子阱提供丰富的采样模式,既有通用模板帮助快速建立分析方法,又有拓展功能满足深入分析的需要。 扫描方式 扫描原理 Data Dependent MS/MS 选择全扫描中满足条件的离子进行二级扫描 Nth Order Double Play 选择全扫描中响应前N强的离子进行二级扫描 Data Dependent Triple Play 全扫描后 Zoom 扫描,选择满足条件的离子进行二级扫描 Nth Order Triple Play 全扫描后 Zoom 扫描,选择响应前N 强的离子进行二级扫描 Data Dependent Neutral Loss MS3 在二级子离子与母离子满足预设的中性丢失的条件下触发三级扫描 Data Dependent lon Tree 对最多25种离子进行 MS至MS之间任意级数的扫描 Ion Mapping 自动生成裂解途径的 MS/MS 3-D图 Data Dependent Zoom Map 在 Zoom 扫描中选择响应最强的母离子进行二级扫描 Isotopic Data Dependent Scan 同位素丰度比与峰间距触发扫描 Charge State Screening 电荷态扫描 注: Zoom 扫描是通过降低扫描速度增加分辨率的一种离子阱扫描方式 目标杂质分析 杂质研究过程中通常需要对药物中的已知或目标杂质进行分析,离子阱的选择反应监测(SRM)可对杂质特定的母离子和子离子进行扫描,保证结果的特异性和准确性,连续反应监测(CRM)更可对杂质特定的母离子,子离子和多级离子进行扫描,获得更高的灵敏度和抗干扰能力。下图中采用 SRM 对目标化合物的母离子 m/z 258 和子离子进行扫描,可看到在 2.65min 有一明显色谱峰,在采用 CRM 进一步对目标化合物的三级离子m/z 133进行扫描后,2.65min 的化合物背景干扰明显降低,信噪比有了大幅提升。 图4.多级质谱提供更高的特异性与灵敏度 未知杂质的鉴定是杂质研究工作中非常重要的一部分内容,因为结构未知,如何采集到准确的杂质母离子和多级质谱信息成为结构解析的前提和关键。数据关联多级质谱及动态扫描功能可以实现对未知杂质信号的采集。 如下图所示,离子阱通过一级扫描,获得化合物质谱信息,根据质谱响应强弱自动选择母离子进行多级质谱扫描,一次进样即可获得杂质多级质谱信息。 图6.数据关联扫描采集洛哌丁胺多级质谱数据 动态排除功能:在药物杂质研究中,常涉及到从液相方法到液质方法的转移过程,而液质方法因为流动相与液相不同,往往无法在短时间内将所有杂质分离,离子阱具有动态排除功能,开启后可以对所有共流出杂质进行多级碎裂,以应对色谱未完全将杂质分离的情况。 在下图中,化合物 m/z 452和m/z 407发生了共流出,开启动态排除后,仪器首先对响应较高的 m/z 407进行二级碎裂,然后将 m/z 407 放入排除列表,在下一次全扫中,响应较高的 m/z 407 即作为排除项,转而选择响应较弱的 m/z 452 进行二级碎裂。所以在一个色谱峰内,即使有多个化合物存在,动态排除都能保证采集到每个化合物的多级质谱信号。 图5.数据关联扫描同时采集已知与未知杂质 在采用数据关联扫描对洛哌丁胺药物的分析中,离子阱通过全扫获得一级质谱信号,然后对响应最强的洛哌丁胺母离子进行二级碎裂,然后自动选则m/z 266 和 m/z 210 两个主要二级离子进行三级碎裂,紧接着对由二级离子 m/z 266产生的三级离子m/z 210 和 m/z 238进行四级碎裂。数据关联扫描可以在一次进样内,即自动完成多级质谱过程,无需预先知道样品中的化合物信息,提高了分析通量和数据信息量。 图7.动态排除采集共流出杂质组分 杂质的种类繁多,即使是相同元素组成的化合物,结构也可能完全不同,所以需要对采集到的数据进行有效的解析,对推测的结构式进行判断, Mass FrontierM为质谱谱图的管理、评估和解析提供精密的特性。它可广泛应用于小分子结构鉴定,应用范围涉及包括药物开发、杂质的分析和毒理研究过程中代谢产物的识别等广阔领域。 图8.Mass Frontier结构解析软件 MassFrontier 专业结构解析软件 使用 Massfrontier,研究人员可以方便的从已采集的数据中获取以下信息: ·化合物的裂解机理 因为杂质的结构和母药的结构往往类似或者具有渊源,所以了解母药的裂解规律可以帮助判断杂质的碎片结构,进一步推测出杂质的结构。以前的方法仅仅依靠研究者的个人经验,或者纯理论的计算,使得数据分析的重现性和准确性受到了限制。 Mass Frontier 所含有的 Fragmentation LibraryM碎裂机理谱图库是从现存的所有关于质谱的出版物中收集而来,几乎涵盖了所有已发表的文献。每一种机理,连同其化学结构,都经过人工和自动核对,然后连同标题、作者及信息来源等附带信息一块储存于谱图库中。谱图库所收集的信息,加上通用的电离、碎裂和重组规则,为碎裂机理的预测提供了有力的保障。Mass Frontier 还可以允许用户创建基于客户自定义碎裂机理上的谱图库,并能学会并运用这些机理来智能预测碎片分子。 图10. Fragmentation Library根据已发表文献提供霉酚酸酯杂质裂解机理 有关物质的检获 一些杂质组分会因为信号响应太低,或者形成的色谱峰不够尖锐,而被研究人员忽略,但是含量很低的毒性杂质严重的影响药物安全性,漏检不仅会极大的影响用药的安全性,也会间接影响到新药申报。 MassFrontier 的 Fragment lon Search (FISh) 可通过过滤无论是由理论裂解预测还是由实验 MS"质谱谱树获得的一组裂解碎片可对结构相似化合物进行快速筛选,通过杂质与母药的碎片比对查找,精确的找出所有有关杂质。 图11.Fragment lon Search (FISh)检索霉酚酸酯痕量杂质 线性离子阱多种解离技术对阿德福韦酯杂质谱的全面鉴定 前言 活性药物成分(API)和成品药的杂质分析是药物研发中不可或缺的一环。杂质的化学结构信息在评估毒性、改进合成途径,以及根据目标成药选择最佳剂型至关重要。 为保证药效与消费者的安全,世界各国的监管机构都制定了药物杂质分析的指引,清楚说明基于日服用量、使用时间,和药物靶标的限量标准。 LCMS 已经成为最常用的未知杂质分析技术。为了能在大量母药中识别并表征痕量杂质,具有高灵敏度、高扫描速度,并且能进行多级质谱分析(MS")的质谱仪必不可少。 在本研究中, Sigma-Aldrich 所售的研究级阿德福韦酯( adefovir dipivoxil, ADP) 被用来作为模型化合物进行API杂质分析。ADP 是广泛用于慢性乙肝病毒感染的一种抗病毒处方药。本研究中使用的 LCMS 系统由Thermo Scientific AccelaM UHPLC 以及 Velos ProM线性离子阱质谱仪构成。碎片信息通过结合应用 CID 与Trap-HCD 解离技术获得。数据处理通过软件 Mass FrontierM完成。 分析方法 材料与试剂 阿德福韦酯( Adefovir dipivoxil, CAS# 142340-99-6)从 Sigma-Aldrich 购得,产品号 A9730。 乙腈和水(Fisher);乙酸铵( Sigma-Aldrich,产品号73594-25G-F);甲酸 (Sigma-Aldrich,产品号33015-500ml)。 样品制备 梯度洗脱: ADP溶液,0.5mg/mL,用1 ml 20 : 80的乙腈和水混合溶剂溶解 0.5mg ADP 获得。 HPLC 方法 HPLC系统: Thermo Accela 1250 泵, 开放式Accela 自动进样器及 Accela PDA 色谱柱: Hypersil GOLD C18 2.1×150 mm, 3 pM,Thermo Scientific 产品号071399 柱温:35℃ 流速:0.5ml/分钟 进样体积:8ul 时间(min ) A% B% C% 0 80 10 10 12.0 20 70 10 14.0 20 70 10 14.1 10 80 10 15.0 10 80 10 15.1 80 10 10 19.0 80 10 10 流动相:A-水,B-乙腈, C-100 mM 乙酸铵,用乙酸调至pH5 质谱方法 质谱仪:配有 HESI-II离子源的 Velos ProTM线性离子阱 离子化条件:电喷雾,正离子模式 1.全扫模式 m/z 120-1000 amu/ Top5 dd MS/MS, HCDNCE 35% 2.全扫模式/按母离子列表 dd MS/ TOP 3 ddMS,CID/ Trap-HCD NCE 20% a. CID MS/ CID MS b. CID MS/HCD MS C. HCD MS"/ CID MS d.HCD MS/HCD MS 结果与讨论 l.全扫—Top5 HCD dd MS/MS 与“FISh” ADP 杂质谱分析流程由两次连续的LCMS实验构成。分析目标是为杂质鉴定和结构解析收集尽可能多的信息。第一个 MS 实验包括全扫描和后续的 Top5 HCD 数据依赖 MS/MS 扫描(图1)。接下来,数据通过 MassFrontier 当中的 Fragment lon Search (碎片离子检索, FISh) 算法进行处理,这是一个新颖的进行杂质检出及鉴定的方法,主要基于母离子解离模式的比较(图2a,b)。与母药拥有相同碎片的成分会被“FISh”识别出来,见图3。 NL: 2.71E8TICF: ITMS+cESI t E Full ms[125.00-1600.001MSAdefovirDipivoxil_Nov29_01 图1.阿德福韦酯的质谱总离子流图 图2.用Mass Frontier“FISh”算法检测出杂质成分 图3.“FISh”算法检测出的杂质成分的XIC 碎片离子进行 HCD MS°- 全扫, CID dd MS² (设定母离子列表),然后对前三的 MS?碎片离子进行 CID MS3- 全扫, HCD dd MS²(设定母离子列表),然后对前三的 MS²碎片离子进行 CID MS°-全扫,HCD dd MS’( 设定母离子列表),然后对前三的 MS²碎片离子进行 HCD MS 当归一化的碰撞能量水平相同时, Trap-HCD 比 CID生成的碎片谱图信息更丰富。Trap-HCD 没有低质量数歧视效应,见图4。CID MS" 能够提供步进的裂解信息,对结构解析非常有价值,见图5, 6。 Full 图4.阿德福韦酯在相同的25%NCE水平下的CID & HCD MS谱图 图5.杂质m/z558.19的CID与HCD谱图比对 图6.杂质 m/z 388.13的CID和HCDMS2,MS谱图 ADP Al A2 A5 图 7. Sigma-Aldrich所售研究级阿德福韦酯(adefovir dipivoxil)样品中所含杂质的可能结构式 根据丰富的 HCD、CID MS²和MS°碎片信息(见图7),对鉴定出的杂质化合物进行了结构预测。每个杂质组分的精确质量数和元素组成通过台式Orbitrap QExactiveM质谱仪的高分辨数据确认。 表1.杂质组分的精确质量数和元素组成通过Q Exactive 高分辨数据确认 峰识别号 分子式 理论值(M+H) 实测值(M+H) 误差(ppm) 母离子 C20H32N,O:P 502.2061 502.2062 0.2 A1 C14H22N,O。P 388.1380 388.1378 -0.6 A2 C12H25N02 216.1958 216.1958 0.2 A3 C19H30N,OP 472.1956 472.1958 0.6 A4 C15H24N,O。P 402.1537 402.1535 -0.4 A5 CHN,O, 250.1299 250.1296 -0.8 A6 C16H26N,O,P 416.1693 416.1690 -0.9 A7 C19H29N,OP 486.1748 486.1750 0.1 A8 C35H54N10014P2 901.3369 901.3375 0.6 A9 C21H34N,O:P 516.2218 516.2214 -0.8 A10 C22H36N,OP 530.2374 530.2373 -0.2 A11 C25H0N,O,P 586.2636 586.2632 -0.7 A12 C26H42N,O10P 616.2742 616.2738 -0.6 A13 C41H64N1001eP2 1015.4050 1015.4055 0.5 结论 两种解离技术-Trap-HCD 和 CID用被用来表征市售研究级阿德福韦酯( adefovir dipivoxil)样品中的十三种低含量杂质。当归一化的碰撞能量水平相同时, Trap-HCD 比 CID生成的碎片谱图信息更丰富。 Trap-HCD 不存在低质量歧视效应。另一方面,CID 能够提供逐级裂解信息和MS" 谱图,对于阐明子结构关联非常有价值。本研究的结果证明,结合数据后处理软件使用这两种互补的解离方式能够出色完成杂质鉴定与结构解析,提高了未知杂质分析的速度与可靠性。 应用 LCQ 离子阱质谱仪和 Mass Frontier 软件分析药物中间体的痕量杂质成分 前言 由于将一个新药带入市场的成本非常高,药物公司能够开发的药物数量就会受到限制。为此,在药物研发的早期,大多使用复杂的筛选技术来剔除那些没有潜力的候选药物。若要成功,必须对代谢物和杂质的吸收、分布、代谢、排泄和毒性(简称ADME/Tox) 做出快速和准确的评估来表征先导化合物。杂质样品的高通量分析对低浓度样品,尤其是生物基质中的低浓度样品提出了挑战。各种可能的修饰作用使数据解释进一步复杂化。 Finnigan LCQ 系列离子阱质谱仪具有高灵敏度、高选择性和复杂数据相关等操作性能,能很好的适应于药物中杂质分析的需求。在组合化学研究中能够快速采集、解析和分析结构数据,对化合物筛选工作的顺利进行是至关重要的。Mass Frontier,是热电用于解析和处理质谱图数据的高级软件包,配置该软件包,能够对所提供分子结构的碎裂途径给出预测。在本文的研究中,使用了碎裂和机理模块来确定一个先导药物关键中间体的三个杂质的结构。 目标 对一个先导药物的关键中间体的杂质的化学结构作结构鉴定。 实验条件 用于分析的药物样品由 Eisai 研究所提供。所有实验在 Finnigan LCQ 离子阱质谱仪上采用 APCI 模式完成。使用 FinniganSurveyorM液相色谱仪和 AQUASIL C18( 250×2 mm)色谱柱完成液相色谱分离分析。液相色谱条件:40%水和60%乙腈的流动相,等梯度洗脱,流速为300ul/ml, 不分流(进入质谱)。 Finnigan LCQ 质谱仪的离子源参数如下: 电离模式:正离子, APCI 加热毛细管温度:175℃ 蒸发温度:325° CAPCI电流: 5uA 鞘气压力:80个单位 辅助气压力:20个单位 Mass Frontier 软件提供了专为提高质谱图解析速度而设计的高级分析工具包。作为八个模块其中之一的碎裂和机理模块,能够根据用户提供的化学结构自动预测碎片途径和反应机理。基于模拟单分子离子离解反应的算法,碎裂和机理模块包含了针对电子轰击电离、质子化反应和化学电离等已知的反应机理。 碎裂和机理模块的主要功能是: 。核查所提供的化学结构与实验得到的质谱图之间的相关性 确认谱库检索给出的结果 ·识别在质谱图中最相关化合物的结构差异 此外,碎裂和机理模块可以模拟二级质谱实验。当用户输入指定化合物结构,就会生成一系列理论碎片离子,与二级质谱实验数据进行比较。在本研究中,对假设化学结构模拟产生的碎片离子与数据相关二级质谱实验观察到的子离子进行关联分析,确认了先导药物关键中间体中三个痕量杂质的结构。 讨论 对一个先导药物关键中间体的最近流程评价, Eisai研究所认为在开始下一步工作前对这些中间体杂质结构的深入分析是必要的。由于产权原因,图1仅给出了这个化合物的部分结构。注射20pL(含100ng/pL的药物中间体和其杂质)样品到色谱系统,洗脱分离 图1.关键药物中间体的部分结构图 后进入质谱仪中检测。LCQ 质谱仪采用了数据相关二级质谱扫描模式,在这个模式下,一次运行分析就可以采集到全扫描质谱和二级质谱数据,而不需要预先指定二级质谱的母离子质量数。 图2a给出了分析的总离子流图。药物中间体在质荷比m/z 486处有很强的信号,对应保留时间是8.5分钟。另外观察到背景离子(与样品不相关) m/z 391, 392 和393。从总离子流图中扣除这些背景离子后,得到三个杂质m/z分别为 538,488和556的色谱图(见图2b)。根据质量数差异和同位素分布图,推断三个杂质为在药物中间体的双键上分别添加了 CIOH, H,和CI(在图1中以红色标记)。 图2.(a)保留时间在8.5分钟的药物中间体(m/z486)的全扫描总离子流图(b)扣除背景(m/z391,392,and393)和药物中间体(m/z486和487)后的低浓度杂质(m/z538,488和556)离子流图 图3为三个杂质的推断结构,图4为三个杂质测得的同位素分布和推断结构同位素分布的比较,图5为药物中间体和三个杂质的提取离子色谱图。两个含氯杂质的信号强度是未修饰中间体的0.1%。由于仪器灵敏度和信噪比高,四个化合物可在一次数据相关的二级质谱实验被检测到。动态排除是数据相关采集的又一个特点,低含量成分即使在和高强度成分共同洗脱时,也能够采集其二级质谱数据,这种功能适合低含量杂质分析的要求。 如果没有动态排除功能,就采集不到二氢杂质的二级质谱数据,因为与二氢杂质共同洗脱的未修饰中间体的强度更高。在二级质谱数据扫描中,排除列表中包括了 m/z 391,392,和393的离子,以避免背景离子的二级质谱分析。由于使用数据相关采集数据,就不需要在方法中输入指定二级质谱扫描的母离子质量数。这样就避免了先进行全扫描实验,然后手动查找二级质谱扫描需要的母离子质量数。对于低浓度成分分析,这个过程费时且造成实验失误。图6中,在与碎裂和机理模块预测结果进行比较前后, Mass Frontier 谱图管理窗口可以显示采集到的药物中间体的二级质谱数据。特别是输入药物中间体化学结构后,软件就使用已知的单分子离解反应模式来预测可能生成的二级质谱碎片离子。然后这些理论预测的二级质谱碎片离子与实验 数据进行匹配分析。图6为程序给出的所有的主要二级质谱碎片峰,证明了碎裂和机理算法对给定化学结构二级质谱预测的有效性。 图7为与预测的碎片离子相比较后的三个杂质的实验二级质谱图。Mass Frontier 的预测是基于图3中三个杂质推断的结构给出的。和图6一样,如预测的碎片离子和实验二级质谱中的离子匹配用红色标记。可以看到,实验得到的二级质谱的所有主要离子都被红色标记,这有力支持了所推断结构的有效性。表1汇总了Mass Frontier 软件预测碎片结构和实验二级质谱的相关性结果,来验证图3推断的杂质结构。为了理解如何获得到这样的结果,必须意识到除了取代发生的位置(图1和图3红色标识),所提议的药物中间体结构和三个杂质结构是相似的。因此,如果实验得到的四个化合物的二级质谱中,每个化合物都有特定的碎片离子,而 Mass Frontier 预测能给出相同的裂解机理,那么所提议的三个杂质结构就是正确的: ·如果 Mass Frontier 软件预测碎裂机理生成的碎片结构不包含取代位,那么在实验得到的四个二级质谱图中应有相同质荷比的碎片离子。 如果 Mass Frontier 软件预测碎裂机理生成的碎片结构包含了取代位(即如果实验得到的二级质谱图中药物中间体的碎片离子的质荷比为M,那么在二氢,氯羟基,,二氯取代杂质分别应该有 M+2, M+52 和M+70质荷比值),那么碎片离子的质荷比应存在取代基质量数的差异。 图3.推断三个杂质的化学结构为:(a)羟化氯杂质(b)二氢杂质和(c)二氯杂杂 图4.三个杂质(a)羟化氯杂质(b)二氢杂质和(c)二氯杂质的加氢离子的实验和理论同位素分布比较图。左面为实验得到的全扫描同位素分布图,右面为根据给定的元素组成用XcaliburTM 软件中的IsotopeViewer算出的理论同位素分布图。 图5.药物中间体和三个杂质的提取离子色谱图,杂质以相对峰面积计算。 图6:(a)药物中间体实验得到的二级质谱图。(b)与理论预测的碎片离子相匹配,其中由Mass Frontier 预测的碎片离子在谱图上以红色标记。 图7:与预测生成的碎片离子匹配后得到的实验二级质谱图(a)氯羟基杂质(b)二氯杂质和(c)二氢杂质, 与Mass Frontier 软件预测匹配的实验碎片离子用红色标记 在表 1, Mass Frontier 软件指定具有相同裂解机理的碎片离子被以相同颜色加重。这样可以从表中看出,在所有情况下,由Mass Frontier 预测形成机理得到的有关联的碎片离子要么有相同的实验质荷比,要么有与取代基差异的实验质荷比,这依赖于 Mass Frontier 预测的碎片结构是否有取代位。通过观察证明了所推断的杂质结构的有效性。 在数据相关二级质谱模式和动态排除的支持下,检测和表征了含量在0.1%或以下的专利药物中间体的三个杂质。同位素分布和质量差说明了推断结构的合理性,并由Mass Frontier 所验证。通过 Mass Frontier 预测碎片离子和实验得到的二级质谱图离子的比较,确定了所建议的三个杂质结构。该分析支持以下的结论:三个杂质都来自于药物中间体某双键位置的化学取代。 ·所要分析的杂质含量是母体成分丰度的0.1%以下,这是法规所要求的。Finnigan LCQ 离子阱质谱仪具有高灵敏度和高选择性,数据相关扫描模式,是成功完成杂质分析的必备工具。 Mass Frontier 谱图管理和碎裂机理模块技术能够快速方便地完成结构分析,并能对推断的杂质结构予以确认。 表1. Mass Frontier软件结构预测汇总 化合物 实验得到的二级质谱碎片离子 Mass Frontier 预测 的碎片结构含取代位吗?(YES/NO) 药物中间体 258 不是 316 是 396 不是 428 不是 454 是 氯羟基取代物杂质 258 不是 368 是 396 不是 428 不是 506 是 二氯取代物杂质 258 不是 386 是 396 不是 428 不是 524 是 二氢取代物杂质 318 是 456 是 注解: 1.二氢取代杂质在中间体药物的峰尾洗脱流出,在质谱图中对m/z 488信号有很 大贡献。由于 m/z 488 是二氢取代杂质二级质谱图的母子子,因此必须在二氢取代杂质的二级质谱中扣除将药物中间体部分,同时也去掉了二者相同的碎片离子。因此,表1和图7仅包含了与药物中间体不同质量碎片的二氢取代杂质的碎片离子。 2.见图1和图3详细说明。 药物杂质分析部分客户文章列表 Title Authors Publications Publication Year Stability-indicating assay method for determination of actarit, process related impurities and degradation products: Insight to stability profile and degradation Abiramasundari A, Joshi RP, Jalani HB J. Pharm. Anal. 2014 pathways LC-MS/MS characterization of forced degradation products of zofenopril Ramesh T, Rao PNageswara J. Pharm.Biomed. Anal. 88(25): 609-616 2014 ESI-MSn and LC-ESI-MS studies to characterize forced degradation products of bosentan and a validated stability-indicating LC-UV method Bansal G, Singh R, Saini B, et al J Pharm Biomed Anal. 72:186-197. 2013 Characterization of impurities in tylosin using dual liquid chromatography combined Chopra S, Schepdael A Van, Hoogmartens J, Talanta. 106:29-38. 2013 with ion trap mass spectrometry et al FORCED DEGRADATION STUDY OF TORASEMIDE: CHARACTERIZATION OF ITS Jovic Z, ZivanovicL, Protic A, et al J. Liq. Chromatogr. Related Technol. 2013 DEGRADATION PRODUCTS 35(15):2082-2094 Investigation and structural elucidation of a process related impurity in candesartan cilexetil by LC/ESI-ITMS and NMR Raman B, Sharma BA, Mahale G, et al J.Pharm. Biomed. Anal. 56(2):256-267. 2011 Mass spectrometric characterization of gentamicin components separated by the new European Pharmacopoeia method Li B, Schepdael A Van, Hoogmartens J, et al J. Pharm. Biomed. Anal.55(1):78-84. 2011 Identification of novel rapamycin derivatives as low-level impurities in active pharmaceutical ingredients Zech SG, Carr M, Mohemmad QK, et al J. Antibiot.64:649-654 2011 Development and validation of indirect RP-HPLC method for enantiomeric purity determination of d-cycloserine drug substance Karthikeyan K, Arularasu GT, Ramadhas R J. Pharm. Biomed. Anal.54(4):850-854 2011 Forced Degradation of Betamethasone Sodium Phosphate Under Solid State: Formation, Characterization, and Mechanistic Study of All Four 17,20-Diastereomers of Betamethasone 17-Deoxy-20-Hydroxy-21-0ic Acid Li M,Wang X, Chen B J. Pharm. Sci.98(3):894-904. 2009 of Betamethasone 17-Deoxy-20-Hydroxy-21-0ic Acid 附录 杂质的分类:ICH指南将杂质分为有机杂质、无机杂质、残留溶剂三大大。 有机杂质: 包括工艺中引入的杂质和降解产物等,它们主要起源于起始原料及其本身所含杂质、生产过程中带入的合成中间体与副反应产物、成品在储存过程中产生的降解产物,辅料中带入的杂质或辅料降解产生的杂质,及药物与包材相互作用产生的杂质。有机杂质的化学结构与活性成分的分子式类似或具渊源,通常称为有关物质。 有机杂质的限度确定:原研药一般已经对杂质的安全性做了全面的研究,故对于仿制药,需要与原研药进行充分的杂质比对和研究,分析杂质的种类和含量,并结合原研药的质量标准,对杂质进行控制,如果因为工艺和处方的不同导致仿制药的杂质与原研药不同,则仿制药中的新杂质需要在表1-1和1-2的限度以内,如果新杂质超出表中限度,或者仿制药的杂质含量明显高于原研产品,则需要通过优化处方和工艺,使杂质的含量降到规定的质控限度以内,如果无法降到规定限度,则需要对超过限度的杂质进行相应的安全性研究。 表2.原料药的杂质限度 最大日剂量 报告限度 鉴定限度 质控限度 ≤2g 0.05% 0.10%或 1.0mg 0.15%或1.0mg >2g 0.03% 0.05% 0.05% 表3.制剂的杂质限度 报告限度 鉴定限度 质控限度 最大日剂量 限度 最大日剂量 限度 最大日剂量 限度 ≤1g 0.10% <1mg 1.0%或5pg <10mg 1.0% 或 50pg 1mg-10mg 0.5%或 20ug 10mg-100mg 0.5%或 200pg >1g 0.05% >10mg-2g 0.2%或2mg >100mg-2g 0.2%或 3mg >2g 0.10% >2g 0.15% 有机杂质其中一类会直接破坏DNA活性,增加病人癌症风险的遗传毒性药物杂质统称为基因毒性杂质,该类杂质包括生产过程产生的杂质或者储存过程产生的降解产物,根据 FDA 和 EMA规定,基因毒性杂质的质控限度远低于一般有关物质,建议接受阈值参见 FDA 和 EMA 指南文件。 ·无机杂质: 原料药及制剂生产或传递过程中产生的杂质,通常是已知的。来源可能包括生产过程中的试剂,如催化剂,配位体等;其他阶段引入的金属,如反应容器,传递管道,过滤材料等 ·残留溶剂: 原料药及制剂生产过程中使用的有机溶剂,例如原料药最后纯化结晶过程会残留少量有机溶剂,很难彻底去除,此类残留溶剂往往对人或者环境有害,或造成原料药降解。残留溶剂一般具有已知毒性, ICH,USP 和 EP都规定了残留溶剂的限量。ICH指南将药物中的残留溶剂分为四类,一类溶剂(苯,四氯化碳等)毒性最大,应避免使用,,二类溶剂(乙腈,三氯甲烷,环己烷等)毒性较大,应限制使用,三类溶剂(醋酸,丙酮,甲酸等)应根据药品 GMP 或其他质量要求进行限制,四类溶剂(石油醚,三氟醋酸等)尚无足够的毒理学资料。 。其他: 外源性污染:微生物,内毒素等 多晶型:晶型杂质 对应异构体:手性杂质 对:江峥 Thermo 质谱资源中心 ·Thermo Scientific 品牌下色谱与质谱部,前身为著名的质谱先驱-美国菲尼根 (Finnigan) 质谱仪制造商。从1967年成立至今的四十多年来,一直以无与伦比的研究成果保持着质谱技术的世界领先地位。为农业、环保、医药卫生、检验检疫、石油化工、制药、公安及生命科学等研究领域中的广大分析、研究工作者提供最完善的解决方案,成为了最可信赖的合作伙伴 ·有关 Thermo 离子阱质谱的更多信息可访问 http://www.thermoscientific.com/en/products/ion-trap-lc-ms.html 赛默飞世尔科技(中国)有限公司 免费服务热线:800810 5118400 6505118(支持手机用户) Thermo 赛默飞的离子阱技术有效解决了药物杂质研究难题,其高灵敏度和宽广的动态范围能够采集到药物中微量杂质的有效质谱信息;离子阱的多级质谱能力可以获得杂质的“指纹图谱”-- 离子树,结合强大的结构解析软件可以对工艺杂质或降解产物的结构进行深入有效的剖析;结合高效的色谱分离、深入的多级质谱分析和智能化的解析软件,赛默飞建立了基于离子阱质谱技术的药物杂质分析解决方案。
确定













还剩18页未读,是否继续阅读?
赛默飞质谱分析为您提供《阿德福韦酯中C12H25N1O2检测方案(液质联用仪)》,该方案主要用于原料药中限度检查检测,参考标准--,《阿德福韦酯中C12H25N1O2检测方案(液质联用仪)》用到的仪器有赛默飞LCQ Fleet 离子阱液质联用仪、赛默飞LTQ XL线性离子阱质谱仪
相关方案
更多
该厂商其他方案
更多