方案详情
文
本文对制备“无核糖核酸酶”水的两个主要过程进行了对比,这种比较给予有关RNA提取、RNA分解、RNA稳定性测试以及核糖核酸酶剂量等几种试验得到的结论。并对比了通过超滤法来清除RNases和利用DEPC化学钝化RNase的两种方案。密理博纯水系统的超滤柱可以有效地替代的DEPC法,提供“无核糖核酸酶”水
方案详情

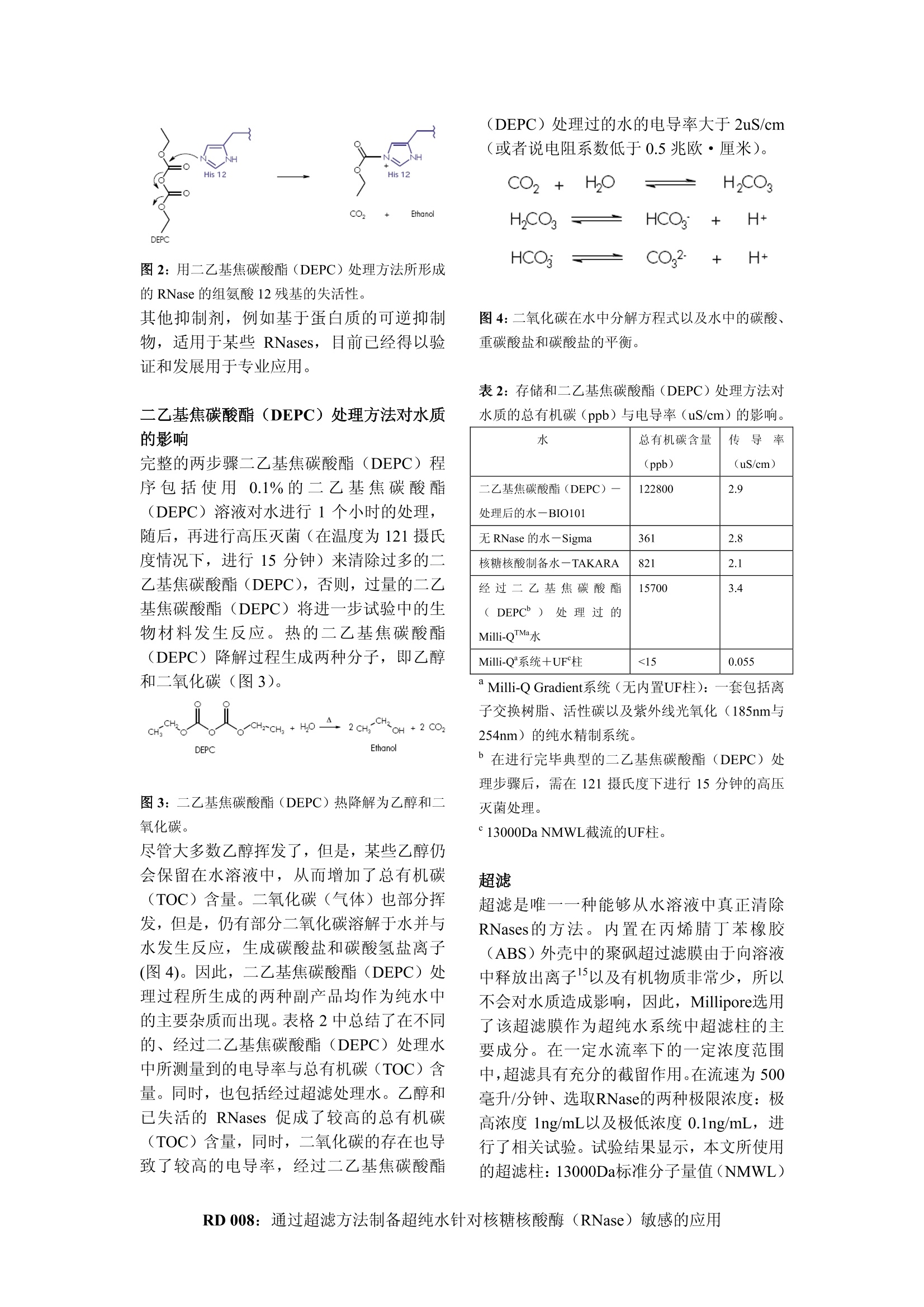
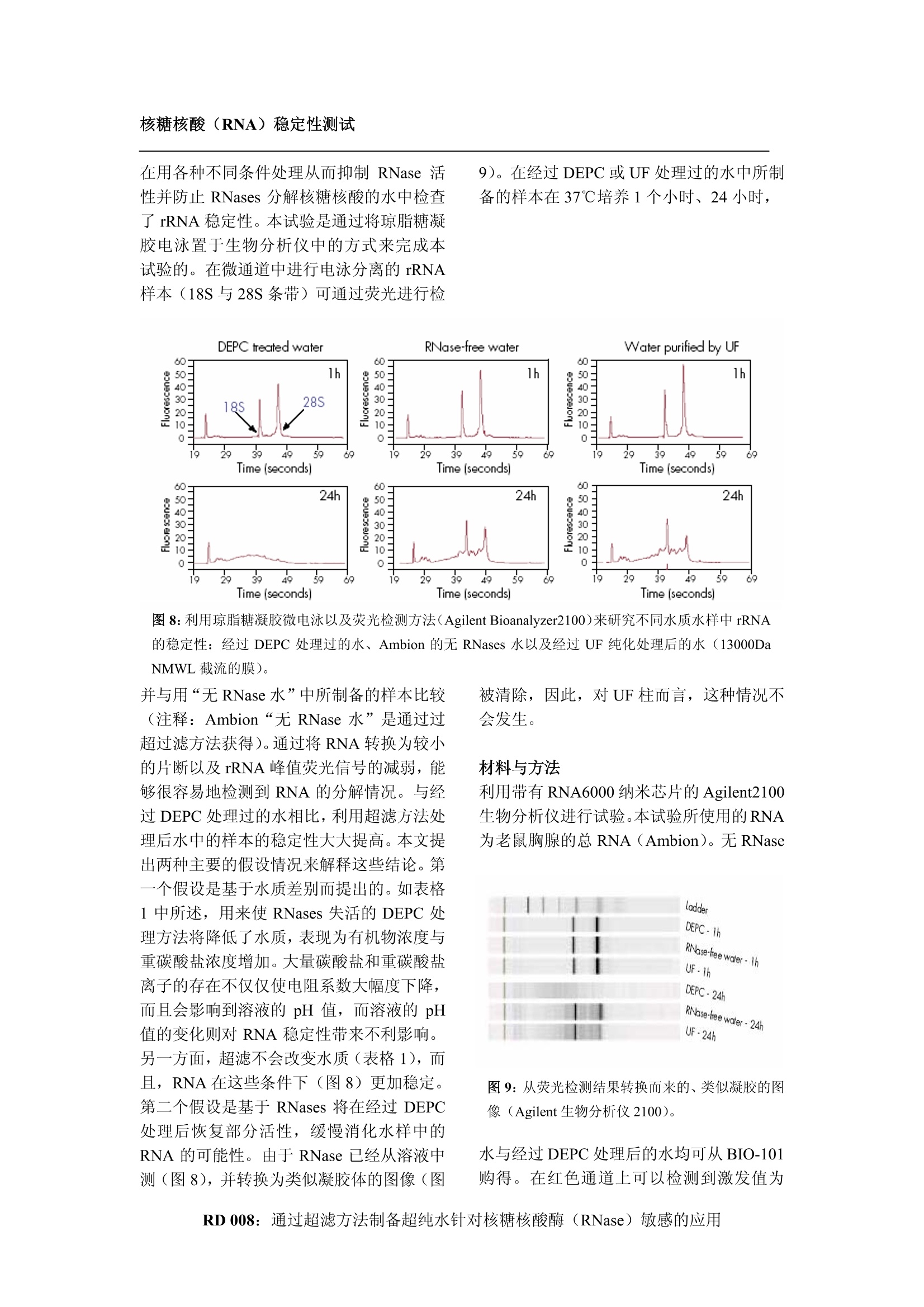
The R&D NotebookA publication of the Laboratory Water Division of MilliporeRD 008 杉糖核酸(RNA)稳定性测试 通过超滤法制备适合对核糖核酸酶(RNase)敏感的应用的超纯水 Stephane Mabic, Ichiro Kano 法国,圣康丁昂伊夫利纳,密理博公司实验室纯水部门研发中心 摘要:为了顺利地进行涉及到核酸,特别是 RNA 的分子生物学试验,必须抑制核糖核酸酶(RNases)的降解。本文对制备“无核糖核酸酶”水的两个主要过程进行了对比,这种比较基于有关 RNA 提取、RNA 分解、RNA 稳定性测试以及核糖核酸酶剂量等几种试验得到的结论。并对比了通过超滤法来清除核糖核酸酶与利用二乙基焦碳酸酯(DEPC)化学钝化核糖核酸酶的两种方法。密理博纯水系统的超滤柱为二乙基焦碳酸酯 (DEPC)处理方法的有效替代方案,可按需提供高纯度无核糖核酸酶水。 简介 核糖核酸酶或者RNases 由一个很宽范围内的降解酶组成,这些酶广泛存在于大多数有机体以及大多数器官和人体体液中的。在这些蛋白质中,存在着大小不一(表格1),特别是功能不同的酶。几十种不同类型的RNases活跃在不同生物条件下(例如, pH值、温度以及离子强度等)的核酸酶底物上。1RNases 的实例包括人体中²所发现的RNases1、2(神经毒素(EDN))、3嗜酸粒细胞阳离子蛋白(ECP)、4与5,同时,也包括在各种不同微生物中所发现的RNasesI、Ⅱ、Ⅲ、P、PH、R、D、T、BN、E、M等. 表 1: RNase多样性之实例 名称 来源 MW【Da】 最有pH值 RNase A 胰腺与牛痘 13700 7-7.5 RNase 1 胰腺与人体2 14000 8 RNase 1 细菌3 27000 RNase ⅢI E.Coli3 25600x2 一 RNase T2 A. Oryzae4 36200 4.5 RNases的主要作用是用来降解核糖核酸 (RNA)。某些被称为核酸外切酶的核糖核酸酶将从外部极点开始此降解过程,并且持续降解核酸分子,同时,被称作核酸内切酶的核糖核酸酶将在核糖核酸(RNA)分子的一定点处开始进行降解。RNases具有不同的种类和酶作用物。例如,人体RNases2 与 3专用来降解单链核糖核酸,而牛胰腺RNease A能够降解单链脱氧核糖核酸、双链脱氧核糖核酸以及环型脱氧核糖核酸。3由于RNase A酶底物作用物范围较广,因此,RNase A是一种常用于质量试验的核糖核酸酶,这些质检方法旨在抑制或者检测RNase活性。 这些降解酶常用于降解异类核糖核酸(RNA),同时也是基因表达机制的一个组成部分:核糖核酸酶用于信使核糖核酸(mRNA)、核糖体核糖核酸(rRNA0 以及转移核糖核酸(tRNA) 的成熟步骤中,同时也可用于通过降解信使核糖核酸(mRNA)和未曾使用的核糖核酸(RNA)的常规方法。最近,通过科学研究工作,已经获得了证证来证明RNases在主体防御 (host defense)?以及诸如抗肿瘤活性、神经毒性以及免疫抑制性等的生理活动性中所起到的作用。 尽管抑制RNase活性是满足了大多数试验的要求,但是,在某些分子生物学保护化验过程中,仍使用了核糖核酸酶,达到避免受到外部核糖核酸(RNA)或者脱氧核糖核酸(DNA)的污染的目的。核糖核酸酶无处不在并且属于一种非常有效的酶,同时,在pg/L浓度至ng/L浓度之间具有一定的活性。因此,在避免受到外部污染源污染例如,体液(唾液与汗液)、管尖与管、实验室表面或者净化水和缓冲器78等方面,核糖核酸酶具有极其重要的作用,在分子生物学或者生物工艺学试验需要使用到核糖核酸和/或脱氧核糖核酸(RNA和/或 DNA)时,几乎每次均需要清除 RNases。此类临界试验的实例,如PCR(聚合酶链反 抑制 RNase 活性 高压灭菌步骤 高压灭菌(在121摄氏度下连续灭菌3个小时)不能有效地效解RNases, 即使是在180摄氏度下进行高压灭菌处理4个小时之后,RNases仍会保持某些活性。而且,高压灭菌除了只能使这些蛋白质部分变性外,还能够高压消灭细菌,从而将更多的RNases释放到媒介中。变性酶也能够恢复到初始形式并且能够再次恢复部分活性。 二乙基焦碳酸酯(DEPC) 分子机制 利用二乙基焦碳酸酯 (DEPC)处理方法使化学酶失活是用来抑制水溶液中 RNase 活性的最常见方法。二乙基焦碳酸酯(DEPC)是一种能够使 RNases 失活的可疑致癌物。基于分子结构基础10,11,1225二发现的RNases 的各种不同的催化机理将有助于更好地理解在二乙基焦碳酸酯(DEPC)与RNases 之间发生的化学反应。我们最熟悉的催化机理之一指的是 RNase AA(EC 3.2.27.5)13,14,是一种124氨基的核酸内 应)以及反转聚合酶连锁反应 (RT-PCR),质体的制备、互补 DNA 殖系基因库(cDNAlibrary)、体外翻译 (In vitro translation)、基因表达、RNA 印迹法以及体外受精。本论文阐述了如何抑制试验用的水溶液中RNase 的活性。探讨了研制并用来抑制RNase 活性的三种主要方法:在使用抑制剂基础上的酶变性作用;通过采取超过滤方法而进行的酶的清除。同时,更加详细地研究并比较了两种主要的方法:利用焦碳酸二乙酯(DEPC)处理方法与超过滤方法(UF)而抑制酶的活性。本文所阐述的是利用内置超滤柱(在Milli-QPF系统中的PyrogardTM5000柱)和取水点(Point-of-use)-次性用超滤柱(Milli-Q Gradient 系统上所使用的 PyrogardD柱),许多试验方案中均采用了这两种技术:测量各种不同水源中RNase 的含量、RNase 剪切化验、核糖核酸稳定性测试以及核糖核酸完整性测试。 切酶。在常规酶机理中,组氨酸残基(His 12)——本机理中酶活性部位的一个关键氨基酸,在RNA 分子主链的核糖2位置与羟基(OH)发生反应(图1)。反过来,这也造成了磷酸二酯键(phosphodiester bond)的断裂,并生成两片核糖核酸。当酶与二乙基焦碳酸酯(DEPC)发生作用时,组氨酸12将与二乙基焦碳酸酯(DEPC)分子发生反应,形成共价氨基甲酸盐型链接(图2),从而不再与核糖核酸分子发生反应。酶将永久性失活,但是,无法从溶液中清除此酶。 图1:用RNase A 进行 RNA 降解的常规催化机理。组氨酸残基(His 12 与 His119) 属于 RNase A 活性部位的两个关键性氨基酸,并参与了化学反应。 图2:用二乙基焦碳酸酯(DEPC)处理方法所形成的 RNase 的组氨酸12残基的失活性。 其他抑制剂,例如基于蛋白质的可逆抑制物,适用于某些 RNases,目前已经得以验证和发展用于专业应用。 二乙基焦碳酸酯(DEPC)处理方法对水质的影响 完整的两步骤二乙基焦碳酸酯 (DEPC) 程序包括使用0.1%的二乙基焦碳酸酯(DEPC) 溶液对水进行1个小时的处理,随后,再进行高压灭菌(在温度为121摄氏度情况下,进行15分钟)来清除过多的二乙基焦碳酸酯(DEPC),否则,过量的二乙基焦碳酸酯 (DEPC) 将进一步试验中的生物材料发生反应。热的二乙基焦碳酸酯(DEPC) 降解过程生成两种分子,即乙醇和二氧化碳(图3) 图3:二乙基焦碳酸酯 (DEPC)热降解为乙醇和二氧化碳。 尽管大多数乙醇挥发了,但是,某些乙醇仍会保留在水溶液中,从而增加了总有机碳(TOC)含量。 氧化碳(气体)也部分挥发,但是,仍有部分二氧化碳溶解于水并与水发生反应,生成碳酸盐和碳酸氢盐离子(图4)。因此,二乙基焦碳酸酯(DEPC)处理过程所生成的两种副产品均作为纯水中的主要杂质而出现。表格2中总结了在不同的、经过二乙基焦碳酸酯 (DEPC)处理水中所测量到的电导率与总有机碳(TOC)含量。同时,也包括经过超滤处理水。乙醇和已失活的 RNases 促成了较高的总有机碳(TOC)含量,同时,.二氧化碳的存在也导致了较高的电导率,经过二乙基焦碳酸酯 (DEPC) 处理过的水的电导率大于2uS/cm(或者说电阻系数低于0.5兆欧·厘米)。 图4:二氧化碳在水中分解方程式以及水中的碳酸、重碳酸盐和碳酸盐的平衡。 表2:存储和二乙基焦碳酸酯(DEPC)处理方法对水质的总有机碳(ppb) 与电导率(uS/cm)的影响。 水 总有机碳含量(ppb) 传导率(uS/cm) 二乙基焦碳酸酯(DEPC)-处理后的水一BIO101 122800 2.9 无RNase 的水Sigma 361 2.8 核糖核酸制备水一TAKARA 821 2.1 经过二乙基焦碳酸酯 ( DEPC)处理过的Milli-QTMa水 15700 3.4 Milli-Q°系统+UF柱 <15 0.055 “Milli-QGradient系统(无内置UF柱):一套包括离 子交换树脂、活性性以及紫外线光氧化(185nm与 254nm)的纯水精制系统。 °在进行完毕典型的二乙基焦碳酸酯(DEPC)处理步骤后,需在121摄氏度下进行15分钟的高压灭菌处理。 °13000Da NMWL截流的UF柱。 超滤 超滤是唯-一种能够从水溶液中真正清除RNases的方法。内置在丙烯腈丁苯橡胶(ABS)外壳中的聚砜超过滤膜由于向溶液中释放出离子15以及有机物质非常少,所以不会对水质造成影响,因此,Millipore选用了该超滤膜作为超纯水系统中超滤柱的主要成分。在一定水流率下的一定浓度范围中,超滤具有充分的截留作用。在流速为500毫升/分钟、选取RNase的两种极限浓度:极高浓度 1ng/mL以及极低浓度 0.1ng/mL, 进行了相关试验。试验结果显示,本文所使用的超滤柱:13000Da标准分子量值(NMWL) 截留的膜,当浓度为0.1ng/mL时,在超过200L容量(图5)情况下,能够完全阻止RNase A的渗透。在两种试验条件下,在超过滤器上所收集的RNase A的数量分别为39mg与22mg。当浓度为 1.0ng/mL情况下,在体积达到100L以后,检测到RNaseA的浓度剧增。 总量(升) 图5:在较大体积情况下对 RNase A 进行超滤处理。 通过强化存贮在容器中的反渗透水中的RNase A (Roche Diagnostics 109 142)浓度为 1ng/mL (A与B)以及 0.1ng/mL(利用Ambion 无 RNase 水对浓度为 1ng/mL 的溶液进行稀释而成)(C与D),从而制备此溶液。在流速为500毫升/分钟情况下,通过使用点超滤装置来实现过滤处理,同时,利用 Ambion RNaseAlertTM 荧光测定测试来监控 RNase 活性。 结论 不同水样中的RNase含量 在取自各个不同纯化阶段的水样中测试RNase活性。这里的试验测量极限值为0.003ng/mL。本检测方法使用了可分解的、带有荧光标记的 RNase 酶底物(图6)。修饰后的核糖核酸寡核苷酸将由 RNase 进行降解,同时,被绿色荧光探针释放出。只有含有 RNases 的样本方能在本试验中显示出绿光,而不含有 RNases 的样本不会发出荧光。荧光的含量与 RNases 存在的数量成正比,该数值能够使用荧光计进行测量。本试验为检测 RNase 提供了一种快速、定量测试方法。 图6:荧光RNase 检测工具示意图 表格3中给出了根据各种不同水样而得出的结论。结论1和结论2、采取 DEPC 方法所生成的水以及无 RNase 水分别用作控制工具。在这两种情况下, RNase 含量低于检测限(小于0.003ng/mL)。在严格条件下进行这些试验的重要性已经与palm-drop-and-recovery 测试(结论3)进行了清晰的阐述,这个实验表明在与皮肤接触时,水很容易受到高含量的核糖核酸酶的污染。自来水中RNase 的数量(结论4)相对较低,这是由于在自来水中所发现的细菌污染物质(是核糖核酸酶的主要来源)含量较低。综合运用电流连续去离子(EDI)与反渗透技术(结论6)在清除大多数酶过程中,要比单独使用反渗透技术(结论5)有效。然而,在任何情况下,水在存储以后,均可测量到浓度较高的 RNase, 这可能是因为孳生了某些细菌的结果。很显然, RNase 在水中的含量大幅度提高,会使水变得浑浊(结论8)。利用双波长(185nm+254nm) 紫外线灯进行的有机分子光氧化方法应用到纯水系统(结论9)中,的确降低了RNase 浓度。配备了UF 膜(结论7与结论10)的系统在清除 RNases 方面非常有效,而 RNases浓度也均低于这些结论中的检测限值。根据这些结论,我们可以看出,除非与水纯化过程中的特定阶段有关,否则,水样中的 RNases 数量与水的滞流和存储期间可能出现的细菌污染之间的关联很大。 表3水纯化过程的各个不同阶段中 RNase 的浓度。 Result Water type / treatment RNase concentrationng/mL 1 RNase-free° <0.003 f 2 DEPC-treated· <0.003 3 RNase-free water dropped on palm and recovered 0.390 4 lap water 0.019 5 Reverse Osmosis system+ reservoir 0.018 to 0.470 6 Elixdsystem +reservoir 0.008 to 0.016 7 Reverse Osmosis system +reservoir + UF cartridge° <0.003 8 Milli-Q Gradient system after power off for 90 days 0.440 9 Milli-Q Gradient system undernormal conditions of use <0.003 to 0.012 10 Milli-Q Gradient system +UF cartridge <0.003 注释: a从Ambion 购得。bMillipore RiOsTM16 系统。c从所采取的水样中样入到Millipore60L 聚乙烯容器中的纯净水。dMillipore Elix10 系统综合采用了反渗透技术与电流连续去离子技术。e带有13000 Da NMWL截流的MIllipore Pyrogard D UF 柱。f“检测限值 0.003ng/mL”. 材料与方法 使用Ambion RNaseAlert 测试工具。培育时间延长为3个小时从而达到 0.003ng/mL检测限值。浓度为 10ng/mL 的 RNase Ambio标准液用 Ambion 无 RNase 水进行稀释,从而获得校准曲线,浓度分别为 0.025ng/mL、0.05ng/mL 以及 0.1ng/mL。使用 SFM25,Kontron 仪器荧光计,按照协议的要求,激发波长设定为 490nm, 而发射波长则设定为520nm。 Rnase 稳定性试验 本试验的目的是为了显示超滤在从水溶液中清除 RNases 的效率和保护 RNA 不受到RNases 的分解。用 4ng/mL RNA 溶液 10uL注入样品,并在37摄氏度情况下培育1个 小时。随后,利用琼脂糖凝胶电泳来监控分解过程(图7)。利用下面所列示的方法,对如下溶液进行了分析: RNase A 溶液(1ng/mL、lane 1、2以及 0.1ng/mL、Lane 3、4)作阳性对照,同时,经过 DEPC 处理过的水作阴性对照 (lane9、10),随后,浓度为 1ng/mL (lane5与6)以及 0.1ng/mL(lane7与8)的溶液将根据超过滤要求进行净化(75毫升/分钟、13000 Da NMWL 截流的膜)。结论显示浓度为 0.1ng/mL 的 RNase 溶液经过超过滤处理后与阴性 DEPC 对照所获得的结果相似。在一个小时后,没有检测到RNA 出现降解,并且,基于凝胶电泳而观察到的条带情况也与 DEPC 处理水的条带情况类似。浓度为 1ng/mL 的溶液无法利用UF柱有效处理,某些 RNase 活性仍然保留,图示为凝胶电泳上RNA 降解情况。 材料与方法 根据如下说明中所述标准步骤来制备琼脂糖凝胶电泳:基于 TBE 缓冲液、浓度为1%并含有 0.5ug/mL 溴化乙锭的琼脂糖凝胶。从配备有 Pyrogard D 柱的 Milli-Q Gradient超纯水系统中获取水源。 图7琼脂电泳。1-2: RNase 溶液 1ng/ml;3-4: RNase溶液 0.1ng/L;5-61ng/ml 以 75ml/min 超滤的 RNase溶液; 7-8: 0.1ng/L 以 75ml/min 超滤的 RNase 溶液;9-10: DEPC处理样品 在用各种不同条件处理从而抑制 RNase 活性并防止 RNases 分解核糖核酸的水中检查了 rRNA 稳定性。本试验是通过将琼脂糖凝胶电泳置于生物分析仪中的方式来完成本试验的。在微通道中进行电泳分离的 rRNA样本(18S与28S条带)可通过荧光进行检 9)。在经过 DEPC 或 UF 处理过的水中所制备的样本在37℃培养1个小时、24小时, 图8:利用琼脂糖凝胶微电泳以及荧光检测方法(Agilent Bioanalyzer2100)来研究不同水质水样中 rRNA的稳定性:经过 DEPC 处理过的水、Ambion 的无 RNases 水以及经过 UF 纯化处理后的水(13000DaNMWL 截流的膜)。 并与用“无RNase 水”中所制备的样本比较(注释: Ambion“无 RNase水”是通过过超过滤方法获得)。通过过 RNA 转换为较小的片断以及 rRNA 峰值荧光信号的减弱,能够很容易地检测到 RNA 的分解情况。与经过 DEPC 处理过的水相比,利用超滤方法处理后水中的样本的稳定性大大提高。本文提出两种主要的假设情况来解释这些结论。第一个假设是基于水质差别而提出的。如表格1中所述,用来使 RNases 失活的 DEPC 处理方法将降低了水质,表现为有机物浓度与重碳酸盐浓度增加。大量碳酸盐和重碳酸盐离子的存在不仅仅使电阻系数大幅度下降,而且会影响到溶液的 pH 值,而溶液的 pH值的变化则对 RNA 稳定性带来不利影响。另一方面,超滤不会改变水质(表格1),而且, RNA 在这些条件下(图8)更加稳定。第二个假设是基于 RNases 将在经过 DEPC处理后恢复部分活性,缓慢消化水样中的RNA的可能性。由于 RNase 已经从溶液中测(图8),并转换为类似凝胶体的图像(图 被清除,因此,对UF柱而言,这种情况不会发生。 材料与方法 利用带有 RNA6000 纳米芯片的 Agilent2100生物分析仪进行试验。本试验所使用的RNA为老鼠胸腺的总RNA(Ambion)。无RNase 图9:从荧光检测结果转换而来的、类似凝胶的图像(Agilent 生物分析仪2100). 水与经过 DEPC 处理后的水均可从BIO-101购得。在红色通道上可以检测到激发值为 RNA的制备 利用经过 DEPC 处理过的16、高压灭菌溶液或者经过 UF 净化的水(5000Da NMWL截流)从不同的兔子的组织:大脑、心脏、肺部、肝脏以及膀胱,人体海绵体平滑肌细胞(HCCSMC)中分离总RNA。, 在琼脂糖凝胶上对样品进行电泳处理,并用溴化乙锭染色(图10)。试验过程中几乎观察不到可检测的 RNA 降解情况,同时,在利用经过DEPC 处理过的水以及 UF 处理后的水所制备的RNA 样本之间,不存在很大的差异。对于所有兔子组织以及人体海绵体平滑肌细胞(HCCSMC)而言, RNA 28S/18S 之间的比率约为 3:1,由于个别组织富含RNases, 因此非常明显。 图10:从RNA制备中所获取的EB 染色、1%甲醛的 RNA 凝胶。Lane1-6:利用 DEPC 处理过的溶液,从兔子大脑、心脏、肺部、肝脏、肾以及膀胱制备 RNA。 Lanes7-12:利用配有 UF 的Milli-Q所获取的水, 从兔子大脑、心脏、肺部、肝脏、肾和膀胱(5000Da NMWL 截流)来制备 RNA。Lanes13 与14则显示了使用 DEPC 处理过的水(lane13)和Milli UF 水 (lane 14)由人体海绵体平滑肌细胞 (HCCSMC)所制备的第二种凝胶样本。 材料与方法 人体海绵体平滑肌细胞(HCCSMC)将按照参考文献17与18中阐述的情况而生长。利用4M异硫氰酸胍和15mM巯基乙醇中的细 胞层溶解的方法来制备 RNA,随后,利用苯酚/氯仿萃取的方法以及异丙醇沉淀方法进行 RNA 的制备。给兔子进行放血可以从3到5公斤重的新西兰雄性兔子提取组织,并立即进行冷却。在干冰上,利用研钵来将各种组织研磨成末。在4M异硫氰酸胍和15mM巯基乙醇中将粉末处置均匀,随后,利用苯酚/氯仿萃取的方法以及异丙醇沉淀方法进行 RNA 的制备。RNA 再次溶解在将要测试的水中,并利用等体积的氯仿与接着等体积的苯酚进行 RNA 萃取。RNA 将再次溶解在将要测试的水中,在吸光值 260nm时检测 RNA 浓度。在使用之前, RNA将在乙醇悬浮存储。从人体海绵体平滑肌细胞(HCCSMC)提取的10微克总 RNA 以及从兔子组织所提取的15毫克总RNA将在1%甲醛——MOPS 溶液琼脂糖胶上进行电泳处理。 RNA 完整性测试 先前利用凝胶电泳进行提取与分离的 RNA样本的完整性需要通过 RNA 印迹分析进行检测。本技术能够确保 RNA 分子在萃取与分离过程中不受到损伤。图11给出了图解过程。老鼠纤维连接蛋白2型以及人体GADPH 基因特异性(图12)进行 Northernblots 杂交。纤维连接蛋白与 GADPH 基因特异性属于普遍存在的基因,由于在大多数的组织和细胞中均存在着相应的 mRNA,使得他们成为非常有用的工具。因此,他们的DNA 最有可能与其取自各类组织的样本中提供的未受损的 mRNA 进行杂交。当大脑、心脏或者肾中的纤维连接蛋白的含量很低时,在经过 DEPC 处理的水溶液中以及利用UF处理过的水之间,在肺部、肝脏和膀胱之间的对比并没有显示出可检测出的差异。 图11: RNA印迹杂交的示意过程 材料与方法 按照如上所阐述的琼脂糖凝胶电泳,总RNA转换至经过尼龙强化处理的硝化纤维上。18利用紫外线处理这些膜从而固定核酸。利用T7DNA聚合酶以及随机引物,适用于含有2型老鼠纤维连接蛋白(Psr270)与554-bpHindlll/Xbal GADPH 基因特异性的双链DNA探针带有【a-32P】dCTP 标签。特殊 活性范围从108至109cpm/mg。在温度为67 摄氏度情况下,两个小时内进行杂交。按照较低的要求【2XSSC0.1%SDS】以及较高的要求【0.2XSSC0.1%SDS】漂洗,过滤器在零下70摄氏度温度下曝露在XAR-5 膜下24-48小时。 图12:与图10相对应的RNA 印迹杂交 本文所阐述的试验需使用两种类型的超滤柱。内置Pyrogard5000 柱具有一个5000Da NMWL截留膜, 在Milli-QPF、Milli-Q Biocel以及Milli-Q Synthesis系统中均有该类纯化柱。第二个是Pyrogard D柱,属于取水点一次性超滤器:此13000Da NMWL截留UF柱能够连接到纯水系统出水口上,如Milli-Q Gradient、SynergyM以及Simplicity系统。这两种UF柱均能够生产无RNase的水。 这些试验表明,超滤处理可有效取代 DEPC 处理方法生产无 RNase 水。而 DEPC 处理方法仍属于为水添加杂质的繁冗步骤,并且无法与诸如 Tris 以及 HEPES缓冲液等氨基缓冲液结合使用。而且, DEPC 为可以致癌物质,因此需要小心处理。 超滤方法与 DEPC 处理方法相比,提供一种更简单、更快捷的替代方法,并能够直接与纯水系统整合使用。此外,在使用具有 UF 的超纯水系统制备的纯水,无论在总有机碳含量(小于20ppb) 方面还是在离子含量(电阻率为18.2兆欧·厘米)方面,所生成的水均显示出比其它方式更高的水质特点。 ( 参考文献 ) ( 1 . D’Alessio, G . ; R i ordan, J.F. "Ribonucleases: Structures and functions " . Academic Press, New-York,(1997). ) ( 2 S . orrentino, S.;Libonati,M. “ Structure-function relationships in h umanribonucleases: main distinctive features of the major RNases". F EB S Letters, 404,1-5,(1997). ) 4. Uchida, T.; Egami, F.6“6Microbial ribonucleases with special reference to RNasesT1, T2, N1, and U2”.The Enzymes, Boyer, E.D., Eds, 3rd ed, Vol 4, pp 205-250,Academic press,New-York, (1971). 5. Matoucek, J.“Ribonucleases and their antitumor activity”. Comp. Biochem.Physiol. Part C, 129,175-191, (2001). 6. Soucek, J.; Raines, R.T.; Haugg, M.; Raillard-Yoon, S.-A.; Benner, S.A.“Structural changes to ribonuclease A and their effects on biological activity". Comp.Biochem. Physiol. Part C, 123,103-111,(1999). 7. Blumberg, D.D. “Creating a ribonuclease-free environment.” Meth. Enzym.,152,20-24,(1987). 8. Wintzingerode, F.; Gobel, U.B.; Stackebrandt, E. “Determination of microbialdiversity in environmental samples: pitfalls of PCR-based rRNA analysis”. FEMSMicrobiology Reviews, 21,213-229, (1997). 9. Ambion website: www.ambion.com. 10. Terzyan, S.S.; Peracaula, R.; de Llorens, R.; Tsushima, Y.;Yamada, H.; Seno, M.;Gomis-Ruth, F.-X.; Coll,M.“The three-dimensional structure of human RNase 4.unliganted and complexed with d(Up), reveals the basis for its uridine selectivity”.J.Mol. Biol., 285,205-214,(1999). 11. Filippov, V.; Solovyev, V.; Filippova, M.; Gill, S.S..“A novel type of RNases IIIfamily proteins in eukaryotes”. Gene, 245, 213-221,(2000). 12. Loverix,S.; Winqvist, A.; Stromberg, R.; Steyaert, J. “Mechanism of RNase T1:concerted triester-like phosphoryl transfer via a catalytic three-centered hydrogenbond". Chem. Biology,7, 651-658,(2000). 13. Findlay, D.; Herries, D.G.; Mathias, A.P.; Rabin, B.R.; Ross, C.A.“The activesite and mechanism of action of bovine pancreatic ribonuclease A”. Nature, 190,781-784,(1961). 14.Raines,R. “Ribonuclease A”. Chem. Rev. 98,1045-1066,(1998). 15. Mabic, S.; Darbouret, D.; Kano, I.“Qualification study of a point-of-useultrafiltration device for the production of pyrogen-free ultrapure water".T.. The R&DNotebook, Millipore RD006 (2001). 16. Ehrenberg, L.; Fedorak, I.; Solymosy, F.“Diethylpyrocarbonate in nucleic acidresearch”.Prog. Nucleic Acid Res.Mol. Biol., 16, 189-262,(1976). 17.Moreland, R.B.; Traish, A.M.; McMillin, M.A.; Smith, B.; Goldstein, I.; Saenz deTejada, I.“PGE1 suppresses the induction of collagen synthesis by transforminggrowth factor-b1 in human corpus cavernosum smooth muscle”. J. Urol., 153,826-834,(1995). 18. Huang, Y.-H.; Leblanc, P.; Apostolou, V.A. ; Stewart, B. ; Moreland, R.B.Comparison of Milli-Q PF Plus water to DEPC-treated water in the preparation andanalysis ofRNA”.BioTechniques, 19, 656-661,(1995). 密理博中国有限公司翻译 Lit.号: RD008EN00.2001年在法国印制版权◎2001, Millipore 有限公司,Bedford,MA, U.S.A.Millipore, Milli-Q and Elix 是 Millipore 有限公司的注册商标。 Milli-Q 和 Progard 是 Millipore 有限公司的商标.Dionex 是 Dionex 有限公司的注册商标。版权所有,违者必究. RD 通过超滤方法制备超纯水针对核糖核酸酶(RNase)敏感的应用
确定







还剩7页未读,是否继续阅读?
默克化工技术(上海)有限公司为您提供《超纯水中超滤法制备工艺检测方案(纯水器)》,该方案主要用于其他中超滤法制备工艺检测,参考标准--,《超纯水中超滤法制备工艺检测方案(纯水器)》用到的仪器有AFS 全自动纯水供应系统、默克Milli-Q Super-Q™ Plus试剂级超纯水系统
相关方案
更多











