方案详情
文
本应用介绍了一种快速同时测定配方食品和保健食品中脂溶性维生素 A、D2、D3 和α、β、γ、δ-维生素 E 含量的方法。该方法采用在线固相萃取结合中心切割二维液相色谱(online SPE-2DLC) 技术。样品经皂化后直接进样,自动完成目标分析物的富集、净化和分离等过程。本文对影响含量测定的关键色谱条件(如 online SPE 的上样和冲洗溶剂、洗脱溶剂和洗脱时间、在线稀释以及一维色谱分离条件)进行了系统优化,并对该方法的线性、精密度、重现性和加标回收率等性能指标进行了评估。测定婴幼儿配方质控样品及其它基质样品,并与标示值进行对比,证实该方法准确可靠。结果表明该方法满足测定要求及现行标准方法要求,并且具有简便、快速、环境友好的优点,尤其适用于样品检测需求较大的实验室。
方案详情

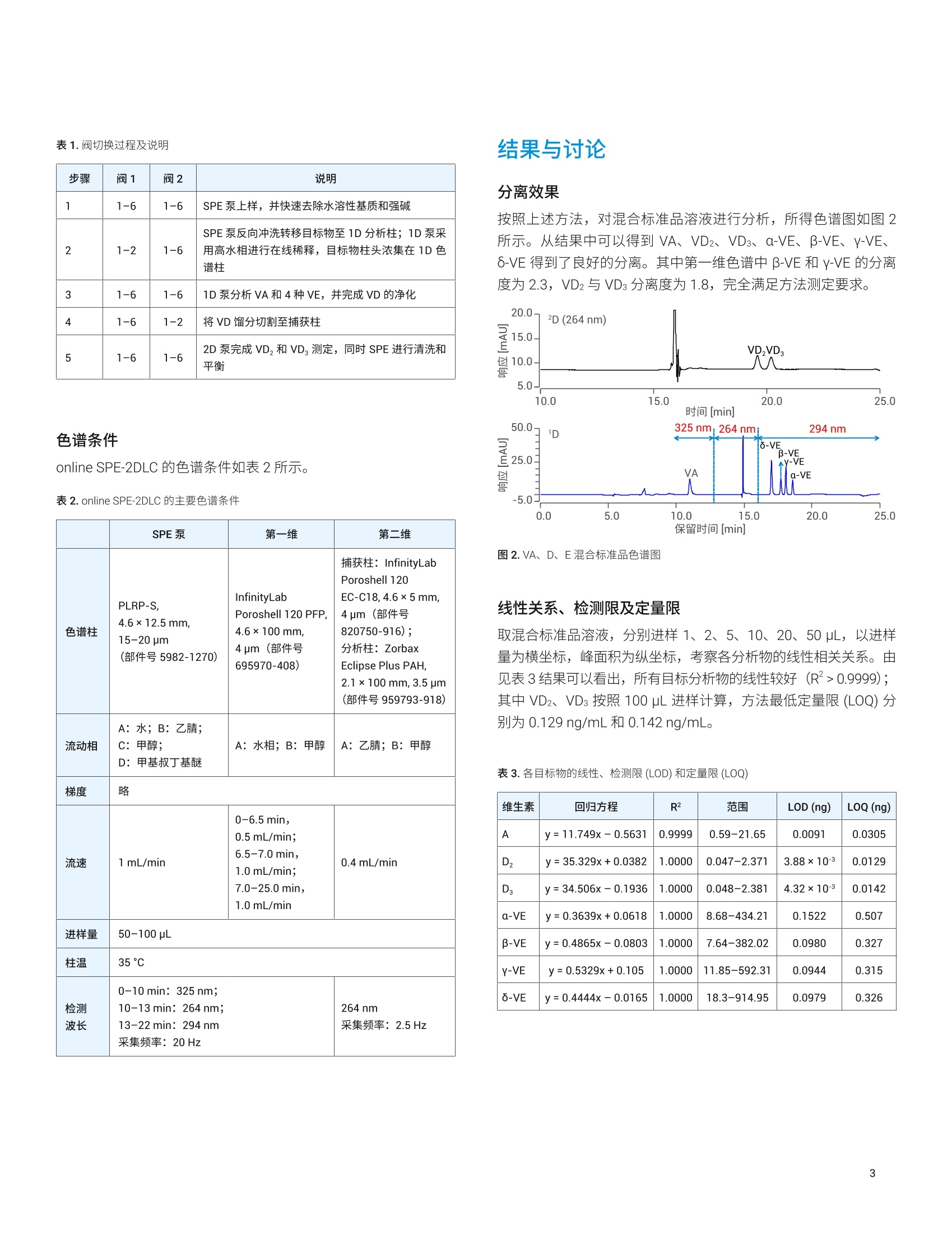
采用在线固相萃取-中心切割二维液相色谱法同时测定配方食品和保健食品中维生素A、D、E的含量 张艳海,杨新磊,陈刚,李浪,鲁锐 本应用简报介绍了一种快速同时测定配方食品和保健食品中脂溶性维生素 A、D2、D3和a、β、y、6-维生素E含量的方法。该方法采用在线固相萃取结合中心切割二维液相色谱(online SPE-2DLC) 技术。样品经皂化后直接进样,自动完成目标分析物的富集、净化和分离等过程。本文对影响含量测定的关键色谱条件(如 online SPE 的上样和冲洗溶剂、洗脱溶剂和洗脱时间、在线稀释以及一维色谱分离条件)进行了系统优化,并对该方法的线性、精密度、重现性和加标回收率等性能指标进行了评估。测定婴幼儿配方质控样品及其他基质样品,并与标示值进行对比,证实该方法准确可靠。结果表明该方法满足测定要求及现行标准方法要求,并且具有简便、快速、环境友好的优点,尤其适用于样品检测需求较大的实验室。 脂溶性维生素A、D、E(VA、VD、VE)是人体维持正常代谢和机能所必需的营养素。强化食品和特殊医疗配方食品是补充维生素的重要途经。准确测定其中的维生素含量对于科学膳食,并保证食品安全具有重要意义。 GB5009.82-2016 是关于食品中 VA、VD、VE测定的现行标准方法,其适用范围涵盖婴幼儿食品、乳品、肉与肉制品、食用植物油、坚果、豆类和辣椒粉等多种食品或食物基质。 目前有关配方食品中VA、VD 和 VE 测定方法的报道较多,其中样品前处理过程通常包括皂化和有机溶剂液液萃取,并且在VD的分析过程中还需要采用固相萃取或正相色谱的净化过程等12-3。其中皂化过程可将目标物从其蛋白包裹的脂肪胶束中游离出来,一一般是必不可少的前处理过程。但液液萃取及其后续的净化制备步骤繁琐、耗时,是制约整个方法分析效率的主要瓶颈,也是测定结果误差的重要来源。 在先前的研究中,已建立一种在线固相萃取-二维液相色谱同时测定食品中的 VA、VD、a-VE、(B+V)-VE 和 6-VE 的方法“,该方法可大大改善样品分析效率,并有效降低分析成本,从而满足样品量较大的实验室的检测需求。但是该方法无法实现 B-VE 与 Y-VE的分离和测定。为完善整体方案并满足 GB5009.82-2016的分析要求,本研究对一维色谱分离进行优化,向 online SPE-2DLC 系统中引入在线稀释过程,同时对影响测定结果的其它关键色谱条件进行优化,实现了对多种配方食品中脂溶性 VA、VD 和 a、β、y和6-VE的快速检测分析。 试剂和样品 抗坏血酸 (C6H606, ACS, ≥99.0%)、甲酸(CH202,色谱级)、氢氧化钾(KOH,分析纯)、2,6-二叔丁基-4-甲基苯酚 (BHT,≥99%)、乙醇(HPLC级),购自上海安谱实验室技术公司;磷酸(HPLC 级,浓度 85%-90%),购自北京迪科马科技有限公司;甲醇及乙腈((HPLC级)购自默克公司;甲基叔丁基醚 (MTBE,HPLC级)购自美国天地有限公司。 维生素(±)a-、β-、(+)Y-和(+)6-生育酚(分析标准品)购自Sigma-Aldrich;维生素A((视黄醇,纯度99.88%)购自TM-standard;维生素D2 和D:(纯度99.9%)购自中国食品药品检定研究院;婴幼儿配方奶粉质控样品购自中国检验检疫研究院;米粉、饼干和面条由某公司提供;其他样品均购自超市。 仪器和设备 安捷伦中心切割二维液相色谱系统,包括: Agilent 1260 InfinityⅡ四元泵(部件号 G711B×2); Agilent 1260 Infinity Ⅱl二元泵(部件号 G7112B); Agilent 1260 Infinity ll自动进样器(部件号G7129A), Agilent 1260 Infinity ⅡI柱温箱(部件号 G7116A, 内置2位6通阀); Agilent 1260 Infinity II VWD (部件号 G7114B),Agilent 1260 Infinity II DAD (部件号7117C, 配备60 mm 超高灵敏度流通池); Agilent 1290 Infinity 阀驱动(独立的阀驱动装置,部件号G1170A,配1个2位6通阀头)。 软件采用 Agilent OpenLab CDS 2.4。 标准品储备溶液制备 准确称取 25.0 mg VA标准品,用无水乙醇溶解后,转移至50mL容量瓶中并用无水乙醇定容,得到浓度为0.5 mg/mL 的 VA标准储备液。 分别准确称取 50.0 mg a-VE、β-VE、Y-VE、6-VE隹准品,用无水乙醇溶解后,转移至50 mL 容量瓶中并用无水乙醇定容,得到浓度为 1.0 mg/mL 的 VE 混合标准储备液。 准确称取 10.0 mg VD2标准品,用无水乙醇溶解后,转移至100 mL 容量瓶中并用无水乙醇定容,得到浓度为 0.1 mg/mL 的VD2标准储备液。准确称取 10.0 mgVD3标准品,用无水乙醇溶解后,转移至100 mL 容量瓶中并用无水乙醇定容,得到浓度为0.1 mg/mL的VD3标准储备液。 各种标准储备液避光保存于-20℃下,有效期为1个月。临用前将溶液回温至20℃,并按照 GB5009.86-2016附录2方法进行浓度校正。 混合标准品溶液制备 分别移取 VA储备液2mL, 四种 VE 混合标准储备液各10 mL,VD2、VDs储备液各 0.5 mL 于100 mL 容量瓶中,用甲醇定容,得到VADE混合标准储备液 (VA: 10 pg/mL;四种 VE: 100 pg/mL,VD2、VDs: 0.5 pg/mL)。再准确移取 VADE 混合标准储备液 1mL于10mL容量瓶中用甲醇定容,得到 VADE 混合标准品溶液 (VA:1 ug/mL;四种VE: 10 ug/mL, VD2、VD3: 0.05ug/mL)。 样品前处理 样品溶液制备参照 GB 5009.82-2016标准第一法样品前处理中的皂化方法。称取3-5g奶粉样品置于圆底烧瓶中(含淀粉较多的米粉等样品需要首先经过a-淀粉酶解),加入20 mL 水将其溶解,混匀;再加入1.0g 抗坏血酸和 0.1 g BHT, 混匀;然后加入30 mL乙醇和 10-20 mL氢氧化钾溶液(50 g KOH/50g 水),混匀后于80℃的恒温水浴中皂化30 min;皂化后冷却至室温,转移至100 mL 容量瓶中并用乙醇定容,摇匀;然后取适量皂化液,高速离心5 min (10000 rpm), 再用安捷伦 0.22 pm 针头滤器过滤(尼龙滤膜,部件号5190-5271)至进样瓶中,待测。 系统构建及阀切换过程 在线固相萃取结合中心切割二维液相色谱 (online SPE-2DLC)的连接见图1。其中阀1用于online SPE 过程;阀2用于2D 接口。阀切换过程及说明见表1。 图1. online SPE-2DLC分析 VA、VD 与四种 VE 的系统示意图 表1.阀切换过程及说明 步骤 阀1 阀2 说明 1 1-6 1-6 SPE 泵上样,并快速去除水溶性基质和强碱 2 1-2 1-6 SPE 泵反向冲洗转移目标物至1D分析柱;1D泵采 用高水相进行在线稀释,目标物柱头浓集在1D色 谱柱 3 1-6 1-6 1D 泵分析VA和4种VE, 并完成 VD 的净化 4 1-6 1-2 将 VD 馏分切割至捕获柱 5 1-6 1-6 2D 泵完成VD, 和 VD,测定, 同时 SPE 进行清洗和 平衡 色谱条件 online SPE-2DLC 的色谱条件如表2所示。 表2. online SPE-2DLC 的主要色谱条件 SPE泵 第一维 第二维 色谱柱 PLRP-S. 4.6×12.5mm, 15-20 pm(部件号5982-1270) InfinityLabPoroshell 120 PFP.4.6×100 mm,4pm (部件号 695970-408) 捕获柱: InfinityLabPoroshell 120 EC-C18,4.6×5mm, 4pm (部件号 820750-916); 分析柱: Zorbax Eclipse Plus PAH,2.1×100 mm, 3.5pm (部件号959793-918) 流动相 A:水; B: 乙;C: 甲醇; D: 甲基叔丁基醚 A:水相;B:甲醇 A:乙腈;B:甲醇 梯度 略 流速 1 mL/min 0-6.5 min,0.5mL/min;6.5-7.0 min,1.0 mL/min;7.0-25.0 min,1.0 mL/min 0.4 mL/min 进样量 50-100pL 柱温 35°C 检测波长 0-10min:325nm; 10-13 min: 264 nm;13-22 min: 294nm 采集频率:20Hz 264nm 采集频率:2.5Hz 结果与讨论 分离效果 按照上述方法,对混合标准品溶液进行分析,所得色谱图如图2所示。从结果中可以得到 VA、VD2、VD3、a-VE、B-VE、V-VE、5-VE 得到了良好的分离。其中第一维色谱中 B-VE 和 y-VE的分离度为 2.3, VD2 与VD3分离度为1.8,完全满足方法测定要求。 图2.VA、D、E混合标准品色谱图 线性关系、检测限及定量限 取混合标准品溶液,分别进样1、2、5、10、20、50uL,以进样量为横坐标,峰面积为纵坐标,考察各分析物的线性相关关系。由见表3结果可以看出,所有目标分析物的线性物好 (R">0.9999);其中VD2、VD3 按照 100 pL进样计算,方法最低定量限(LOQ)分别为 0.129 ng/mL 和0.142 ng/mL。 表3.各目标物的线性、检测限 (LOD) 和定量限(LOQ) 维生素 回归方程 R2 范围 LOD (ng) LOQ (ng) A v=11.749x-0.5631 0.9999 0.59-21.65 0.0091 0.0305 D2 v=35.329x+0.0382 1.0000 0.047-2.371 3.88×103 0.0129 D y=34.506x-0.1936 1.0000 0.048-2.381 4.32×10-3 0.0142 a-VE y=0.3639x+0.0618 1.0000 8.68-434.21 0.1522 0.507 B-VE y=0.4865x-0.0803 1.0000 7.64-382.02 0.0980 0.327 V-VE y=0.5329x+0.105 1.0000 11.85-592.31 0.0944 0.315 0-VE y=0.4444x-0.0165 1.0000 18.3-914.95 0.0979 0.326 精密度及重现性 取混合标准品溶液,连续进样5次,每次进样10uL,计算峰面积和保留时间的 RSD。结果显示,所有目标分析物分留时间的 RSD 均小于0.5%,峰面积的 RSD 小于2%。另取奶粉质控样品5份,分别按照样品溶液制备方法制备待测溶液。结果显示,目标分析物的含量RSD 均小于2%。以上结果表明本方法重现性良好,显著优于 GB 5009.82-2016 的要求(15%)。 表4.方法重现性考察结果 VA 6-VE B-VE y-VE a-VE VD, NO R.Tmin] 含量(pg/100 g) R.T[min] 含量 (mg/100 g) R.Tminl 含量 (pg/100 g) R.TImin 含量 (mg/100 g) R.Tmin 含量 (ug/100 g) R.T [min] 含量 (mg/100 g) 1 11.64 507.43 17.329 4.78 18.028 0.58 18.315 11.93 18.851 10.85 20.809 7.31 2 11.637 508.38 17.326 4.81 18.022 0.57 18.309 12.01 18.844 10.90 20.801 7.57 3 11.644 506.73 17.324 4.78 18.023 0.57 18.311 11.97 18.846 10.90 20.814 7.37 4 11.639 510.19 17.327 4.76 18.025 0.57 18.312 11.97 18.846 10.90 20.79 7.41 5 11.627 499.99 17.312 4.77 18.01 0.56 18.297 11.77 18.833 10.75 20.756 7.46 平均值 11.637 506.55 17.324 4.78 18.0216 0.57 18.3088 11.93 18.844 10.86 20.794 7.42 Stdev 0.0063 3.8868 0.0067 0.0173 0.0069 0.0056 0.0069 0.0923 0.0067 0.0657 0.0231 0.0964 RSD% 0.055 0.767 0.039 0.362 0.038 0.974 0.038 0.773 0.035 0.605 0.111 1.299 方法准确性 取空白奶粉基质样品,分别按照高、中、低三个水平加入目标分析物标准品,按照样品前处理方法制备待测溶液,测定加标后的总量,按照下面公示计算回收率: 结果见表 5。 VA 和 VE 的加标回收率为100.86%-101.63%, RSD 为 0.59%-1.93%; VDs 的回收率在92.01%-95%之间, RSD 为 1.18%。表明采用本方法完全满足样品测定要求,且所有目标分析物在样品分析过程中损失较少,测定结果准确。 表5.样品皂化液加标实验结果(n=2) 分析物 回收率(%) 平均值(%) RSD(%) High-1 High-2 Medium-1 Medium-2 Low-1 Low-2 VA 100.48 100.62 101.70 100.39 102.93 103.66 101.63 1.37 O-VE 99.97 100.87 101.94 101.25 99.72 105.10 101.47 1.93 B-VE 100.10 101.18 101.26 100.88 99.79 101.96 100.86 0.80 Y-VE 100.24 101.10 101.32 100.87 100.78 103.51 101.30 1.13 a-VE 101.28 102.14 101.44 100.88 100.83 102.20 101.46 0.59 VD, 93.86 95.00 93.48 93.19 92.22 92.01 93.29 1.18 注: High、Medium 和 Low分别表示向空白奶粉基品样品中加入VADE 混合标准品储备溶液10、5和1mL等高、中、低三个加标水平。 另取婴幼儿配方奶粉质控样品,按照本方法测定目标分析物含量,并与质控范围进行比较。结果表明, VA 的含量测定结果为576.86±2.57 pg/100 g(特性值564.8pg/100 g, 范围495.9-633.7 pg/100 g); a-VE 的含量测定结果为13.23±0.05 mg/100 g(特性值14.73mg/100g, 范围10.88-18.58 mg/100 g); VD3的含量测定结果为9.05±0.22 pg/100g (特性值9.949 pg/100 g,范围8.51-11.38 pg/100 g)。所有目标分析物均在含量区间范围内,证明了本方法测定结果准确、可靠。 实际样品测定 为进一步验证本方法对多种食品基质中目标物测定的适用性,选择营养米粉、饼干、面条及保健品多维维生素片等样品,测定其中VA、D、E的含量。分析得到的各种样品的谱图如图3所示,从中可以看出,目标分析物分离度良好,测定结果列于表6中。所有目标物的测定结果均符合或在标示量范围内或接近标示量。 图3.典型样品的第一维(A)和第二维(B)分离谱图(a.配方奶粉, b.多维维生素片;c.营养面条;d.营养饼干;e.原味米粉; f.核桃味米粉 表6.样品中维生素A、D、E含量测定结果 样品 VA(pg/100 g) VD3(pg/100 g) a-VE(mg/100 g) 含量 标示量/范围 含量 标示量/范围 含量 标示量/范围 xxx品牌婴配粉 358.90±2.43 395 8.14±0.06 8.88 13.46±0.22 12 原味米粉 291.08±2.09 274 7.79±0.26 5.0 10.99±0.27 <12 核桃味米粉 579.34±8.46 符合 9.46±0.04 符合 10.41±0.07 <12 营养饼干 461.95±1.38 符合 12.24±0.17 符合 5.31±0.098 5-7 营养面条 342.98±0.42 300 6.01±0.82 5-7 n/a n/a 多维维生素片 309.55±1.81 300 7.03±0.1 6 8.88±0.095 g 与 AOAC 及 GB5009.82-2016方法分析流程对比 本方法与 AOACI5-6及 GB5009.82-2016分析流程对比见图4所示。其中热皂化可将目标分析物从脂蛋白包裹状态中释放出来,无论AOAC 还是 GB 方法,液液萃取步骤都使样品制备流程耗时费力,成为制约整个方法效率的主要瓶颈。而本方法采用 onlineSPE 替代此步操作,使整个分析流程变得简便快速。由于样品分析流程简化,也显著改善了样品测定结果的重复性,同时减少了有机溶剂消耗,因此本方法更加环保。另外 AOAC 和 GB 方法需要将含量差异较大的 VA、VE 与 VD 分开测定。本方法采用2DLC结合常规紫外检测器和高灵敏度的 DAD 检测器,可实现常量 VAE与微量VD 的同时定量分析,分析时间只需约25 min, 整体分析效率提升近4倍,分析成本下降约60%,对于有高通量分析需求的实验室具有重要意义。 AOAC 本方法 称样(5 min) 加入内标或外标法(5min) 淀粉含量较高的食品需要淀粉酶解(30 min) 热皂化 (30 min) 冷却到室温(5 min) 7 乙醇定容到100 mL (2 min) 离心(3 min) 维生素A、D和四种E同时定量 (online SPE-2DLC) 结论 本应用在先前研究的基础上,对关键色谱条件进行了优化,开发出用于同时测定配方食品中脂溶性VA、D2、Ds 和a、β、y和6-VE 的 online SPE-2DLC 方法。对加标回收率及质控样品的测定结果证明,本方法准确可靠。与标准方法的分析流程相比,本方法在分析效率、分析成本、环境友好性、结果重现性等方面都具有明显优势,尤其适用于样品检测需求量较大的实验室。 ( 1.( GB 5009.82-2016.食品安全国家标准食品中维生素A、D、E 的测定 ) ( 2.BS EN 12821:2009.Foodstuffs-Determination of vitamin D by high performance liquid chromatography-Measurement ofcholecalciferol ( D s) or ergocalciferol (D2) ) 查找当地的安捷伦客户中心: www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278,400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: www.agilent.com/chem/erfq-cn www.agilent.com 安捷伦对本资料可能存在的错误或由于提供、展示或使用本资料所造成的间接损失不承担任何责任。 ( 本文中的信息、说明和技术指标如有变更,恕不另行通知。 ) ( ◎安捷伦科技(中国)有限公司,2021 ) 本应用介绍了一种快速同时测定配方食品和保健食品中脂溶性维生素 A、D2、D3 和α、β、γ、δ-维生素 E 含量的方法。该方法采用在线固相萃取结合中心切割二维液相色谱(online SPE-2DLC) 技术。样品经皂化后直接进样,自动完成目标分析物的富集、净化和分离等过程。本文对影响含量测定的关键色谱条件(如 online SPE 的上样和冲洗溶剂、洗脱溶剂和洗脱时间、在线稀释以及一维色谱分离条件)进行了系统优化,并对该方法的线性、精密度、重现性和加标回收率等性能指标进行了评估。测定婴幼儿配方质控样品及其它基质样品,并与标示值进行对比,证实该方法准确可靠。结果表明该方法满足测定要求及现行标准方法要求,并且具有简便、快速、环境友好的优点,尤其适用于样品检测需求较大的实验室。
确定





还剩5页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《配方食品和保健食品中维生素 A检测方案(液相色谱仪)》,该方案主要用于其他特殊膳食产品中营养成分检测,参考标准--,《配方食品和保健食品中维生素 A检测方案(液相色谱仪)》用到的仪器有安捷伦1260 Infinity II 二元液相色谱系统、OpenLAB 软件
相关方案
更多
该厂商其他方案
更多











