推荐厂家
暂无
暂无



 400-612-9980
400-612-9980
 留言咨询
留言咨询

 400-860-5168转2141
400-860-5168转2141
 留言咨询
留言咨询

 留言咨询
留言咨询



一、食品中的香味物 食品工艺学的研究必然地要将重点放在工厂和加工工艺上,放在用来制备各种食品的基础材料上。人们接触任何食品或饮料的最初印象是它们的外观,当然也包括它们的颜色。外观对人们选择食品有最大的影响,因为直观的吸引力会将营养价值相同的两种食品中的一种变得突出,不管这些食品是在包装中、或已准备好就可以吃或喝的。它们的外观直到食品摄取前都是一个有价值的特征(Hicks,1979)。在吃喝过程中,挥发性组分首先通过鼻子吸入,激发了嗅觉感受器,这一作用靠食物在嘴中咀嚼和吞咽时释放的挥发物又得以加强。同时,基本的味觉因素(即咸、甜、酸或苦)经过舌头上的味蕾得以感知,而口腔深部和咽喉对触觉、温度和/或化学刺激(即组织感、刺激性、涩味等)有感受。只有在这时候才认识了完整的香味。就在这一阶段,对食品由其外部到内部的性质作出了评价,从而对气息、味道、滋味和其他的整体感觉的享受才成为重要。人们早已认识到,香味具有这样一种特性,即它对于饮食说来,没有化学或生理学基础,但没有它,人们可能会挨饿,因为身体不能长期地接受一种无味的饮食。 不管普遍的错误概念如何,香味是由挥发的和非挥发的化合物(不管这些化合物是天然的还是合成的)引起的一种感觉,这些化合物存在于我们的饮食中,并在摄入时处于均衡状态。 香味的来源有:预先存在于如肉、鱼、水果、蔬菜等原料中,这些原料构成了我们饮食的主体,营养上也是必要的;由基础食品组分中存在的前驱体经烹调过程中的热作用引起的化学变化所产生;以浓缩的天然或合成的食品香精或调味品的形式有意加入的(Heath 1980)。 食品中的香味不是静态的,而是处于动力平衡状态,能受下列因素影响并发生变化:原材料、加工条件、包装材料、从开始直至食品的最后制造过程中的处理和贮藏条件。工艺学家在食品配方和生产中最关心的问题之一是对这些变化的认识,以便利用这些变化来尽可能改进产品的可接受性,或者来消除、限制那些会毁损最后产品质量的变化。所有食品原料都有其基本的香味轮廓,这一香味轮廓主要来自具有低香味强度的原料(这些原料因其营养价值和组织感作用而被使用)。许多这样的食品原料含有前驱体和酶体系,这些酶体系在制备和食品加工过程中会活化起来。所有的食品原料并不都会产生人们所喜爱的香味性质,要去除讨厌的气味必须有特殊的加工技术。也可以加入其他组分,以增强喜爱的香味特征、掩盖讨厌的气味特性或赋予完全新型的香味轮廓。
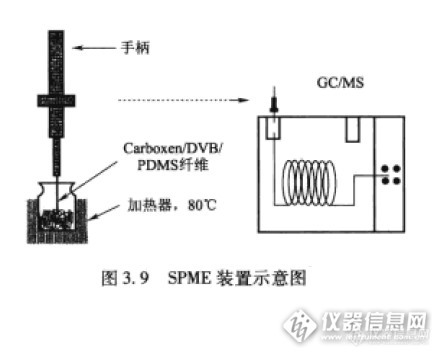
看见一本书:香味化学与工艺学,作者为美国的加里·赖内修斯。里面有讲到香味的分离方法,虽是总结前人的经验,但是有很多详实的数据,原理也讲得很透彻。现在把这一段分享给大家。香味分离法(有删节) 想要分析目标物(食品等)的香气成分,需要整体香气的轮廓,很可能就要将好几种香味分离法向结合。每一种分离法都只能提供一部分的整体轮廓。虽然这样说,但还是简单介绍下常用的一些香气分离法和它们的主要优缺点。 先来看下面一张图,采用不同香气分离法的回收率。这个图很直观的表面了各种香气分离法的“侧重点”。http://ng1.17img.cn/bbsfiles/images/2014/08/201408121509_509987_1060664_3.png1. 静态顶空 香气研究用的一种立项方法是直接分析食品上方的平衡顶空,该方法不仅简单、方便,而且容易自动化。该方法最大的缺点是灵敏度不高(图3.2)。由于直接注入气象色谱的顶空量常限制为10mL或更少,由表3.2可看出,只有顶空浓度超过10-7g/L的挥发物才能被气相色谱检测到,只有浓度超过10-5g/L的挥发物才能用质谱分析。由于食品上方的挥发物浓度范围通常为10-4~10-10g/L,因此只有含量最丰富的挥发物才可以通过直接顶空取样检测到。http://ng1.17img.cn/bbsfiles/images/2014/08/201408121509_509988_1060664_3.png 静态顶空的第二个不足是它们很难用于定量研究,得到的分析数据只反映顶空中香气组分的含量。2. 顶空浓缩法(动态顶空) 利用某种气提和浓缩的顶空浓缩法常被称为动态顶空。在该方法中,样品用惰性气体例如氮气或者氦气吹扫,使香气组分从样品中分离,然后再由气流捕集吹扫气中的挥发物(设法移走)捕集香气组分可以用低温、Tenax(或其他吸附聚合物)、活性炭或其他合适的体系。 低温冷阱的选择性最差。如果设计和操作得当,低温冷阱能捕集几乎所有的香气组分。它最大的问题是也鞥捕集到水——几乎所有食品中含量最丰富的挥发物。因此,最终得到的是含水的食品馏分,因而必须设法将水除去(香气轮廓再次出现较大的改变)。 人们常用Tenax阱(苯乙烯聚合物)捕集香气。但表面积小,吸附量也小。此外,Tenax对极性化合物吸附弱(因此不会吸附大量水),对非极性化合物吸附较强。 虽然常见的捕集材料是Tenax,但由于活性炭阱对大多数香气组分不仅吸附能力强而且容量大,因而也用作捕集材料。1~10mg的活性炭就能捕集10-100L吹扫器中夹带的挥发物。活性炭阱最大的问题是在洗脱香气成分是,难以消除杂质的引入。3. 蒸馏法 蒸馏的定义非常广,包括高真空分子蒸馏(图3.4)、水蒸气蒸馏(图3.5)和简单加热食品后将蒸出的香气组分谁扫入气相色谱(图3.6,热脱附)。http://ng1.17img.cn/bbsfiles/images/2014/08/201408121510_509989_1060664_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/08/201408121510_509990_1060664_3.png 高真空蒸馏用于纯脂肪或油、含脂肪食品的溶剂萃取物(例如干酪)和水质食品(例如水果)。 水蒸气蒸馏可以通过多种方法来实现。例如,可以讲食品简单放入旋转蒸发仪(假如为液体,固体需要先在水中制浆)并收集馏分,然后将所得馏分用溶剂萃取,得到供气相色谱分析用的香气分离物。最常见的水蒸气蒸馏是同时蒸馏萃取(SDE,也称为Likens-Nickerson法)。图3.5给出了常压下同时蒸馏萃取的装置图。4. 溶剂萃取 直接溶剂萃取是一种最简单、最有效的香气分离方法,该方法最大的局限性是它不适合含油脂的食品。溶剂萃取的第二个限制因素是溶剂的纯度。溶剂纯度必须很高,因而使用前通常需要在公司内重新蒸馏。 即使简单的溶剂萃取,也会给香气轮廓带来很大的改变。5. 吸附萃取 相比较而言,吸附萃取(SPME和搅拌棒萃取)是分离食品香气的新技术。固相微萃取技术,首先用于环境分析,后来开始成为分析食品挥发物常用的技术。 图3.9给出了SPME装置的示意图。涂油吸附剂的纤维是一个改装的注射器,针头可以在外鞘中自由伸缩(保护纤维不受物理损伤和污染)。纤维头放入样品顶空吸附挥发物,然后将吸附了挥发物的纤维头放在气相色谱载气流中热
[align=center][font=DengXian]香气香味物质分析样品处理概要[/font][/align][font=DengXian]样品制备是香气香味物质分析中的重要环节,它一般包括从样品中提取香气香味化合物[/font]([font=DengXian]包括去除样品中的干扰性杂质的分离净化[/font])[font=DengXian]、浓缩提取液等步骤,是将待测样品处理成适合[/font]GC/MS[font=DengXian]的检测溶液的过程。[/font][font=DengXian]有各种各类样品,其基质和香气香味物质化学组成极为复杂,要能适合[/font]GC/MS[font=DengXian]分析,必须对样品进行细致的提取、浓缩和净化处理。样品制备在香气香味物质分析中是耗时、费力的过程。其效果好坏直接影响到分析结果的准确性,而且还影响[/font]GC/MS[font=DengXian]仪器的工作寿命。在提取过程中要求尽量完全地将香气香味组分从样品中提取出来,同时又尽量除出基质和干扰性杂质。当样品中香气香味含量很低时,常常通过增大样品量和浓缩提取液来达到仪器检测限的要求。[/font][font=DengXian]用[/font]GC/MS [font=DengXian]分析时,样品组分必须为挥发性,无纤维,无油脂,无碳水化合物(糖)类,无蛋白质,有足够量,不含水,基质的峰不干扰香气香味成分。一般能满足直接进样的样品不多,通常样品净化非常需要,也很重要。如果没有良好的样品提取方法,就无法获得足够的,准确的待分析的香气香味成分进行[/font]GC/MS[font=DengXian]分析。[/font] [font=DengXian]样品提取原理[/font][font=DengXian]如何从基质中分离待测香气香味成分?一般从下面三个方面考虑:[/font][font=DengXian]从挥发性[/font]([font=DengXian]沸点[/font])[font=DengXian]考虑,采取蒸馏的方法。[/font][font=DengXian]从极性[/font]([font=DengXian]溶解度[/font])[font=DengXian]考虑,依据“相似相溶”原理,采取溶剂萃取的方法。[/font][font=DengXian]从功能团的相互作用考虑,采取吸附的方法。[/font]


