对于常见的固相反应来说,其反应方程可以表示为
![]() (1)
(1)
其反应速度可以用两种不同形式的方程表示:
微分形式
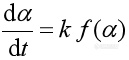 (2)
(2) 和
积分形式
式中:
α——t时物质A已反应的分数;
t——时间;
k——反应速率常数;
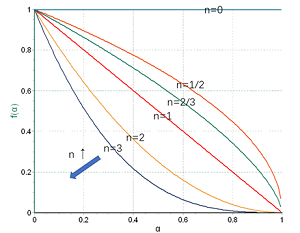
f(α)——反应机理函数的微分形式;
G(α)——反应机理函数的积分形式。
由于f(α)和G(α)分别为机理函数的微分形式和积分形式,它们之间的关系为:
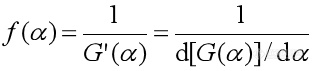 (4)
(4) k与反应温度T(绝对温度)之间的关系可用著名的Arrhenius方程表示:
![]() (5)
(5)
式中:
A——表观指前因子;
E——表观活化能;
R——通用气体常数。
方程(2)~(5)是在等温条件下出来的,将这些方程应用于非等温条件时,有如下关系式:
即:
式中:
T0——DSC曲线偏离基线的始点温度(K);
β——加热速率(K·min-1)。
于是可以分别得到:
非均相体系在等温与非等温条件下的两个常用动力学方程式:
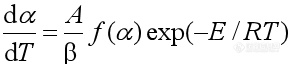 (非等温) (8)
(非等温) (8) 动力学研究的目的就在于求解出能描述某反应的上述方程中的“动力学三因子” E、A 和f(α)
[原帖链接]
内容
 JOE HUI
2019-07-31
JOE HUI
2019-07-31
了解行业最新动态
 huacai
2019-07-29
huacai
2019-07-29
非常好的事
 慢慢来比较快
2019-07-27
慢慢来比较快
2019-07-27
怎样选择应该用哪个方程?激活能具体的计算过程详解
 KK-yiqi
2019-07-14
KK-yiqi
2019-07-14
结晶动力学
 赛孚瑞化学试剂
2019-07-01
赛孚瑞化学试剂
2019-07-01
好