







自律,自由。


3月18日,深圳华大基因股份有限公司(以下简称“华大基因”)发布公告,称其新型冠状病毒核酸检测试剂盒产品已启动美国食品药品监督管理局(FDA)的EUA申报,目前Pre-EUA已被正式受理。根据美国近期发布的新型冠状病毒肺炎相关检测政策指南,公司将正式启动该产品在美国临床市场的商业销售。

产品信息
Real-Time Fluorescent RT-PCR Kit for Detecting SARS-nCoV-2(中文名称:新型冠状病毒SARS-nCoV-2核酸检测试剂盒(荧光PCR法))
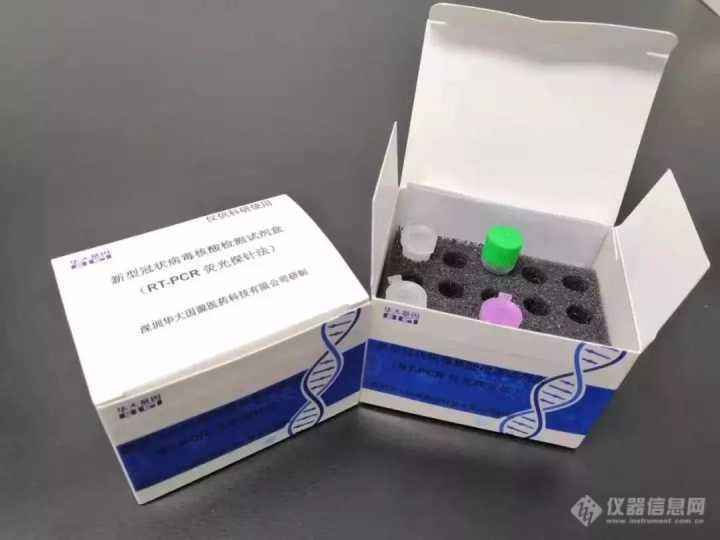
该试剂盒适用于新型冠状病毒感染的肺炎疑似患者或其他需要预期用途进行新型冠状病毒感染诊断或鉴别诊断者,通过检测从受检者采集的咽拭子或肺泡灌洗液样本中提取的核酸以确定受检者是否有新型冠状病毒感染。
使用条件 :For Emergency Use Only(紧急情况下使用)
仪器信息网了解到该试剂盒日前已取得了中国国家药品监督管理局颁发的医疗器械注册证,完成了欧盟 CE 认证,并获得了欧盟自由销售证书,
什么是EUA申报
根据美国《联邦食品、药物和化妆品法案》第564条,在紧急情况下,当现有市场的产品无法满足需求时,FDA官员可以允许,将未经FDA审批的医疗产品或现有医疗产品中未审批的新应用,用于诊断、治疗、预防威胁到生命的疾病或情况。通常情况下,紧急使用授权(英文全称“Emergency Use Authorization”,简称“EUA”)的申报分为两个阶段,紧急使用预授权(英文全称“Pre-EUA”)和紧急使用授权(英文全称“EUA”)。
华大基因本次紧急使用预授权尚在审核过程中,后续还需要FDA的进一步反馈与认同,才能获批EUA
FDA允许符合条件产品面向临床商业销售
根据目前新型冠状病毒在美国的蔓延情况,FDA于当地时间2020年3月16日发布《新型冠状病毒肺炎在公共危机下的诊断检测政策指南》(英文全称“Policy for Diagnostic Tests for Coronavirus Disease-2019 during the Public Health Emergency”,以下简称“《指南》”),根据《指南》相关内容显示,符合条件的产品可以面向临床市场进行商业销售。在《指南》条款下,公司已向FDA报备产品用途等相关信息,并提交销售意愿,在基于现有的方法学验证基础上,FDA已接受公司的产品申报,并允许公司在EUA获批前,即自2020年3月17日起,在美国临床市场销售其新型冠状病毒SARS-nCoV-2核酸检测试剂盒(荧光PRC法)产品。在紧急情况有效期内,公司上述检测产品符合《指南》所述的商业销售条件。如果在紧急情况终止后,公司仍希望在美国临床市场销售该产品,则需要另行向FDA提交产品注册申请
截至目前,根据美国 FDA 官网信息显示,已有 8 家国外企业或机构的新型冠状病毒检测产品获得了美国 FDA 的紧急使用授权。
[来源:仪器信息网] 未经授权不得转载

3626.7万元!中华人民共和国广州海关10月拟采购超过40台/套仪器设备
2024.08.26

4821.56万元!厦门大学9月仪器采购意向公布:聚焦生命科学领域
2024.08.26

2024.08.21
2024.08.21

2024.08.20

涉及大量仪器设备,成都发布53.6亿预算大规模设备更新需求清单
2024.08.19
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~