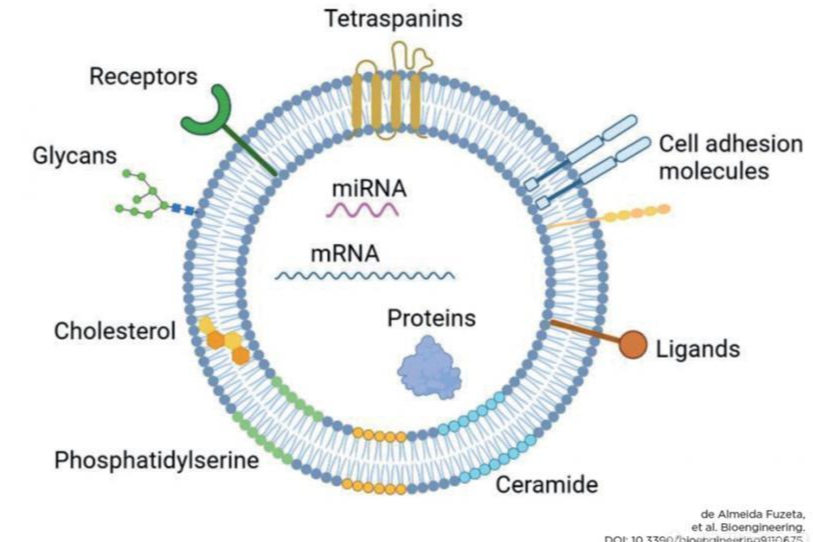
【直播预告】高维流式数据分析系列课程:从理论到实战——第一期
课程主题:高维流式数据分析系列课程:从理论到实战——第一期【高维数据的艺术:用 Cytobank 实现降维分析的最佳实践】课程时间:2024/09/19 14:00课程简介:在流式细胞术中,随着数据维度的增加,传统的散点图和直方图 无法充分展示隐藏在多维数据中的细胞群体差异。面对这样的挑战,降维分析成为解锁数据复杂性、揭示重要科研发现的关键工具。如何在二维图像中揭示复杂的群体模式?Cytobank 平台提供了先进的降维分析工具,帮助您将复杂的数据高效转化为直观图表。主要内容包括•掌握 viSNE、opt-SNE 和 UMAP 等主流降维算法,生成高质量的科研图表。•优化数据工作流,实现raw data to P value的丝滑操作。•通过实操案例,全面理解数据背后的科学逻辑,提升科研效率。讲师简介:喻龙 贝克曼库尔特生命科学高级应用专家毕业于武汉大学,拥有丰富的国际学术交流经验,曾在澳大利亚莫纳什大学和美国国家犹太健康中心分别进行为期一年的研究交流,在流式细胞术领域具有丰富的专业知识和实践经验。施敏 贝克曼库尔特生命科学高级应用专家专注于流式细胞术的最新技术和应用,拥有超过 10 年的流式细胞术工作经验。精通流式细胞术实验管理,在样本实验设计、数据分析、实验流程优化方面具有丰富的经验。扫描二维码报名
企业动态
2024.09.14
直播预告-从大规模纯化到标准化检测:外泌体载体成药之路
讲座主题:从大规模纯化到标准化检测:外泌体载体的成药之路讲座时间:9月25日(周三)14:00参与方式:>>>点此报名或扫描下方二维码报名参加讲师简介:王金丽 贝克曼库尔特生命科学高级应用专家• 负责流式细胞仪的应用开发、技术支持等售前及售后工作。• 熟悉肿瘤免疫、细胞生物学和生物制药等领域的前沿进展,并且在流式分析/分选、小颗粒流式检测和多色方案设计方面具有卓越的技能。马骁 健新原力病毒载体事业部负责人• 博士毕业于中国科学院遗传发育所,拥有近8年生物制药行业经验。• 曾在PD,MST等多个部门任职,拥有early-stage工艺开发的研发经验,以及late-stage如技术转移,工艺表征,工艺验证,大规模GMP生产等过程的经验。• 主导或参与了多个项目的IND申报,多个项目的技术转移以及2个产品的BLA申报。王聪 高级产品专家• 博士,拥有8年生命科学领域各类仪器服务支持工作经验。• 现负责贝克曼库尔特生命科学离心机产品线的技术支持服务工作。熟悉不同样品离心分离制备技术和各种应用场景。讲座内容:• 14:00 – 14:30 纳米流式细胞术:更清晰的EV视界揭示细胞外囊泡(EV)异质性从而挖掘其在疾病诊断和治疗中的应用潜能是近年来备受关注的研究方向。想要真正了解EV,准确且可重复的检测技术至关重要。纳米流式细胞术是一种能够提供包括表面特异性、粒径、浓度等多维度单颗粒信息的尖端技术,使研究人员能够以卓越的精度和灵敏度分析和表征EV,研究其异质性。• 14:30 – 15:10 外泌体载体的成药性之路围绕成药性,分享外泌体作为先进治疗药物载体的现状,从载药方式和CMC两个方面介绍了外泌体的优势和挑战,涉及外泌体的生物学发生过程,作为药物载体的现状、发展,工艺开发过程中的问题等等• 15:10 – 15:40 外泌体超离纯化:从小体积到大规模伴随着细胞外囊泡(EV)研究和临床工业应用的发展,对于EV纯化体积的需求与日俱增。本次分享将围绕如何使用超速离心机应对从研发阶段的少量样品,到小试或者中试时的几升样品,最后到大规模生产时的几十升体系。涉及离心原理,设备搭配,转子耗材选择等内容。• 15:40 答疑
企业动态
2024.09.13
除了美容,合成生物学还在生活的这些方面帮助我们
相对于“医疗美容”,“生活美容”是非侵入非创伤性的,是指运用化妆品、保健品和非医疗器械等,采用涂擦、喷洒或者其他类似方法,应用于皮肤、毛发、指甲、口唇等人体表面部位,达到清洁、消除不良气味、护肤、美容和修饰的目的。目前,通过合成生物学结合基因编辑技术合成的化妆品原料有:透明质酸、羟基积雪草苷、角鲨烯、白藜芦醇、辅酶Q10、胶原蛋白、茶多酚,广泛应用于护肤面霜、精华液等产品中,分别起到保湿、抗炎、修复、抗氧化抗衰等功效。通过工程酵母发酵生产的Valencene和Nootkatone分别被用于香水和化妆品中以提供橙子和葡萄柚的香气;同样,通过对藻类进行改造,总部位于加州旧金山的Solazyme将这些微藻自然产生的油供应给丝芙兰用于添加到其所销售的化妆品之中。由于具有开发时间短、开发成本和风险低等特点,越来越多的化妆品原料通过发酵的方式替代传统的从自然界提取的方式,国内也有越来越多的企业通过合成生物学新技术成为众多品牌化妆品企业的原料供应商。随着合成生物学的快速发展,其所涉及的技术范围也不断扩大,并与其他领域有相当大的重叠,除了通过生物勘探技术筛选鉴定天然源小分子、大分子的生物活动,发展化妆品、生物修复和药物等产品外,还在科研和工业中使用的技术有:遗传元件(启动子、终止子、RBS)、广谱宿主质粒、代谢工程、DNA测序、密码子优化、DNA数据存储、蛋白质工程、CRISPR-Cas、多路复用基因组编辑、高通量筛选和自动化、微生物组工程、DNA组装、基因驱动、无细胞系统、遗传逻辑电路、建模和机器学习、DNA合成、定向进化;仅停留在科研阶段的有:基因组小型化、自组织多细胞结构、合成染色体、异种生物学和合成细胞器。这些技术未来将进一步推动合成生物学成为下一代生物制造,形成一场制造革 命,探索替代原料和生产工艺,并进一步延伸到开发性能更好的产品,广泛影响我们的生产和生活。1新一代生物制造利用微生物按需生产化学品、利用农业和能源作物、二氧化碳、农业和工业废物等原料生产生物基燃料和化学品、新型功能材料和利用藻类生产生物燃料。2007年国务院发布的“限塑令”,将生物降解塑料材料推向了历史舞台,而其中的“种子选手”则是聚乳酸(PLA),广泛应用于一次性餐具、塑料包装、3D打印等领域。Total Corbion PLA位于泰国罗勇府的设计年产能7.5万吨PLA的工厂已实现满产运行,同时又宣布将在法国Grandpuits建造第二家即欧洲第一家产能10万吨的PLA工厂。全球PLA第一梯队除了Total Corbion之外,还有美国NatureWorks公司,中国丰原集团和海正生物材料公司,其中丰原集团依托自身发酵国家工程研究中心还实现了年产3万吨一步发酵法L-苹果酸生产示范线建设;浙江海正2023年更是将PLA年产能扩大到15万吨。作为基于化石燃料的传统塑料的替代材料,使用微生物发酵还可生产的生物降解聚合物有,聚丁二酸二醇酯(PBS)和聚羟基链烷酸酯(PHA),通过合成生物学研究可优化筛选宿主生物、酶和代谢途径。作为亚洲为数不多的通过微生物发酵进行PHA商业生产的企业,BluePHA蓝晶微生物已建成年产5000吨的超级工厂,并将在二期形成25000吨的年产能供应。日本的 Spiber 和美国的 Bolt Threads 等公司已经开发出源自蜘蛛丝蛋白的发酵产品,这些产品重量轻,具有理想的机械性能。总部位于新加坡的丰益国际(Wilmar International)和美国的Elevance在印度尼西亚成立了一家合资生物精炼厂,产能为180kMT,利用当地的棕榈油生产新型特种化学品。通过开发CO2光合代谢工程,台湾科学家使用蓝藻生产丁酸盐。2未来医学使用活细胞和无细胞系统按需生产、使用CRISPR - Cas对遗传性疾病进行精确的基因组编辑、工程微生物和噬菌体作为治疗药物、CRISPR - Cas用于病毒的敏感检测。在重组DNA技术出现之前,大多数药品仅限于小分子,而合成生物学通过扩大治疗药物生产能力,将进一步推动制药行业的进步。第一个商业化合成的人胰岛素于1982年利用工程大肠杆菌生产,替代了从动物中提取它的历史标准;而青蒿素和大麻素的微生物生产则是替代了传统植物的来源;而无细胞系统(CFPS)由于可以采用冻干方式,具有便携式、按需生产的特点,可生产从小分子、短肽到抗体偶联物和疫苗等药物,未来将彻底改变药品的制造和分销模式。2017年FDA批准了首个CAR-T细胞疗法,随后2018年又为第一个直接给药的基于病毒载体的基因疗法上市开绿灯,此外,工程化免疫细胞又进一步拓展到NK和巨噬细胞,工程细菌、单物种或多物种联盟也正在开发用于皮肤、胃肠道和其他微生物组相关疾病,工程噬菌体也被用于高效特异性抗菌剂应用于强化癌症治疗,这些开创性的细胞和基因疗法的例子预示着合成生物学将为未来医学带来更多的治疗创新。3粮食、农业和环境基因组编辑作物,提高产量、抗病性和改善营养,微生物肥料,微生物降解传统塑料,工程微生物回收电子废物。民以食为天,面对当前人口增长所带来的粮食安全的挑战,全球在粮食和农业技术方向进行了大量的投资,主要聚焦在提高农作物产量和改善营养成分两个方向。基因组编辑驱动的精确育种大大提高了植物合成生物学选择理想性状的效率;有三种策略可以提高作物的产量,即提高固碳效率、最大限度地减少植物呼吸性CO2损失和建立非豆科作物固碳机制;通过基因组编辑技术设计香米、设计含有维生素A原的“黄金大米”用于改善维生素A缺乏地区营养负担、设计增强小麦对白粉病的抵抗能力、提高水稻抗细菌枯萎病能力;利用酵母生产母乳低聚糖作为配方奶的补充、生产植物或动物细胞替代蛋白产品用于替代能量和资源密集型动物肉等。而早在2014年,瑞士合成生物学公司Evolva就利用基因编辑技术使用酵母将糖转化为食品添加剂香兰素。总部位于美国的Pivot Bio开发出了一种基于微生物的玉米肥料,有望取代传统肥料避免化学污染的同时,更好地提高作物产量;除了前文提到的替代传统塑料的生物降解聚合物外,还可通过在提高PTE降解菌Ideonella sakaiensis和两种关键酶的效率,通过合成生物学蛋白质工程实现酶的定向进化,降低塑料污染;此外,还可通过基因工程微生物生物积累进行重金属和稀土元素的回收,减少电子废物污染和提升回收效率升级回收模式。工欲善其事必先利其器,合成生物学大规模试错工程实验对生物制造的发展形成了巨大的挑战,这些挑战超出了传统的劳动密集型研究方法的能力,因此,建立高通量工程研究平台势在必行。随着全球各个国家对合成生物学下一代生物制造的重视与投入,国内外许多公司和研究机构都开发了以自动化合成生物学技术为中心的自动化DNA组装平台BioFoundry,这些BioFoundry的建立,既适用于研究,也适用于工业应用,为简化复杂的研究程序和促进各领域创新提供了无与伦比的强大动力。作为全球领先的实验室自动化制造商,贝克曼库尔特生命科学为您提供专业的从硬件到软件,以及应用开发整体解决方案,在合成生物学、基因组和蛋白质组研究等各个领域享有很高的声誉。秉承创新、简单易用、智能与自动化的理念,同时兼顾国际化和本地化的技术服务,不仅能提高实验处理通量和效率,更能保证高质量的结果产出。正因如此,Lesaffre Biofoundry通过3台Biomek液体处理工作站,Echo声波移液系统及超过60种设备的整合系统,实现将原有手工处理样本的传统方式进化到每天处理数千个。例如在第二轮菌株筛选中,采用多种菌株表型assay或生长监测,评估分离在384孔板中的不同菌株。该Biofoundry可以处理高达100,000菌株,对一些特定方法每天可开展20,000个assays。相信未来在小贝和众多Biofoundry的共同协作与努力下,更多的生物制造产品将不断推陈出新,以更节能、环保、健康的方式深入影响我们生活的方方面面。图 Lesaffre Biofoundry参考文献1、化妆品与医疗美容产品科普知识之一:医疗美容产品不是化妆品 应由医生操作使用;国家药品监督管理局https://www.nmpa.gov.cn/xxgk/kpzhsh/kpzhshhzhp/20190905160901577.html2、Hayden EC. Synthetic-biology firms shift focus. Nature. 2014 Jan 30;505(7485):598. doi: 10.1038/505598a. PMID: 24476868.3、满负荷!Total Corbion PLA泰国官宣7个季度达成10万吨里程碑 下一个丰原?海正?;聚如如咨询https://jururu.info/news/7624、“椒”傲|海正生材:做国内聚乳酸的“拓荒者”;澎湃新闻https://www.thepaper.cn/newsDetail_forward_195477745、Mao N, Aggarwal N, Poh CL, Cho BK, Kondo A, Liu C, Yew WS, Chang MW. Future trends in synthetic biology in Asia. Adv Genet (Hoboken). 2021 Mar 5;2(1):e10038. doi: 10.1002/ggn2.10038. PMID: 36618442; PMCID: PMC9744534.6、Ma Y, Zhang Z, Jia B, Yuan Y. Automated high-throughput DNA synthesis and assembly. Heliyon. 2024 Feb 25;10(6):e26967. doi: 10.1016/j.heliyon.2024.e26967. PMID: 38500977; PMCID: PMC10945133.
应用实例
2024.08.09
实验室自动化:中药研究的创新催化剂
前言在全球化的今天,人们对健康的需求日益增长,作为中华民族几千年智慧的结晶,中药的价值逐渐被重新发现和重视。然而,传统中药研究方法在面对现代医药需求时,显得力不从心。为了更好地发挥中药在现代医疗体系中的作用,中药研究现代化势在必行。中药现代化的发展趋势是走向科技化,通过科技创新以及多学科融合,构建适合中医药特点的技术方法和标准规范体系。这包括对中药有效成分的深入分析以及通过药理学、药效学、毒理学研究等提高药效和安全性,推动中药从经验医学向精准医学的转变,确保现代中药具备有效性、安全性和可审查性。实验室自动化是指使用自动化技术来执行实验室任务,最小化或无须人工干预,以提高生产力、提高实验数据质量、缩短实验周期或完成原本不可能开展的实验。在中药研究的漫长历程中,实验室自动化设备正扮演着越来越重要的角色。这些高科技设备不仅提升了研究的效率和精度,还为中药的现代化研究打开了新的大门。提升研究效率 中药成分复杂,研究过程繁琐。实验室自动化设备可以通过精确控制实验条件,减少人为误差,大幅提升实验的重复性和可靠性。例如,高通量筛选系统,具有微量、快速、灵敏和准确的特点,能够在短时间内对成千上万种化合物进行筛选,快速识别出具有特定药效的分子;甚至可以结合中药复方配伍理论,轻松实现药物组合筛选,为中药的精准治疗提供了可能。保障转化质量中药的安全性和有效性是其能否被广泛接受的关键。随着中药研究的深入,药效评价和毒理学评价方法也在不断创新,评价方法越来越多样化。传统的动物实验存在伦理和成本的多重挑战,而基于细胞模型的体外试验更易于大规模应用。例如,利用肝脏类器官模型,可以研究中药成分对肝脏的毒性和代谢途径,评估其潜在的肝毒性。促进国际交流与合作随着中药走向国际市场,符合国际标准的中药研究变得尤为重要。自动化设备的应用,使得中药研究更加规范化、标准化,有助于中药在国际医药体系中获得认可和信任。新药发现全靠数字,然而跟踪数十亿细胞或数百甚至数千个化合物所设计的数据量非常庞大。实验室自动化设备和软件可以帮助管理追踪日益增长的实验数据的变化,确保数据的准确性和可追溯性。激发创新潜力实验室自动化设备不仅提高了研究的效率和精度,还为研究人员提供了更多的时间和空间去思考和探索。随着中药研究的深入,针对中药有效成分在体内的作用机制、代谢过程等已广泛使用系统生物学方法,涉及基因组学、转录组学、代谢组学等前沿技术,实验室自动化设备可以帮助实现复杂样品制备过程,促使更深入、全面的机制研究,发现新的治疗潜力,推动中药研究的创新发展。贝克曼库尔特生命科学自动化方案 纳升级液体处理系统:采用声波移液方式克服了传统移液方式的局限,高精度地移取纳升级液滴,无交叉污染,使分析检测实现微量化,提升筛选速度,节约试剂和药物。此外移取纳升级液体的能力使其在剂量分析实验中采用直接稀释法,因为稀释曲线上每个浓度点均为单独而非连续生成,所以避免了传统化合物稀释方法沿曲线传递误差的风险,显著提高数据质量。 自动化移液工作站:用于准确快速地对样品和试剂进行高通量移液,可以处理从微升到毫升的体积。同时具备可拓展性,可以作为自动化整合系统核心灵活集成第三方设备实现高度自动化。贝克曼库尔特凭借Biomek软件解决方案,助您通过易于操作的智能化软件,高效简化复杂的样品和数据处理工作流程。Ending中药研究现代化,不仅是科技进步的必然选择,也是文化传承和国际交流的需要。实验室自动化设备的应用,是中药研究现代化的重要标志。它们不仅提升了中药研究的科学性和系统性,也为中药的未来发展提供了无限可能。随着科技的不断进步,中药研究将更加精准、高效,为人类健康事业做出更大的贡献。
应用实例
2024.08.09
分选技术新突破:纯度与得率的全面提升
Q为什么CytoFLEX SRT分选能够达到这么高的纯度与得率?仪器这么小的体积,分选细胞的得率却比以前的‘大块头’明显高很多,我感觉以前分选准备那么多细胞好浪费。这是许多体验过CytoFLEX SRT的用户的共同疑问。今天,让我们揭开CytoFLEX SRT卓越分选性能背后的秘密,了解它如何通过双域精准DCD计算实现分选纯度和得率的全面提升。分选液滴延迟(Drop Charge Delay,DCD)的重要性在细胞分选过程中,分选液滴延迟(drop charge delay,DCD)有时也被简写为(drop delay,DD),是指从被检测颗粒通过激光检测点,到形成分选液滴断裂点(break off point,BOP)并施加电荷之间的时间延迟,这一时间延迟通常以“cycle(周期)”为单位表示。这是因为液滴的形成是由分选振荡频率与振幅共同决定,液滴形成的过程被分为若干周期或循环(cycle)。在BOP处,液滴开始与液流断开,带着相应的电荷,经过电场偏转进入收集管中。DCD的准确性对于确保目标颗粒被正确地偏转到收集容器中至关重要。若DCD设置不准确,目标颗粒可能会被错误地分类为废液,导致分选回收率和纯度下降。Rmax全面的分选质控Rmax(maximum expected recovery)是一种用于评估细胞分选仪性能的系统方法,通过计算样本在未分选部分中损失的目标细胞百分比,来确定分选回收率的最大值。与仅依赖纯度的评估方法相比,Rmax提供了更全面的分选性能评估,特别是在分选效率和回收率至关重要时。一般的分选后质控,会将分选细胞进行简单的回测,检测纯度,但实际上会忽略掉分选得率。分选得率相较于分选纯度,更容易受分选液滴延迟的影响。传统技术的局限传统的分选液滴延迟只是机械地使用微球进行简单估算,估计出大致的DCD分布区间,最终确认可能的最优值。但是由于分选过程涉及细胞在不同域中的流体动力学表现,从流动室内到接近喷嘴,再到喷嘴通过,这些都会影响DCD的准确性。在流动室内,鞘液形成的流体动力学聚焦过程中,细胞距离中心轴的位置不同,其流体速度也不同。靠近鞘液流的细胞加速较慢,而位于中心轴的细胞加速较快。通过喷嘴后,由于动量守恒,速度方程又会变化。因此,有些仪器虽然能够通过微球自动估算出DCD的值,但却与Rmax的最优解存在较大误差。例如,Rmax方法获得的最优DCD,得率可以达到90%,但自动计算获得的DCD虽然对纯度没有影响,却导致得率下降。创新的双域精准DCD计算方法CytoFLEX SRT采用了一种创新的双域精准DCD计算方法,结合了时间域测量和空间域分析,确保了计算的精确性和可靠性。时间域测量(DD1) 首先,CytoFLEX SRT通过测量QC微球从激光触发点到专用激光点的行进时间来计算DD1。QC微球是标准化的校准颗粒,能够提供一致且可重复的测量结果。这一步骤确保了初始测量的高精度和可靠性。空间域分析计算(DD2)接下来,CytoFLEX SRT基于高精度图像分析,通过高速摄像技术捕捉液体射流在BOP处的断裂和形成液滴的过程。通过分析这些图像,能够精确计算从QC微球经过专用激光点到BOP的剩余时间。高精度图像分析能够捕捉到微小的时间变化和液体射流的动态变化,确保了更高的时间测量精度。双域精准DCD计算的优势1提高分选精度和回收率通过双域精准DCD计算,CytoFLEX SRT确保分选仪在最佳条件下运行,从而大幅提高了分选的回收率和精度。准确的DCD设置,使得目标颗粒能够被更有效地偏转到收集容器中,减少了样品浪费。2实时监控和调整图像分析提供了实时反馈,允许在分选过程中动态调整DCD。即使在样品条件变化或仪器状态波动时,也能确保分选仪始终在最佳状态下运行,进一步减少误差。3减少实验误差自动化的双域精准方法减少了环境与样本等因素的干扰,通过标准化的操作步骤和自动化计算,保证了测量结果的一致性和准确性。结语通过采用创新的双域精准DCD计算方法,CytoFLEX SRT不仅在分选纯度和得率方面取得了显著突破,还实现了分选过程的自动化与智能化,让流式分选变得竟然如此简单。2024年CytoFLEX家族迎来十周年,我们持续为科研人员提供更加高效和可靠的工具。未来,我们期待更多用户能够体验到CytoFLEX SRT带来的卓越性能和便利,加速科研前沿的探索。参考资料1.PEREZ‐GONZALEZ, Alexis, et al. Evaluation of Sort Recovery via Rmax. Current Protocols, 2024, 4.2: e986.2."Method and apparatus for compensating for variations in particle trajectories in electrostatic sorter for flowcell cytometer" (控制液滴可控充电并与载运流体断开的时间点的的方法以及细胞仪系统) -专利编号: CN101675334B,, 专利持有人: 贝克曼库尔特公司 (Beckman Coulter, Inc.)3."Flow Cytometer Sorter" - 专利编号: US8889072B2, 专利持有人: Beckman Coulter, Inc.
参数原理
2024.07.29
一文揭秘:流式细胞指纹与细胞外囊泡应用
在现代生物医学研究中,流式细胞术(Flow Cytometry)已经成为不可或缺的分析工具。它能够通过分析单细胞的多参数特性,揭示细胞间的复杂异质性。而在这一领域,流式细胞指纹(Flow Cytometry Fingerprint)作为一种前沿技术,正在为我们揭示细胞微观世界的更多奥秘。本期,我们跟随贝克曼库尔特一同探究流式细胞指纹,特别是在纳米流式领域,CytoFLEX nano凭借其独特的技术优势,正在引领这一领域的进展。 什么是流式细胞指纹?流式细胞指纹是指通过流式细胞术获得的细胞或颗粒的特定光学特征,这些特征包括散射光和荧光信号。每一种细胞或颗粒都有其独特的指纹图谱,这些图谱反映了它们的物理和生物化学特性。通过对这些指纹图谱的分析,研究人员能够识别并分类不同类型的细胞,甚至可以在同一细胞群体中发现不同的亚群。传统纳米流式在细胞外囊泡(Extracellular Vesicles, EVs)领域的挑战尽管流式细胞术在细胞分析中取得了巨大进展,但在传统纳米流式领域仍面临一些独特的挑战。一个主要问题是缺乏免疫分型的共识,并且同时检测的荧光信号非常有限。目前,细胞外囊泡(Extracellular Vesicles, EVs)亚群的研究还在起步阶段,并没有像免疫学中那样成熟。免疫细胞可以通过多色免疫分析,利用不同的CD分子的表达谱型(指纹)去定义其亚群,但在EV的研究中,类似的标记和分类标准尚未建立,并且相较于免疫细胞,EV有着更丰富的多样性,可供标记的潜在靶点也更多。 CytoFLEX nano的突破2024年3月份发布的CytoFLEX nano作为一款先进的纳米流式细胞仪(查看:3i流式新品|贝克曼库尔特发布CytoFLEX nano纳米流式分析仪),通过结合散射光和荧光信号的综合分析,显著提高了检测的准确性和灵敏度。CytoFLEX nano纳米流式分析仪品牌:贝克曼库尔特型号:CytoFLEX6荧光通道检测能力,实现精准指纹描述CytoFLEX nano能够同时检测6 个荧光通道,提供更加全面和详细的EV荧光指纹信息。5散射光通道检测能力,释放无限潜力CytoFLEX nano分析仪通过提供5个侧向散射通道扩展了您的研究可能性。通过分析不同散射的比率来研究新群体,而无需依赖染料进行鉴定或分离。这种创新方法不仅提高了实验的灵活性和精度,还为细胞外囊泡研究提供了新的可能性和洞察力。CytoFLEX nano分析仪无疑是未来EV多样性研究的重要工具。高灵敏度,确保捕捉每一个潜在的实验现象与信号在一个细胞外囊泡(EV)上,可能只有10个抗原的拷贝,而目前的流式细胞仪无法测量如此少量的抗原。CytoFLEX nano流式细胞仪的主要优势在于其改进的散射和荧光灵敏度,使得可以测量更小的颗粒并检测低密度的抗原。高阶算法应用:利用Cytobank解析EV“指纹”高阶算法的引入为细胞外囊泡(EV)研究带来了一定的变化。Cytobank平台提供了一系列强大的高阶数据分析工具,如ViSNE、FlowSOM、SPADE和CITRUS,这些工具能够高效解析流式细胞数据,揭示复杂的生物学特征。这些高阶算法在解析EV“指纹”中的应用,使得研究人员能够更精准地解析流式细胞数据,发现传统方法难以识别的细微差异。例如:癌症诊断:利用ViSNE分析癌症患者血液中的EV,发现特定的EV亚群与癌症类型和阶段相关联,为早期诊断和个性化治疗提供了新的生物标志物。心血管疾病研究:通过FlowSOM聚类分析心血管疾病患者的EV数据,识别出与疾病进展相关的特定EV亚群,为疾病机制研究提供了重要线索。免疫监测:利用SPADE分析免疫治疗前后患者的EV变化,揭示免疫反应的动态过程,为评估治疗效果提供了新的视角。差异分析:使用CITRUS对不同病理状态下的EV进行差异分析,发现与疾病相关的特定细胞亚群,帮助识别潜在的生物标志物。von Lersner, Ariana K., et al. "Multiparametric single-vesicle flow cytometry resolves extracellular vesicle heterogeneity and reveals selective regulation of biogenesis and cargo distribution." ACS nano 18.15 (2024):10464-10484.所见即所得,利用CytoFLEX SRT实现分选与分析的相互验证。CytoFLEX nano不仅让研究人员能够在EV分析阶段实现“所见”,更通过CytoFLEX SRT的精确分选功能,将这些识别出的EV亚群进行进一步的分选和深入分析,实现“所得”。这种协同工作流程,确保了数据的准确性和可靠性。CytoFLEX nano与CytoFLEX SRT的结合,为EV研究提供了一个强大的工具组合。前者通过高灵敏度的多通道检测,实现对细胞群体的初步识别;后者则通过精准的分选功能,对这些群体进行进一步的验证和分析。这一协同工作流程,使研究人员能够在分子水平上揭示EV的复杂特征和生物学功能,开拓新的研究领域和应用前景。通过这种多种方法的联动,科学家们能够更全面地理解EV的特性,从而在疾病诊断、治疗和预防中发挥更大的作用。CytoFLEX nano和CytoFLEX SRT的完美结合,真正实现了分选与分析的相互验证,尽可能捕捉到每一个潜在的EV亚群。John Tigges, DirectorFlow Cytometry Core Facility and Center for Extracellular Vesicle Detection, Beth lsrael Deaconess Medical Center“Having all these scatters at hand together with the greater sensitivity gives you the power to ask, what could I do now?lt opens up new research possibilities.“拥有这些散射通道以及更高的灵敏度,让你可以问自己,我现在还能做些什么?这开启了新的研究可能性。” 数据示例通过流式分选验证散射光流式细胞指纹的真实性在细胞外囊泡(EVs)的研究中,准确识别和表征其特性是至关重要的。使用CytoFLEX Nano流式细胞仪,我们能够通过高灵敏度的散射光检测捕捉到EVs的初步指纹信号。然而,为了验证这些散射光指纹的真实性,我们进一步利用CytoFLEX SRT进行精确分选。通过分选前后的对比分析,并使用标准微球验证散射光信号的差异,我们确保了这些指纹的准确性和可靠性。使用CytoFLEX SRT对在CytoFLEX Nano上观察到的不同散射差异信号进行分选,并通过回测确认这些差异的真实存在。同时,CytoFLEX SRT的精确分选功能也得到了验证。 结语CytoFLEX家族和Cytobank的结合,为细胞外囊泡(EVs)研究提供了一个强大且全面的分析工具组合。通过纳米流式细胞术,研究人员能够捕捉到EVs的复杂指纹信号,并通过精确分选技术,进一步验证和深入分析这些信号的真实性。这种多方法学联动,不仅提高了数据的准确性和可靠性,还揭示了EVs在不同生理和病理状态下的潜在作用。高灵敏度的散射光和荧光检测能力,加上Cytobank平台的高阶算法,使得研究人员能够更全面地理解EVs的特性,从而在疾病诊断、治疗和预防中发挥更大的作用。通过这些先进技术的应用,EVs研究已经进入了一个新的纪元,开创了更多的研究领域和应用前景。CytoFLEX nano和CytoFLEX SRT的完美结合,为现代生物医学研究带来了前所未有的便利和创新。未来,我们有理由相信,随着技术的不断进步和应用的不断深入,流式细胞术将继续在EVs研究中发挥关键作用,为生命科学的探索开辟更多可能性。贝克曼库尔特CytoFLEX SRT桌面型流式细胞分选仪品牌:贝克曼库尔特型号:CytoFLEX
媒体关注
2024.07.26
团聚细胞计数的应用解决方案:Cell Type参数优化
前言Vi-CELL BLU细胞计数和活率分析仪最少仅需170uL样品体积即可得到细胞密度和活率结果。为了准确分析不同细胞,Vi-CELL BLU提供了创建和优化自定义Cell Type设置的功能。本文我们拿容易团聚的HEK293细胞给大家介绍下Cell Type的设置是如何影响样品的处理和图像分析。在分析团聚细胞时,Cell Type设置中首先会使用到的参数是Decluster degree,我们可以设置为None,Low,Medium或High,并且使用更靠后的值会增加软件对团聚细胞的识别能力。当出现过多的团聚,我们还需要考虑增加对样品的Aspiration和Mixing Cycles次数。在每次Aspiration过程中,细胞样品会在样品管和注射器之间来回吹打混悬。对于那些很难混悬分散或倾向于粘到样品杯壁上的细胞样品,建议使用这种方法。在Mixing Cycle过程中,台盼蓝和细胞样品一起在样品管和注射器之间来回混匀。增加Mixing Cycles次数会让台盼蓝混匀地更好。Vi-CELL BLU细胞计数和活率分析仪的设计降低了剪切力对细胞的伤害。另外,低剪切力可以提高结果的重现性。但增加Aspiration或Mixing Cycles会提高额外剪切力,从而对比较脆弱的细胞产生潜在的危害。但是,对于团聚细胞系,这些额外的剪切力则可以用于破坏细胞的团聚。Decluster degree和Aspiration/Mixing Cycles之间重要的区别在于它们是在哪个时刻影响的分析结果。Decluster degree只对测试结束后保存在软件上的细胞照片根据不同设置的Decuster degree重新进行分析。而Aspiration和Mixing Cycles是在拍照前对细胞样品就产生了影响,测试结束后无法再修改Aspiration和Mixing Cycles数值,得到再分析的结果。因此,优化Cell Type对于得到好的结果很重要,本文中对于团聚细胞分析,如何调整Cell Type提供了一些指导。团聚的细胞悬液也是细胞培养条件欠佳的指标,包括但不限于过度消化、环境应激、过度生长和污染。细胞团聚限制了细胞对资源和可用增殖空间的获取。这将阻碍细胞生长,降低通量,并影响下游分析结果,譬如像流式细胞仪分析方法需要单细胞溶液。此外,ISO 20391-1(4)中声明,为了获得最佳计数结果(与所使用的分析方法无关),需要单细胞悬浮液,并且需要正确的样品制备流程。Vi-CELL BLU 细胞计数和活率分析仪用红色框标记(非常)大的细胞团。由于对大细胞团进行计数容易出错,因此这些大细胞团不会进行去团聚处理,并会自动从计数中排除。这些大细胞团的数量可以在结果文件的“Cluster Count”中找到,这是培养物中细胞团聚的良好指标。如果观察到细胞团较多时,建议进一步优化培养条件或进行样品处理。方法这些实验中使用的是FreeStyle 293-F 细胞(Thermo Fisher,Cat.编号:R79007)。将 HEK 悬浮细胞在含有FreeStyle 293(30 mL)表达培养基的 50 mL Falcon 管中培养,每 3-4 天传代培养一次,接种细胞密度为 0.2x106 个细胞/mL。它们在 37°C、250 rpm 和 5% CO2 浓度下孵育。使用培养 4 天的细胞样品进行初始测量,在Normal模式下使用Mammalian Cell Type重复测量 5 次。然后结果被导出(每 10 张图像照片保存一张)并离线重新分析。为了重新分析,基于默认的Mammalian Cell Type创建了另外两个Cell Type,但将去团聚度设置为Low和High。为了研究不同去团聚度设置的有效性,比较了这三种Cell Type总细胞密度和活细胞密度以及活率的结果。之后,开始用 HEK 293-F 细胞进行新鲜培养,并在第 0、1、2、3 和 6 天取样。然后,测试了其他采样参数,因为所有日期的样品都用默认的Mammalian Cell Type,以及将Aspiration和Mixing Cycles增加到10次的Cell Type。在所有采样日,将细胞培养液用 5 mL 移液器混合 2 次,然后将 5 mL 细胞培养液转移到 15 mL Facon管中。接着,用 1000 μL 移液器将样品再混合 3 次,再将 3 x 500 μL 细胞样品转移到 Vi-CELL XR 细胞计数和活率分析仪样品管中,以及将 6 x 200 μL 细胞样品转移到 Vi-CELL BLU 96 孔板中。Vi-CELL XR 细胞计数和活率分析仪上的样品,使用图 1 所示的Cell Type分析;在Vi-CELL BLU细胞计数和活率分析仪上,两种Cell Type交替进行。然后,将 2 x 10 μL 细胞样品与台盼蓝 1:1 混合并转移到一次性血球计数板中手动计数。图1:Vi-CELL XR上的分析设置,选择的设置类似于Vi-CELL BLU上的设置然后,在Vi-CELL BLU细胞计数和活率分析仪上运行的样品以High Decluster degree重新分析,在 Vi-CELL BLU 细胞计数和活率分析仪上共生成4种不同的细胞计数结果,以与 Vi-CELL XR细胞计数和活率分析仪的结果和手动计数结果进行比较。表1. Vi-CELL BLU分析HEK 293-F的Cell Type,Mammalian Cell Type作为其他3个Cell Types的模板。结果在三个Decluster degree下(Low,Normal和High)得到的平均总细胞密度和活细胞密度(分别为 TCD 和 VCD)和活率进行了比较(图2)。更高的去团聚度使得TCD 和 VCD 值均明显增加(R2 > 0.98)。然而,使用较低或较高的Decluster degree时,细胞活率却并不显著增加或减少。图2:Vi-CELL BLU使用不同Decluster degree设置分析HEK 293-F的结果。平均总细胞和活细胞密度显示在左轴上,平均活率显示在右轴上。误差线表示标准差。表 2 中的图像显示了Decluster degree如何影响样品分析,从而影响细胞浓度结果。所选图像是图2中其中一个测量样品的图像(部分),并且很好地表示了细胞样品的状态。如前所述,HEK 293 F细胞倾向于形成团聚体,而这些团聚体中的细胞可能难以计数准确。当 Decluster degree 设置为 low 时,某些团聚将不再被解聚,并且标有蓝色圆圈,表示Vi-CELL软件错误地将它们识别为单个颗粒,因为其尺寸较大,根据所选Cell Type参数未归为一个细胞。通过更高的去团聚度,可以分析更多这些团聚细胞,从而产生单个团聚标记为Normal Decluster degree,所有团聚细胞均在High declustering下进行分析。更高的Decluster degree设置会导致识别出额外的细胞,可能导致人为地提高细胞密度,因为单个细胞可能(几乎)分裂成两个或多个颗粒。这些颗粒是被忽略还是算作活细胞或死细胞取决于其他Cell Type参数,例如大小、圆度和亮度。因此,优化Cell Type设置对于获得准确的结果很重要。表2. 不同Decluster degree设置的分析结果,随着Declustering增加,更多的细胞团聚被分析,细胞团聚体中更多的细胞被识别。请注意,Cluster count不受Decluster degree的影响。对于“Low”和“High”设置,每次测量平均计数 1.6 个Clusters。Cluster count指示在样本中发现了多少个过大的细胞团聚体。这些Cluster用红色框标记,并且无论Decluster degree如何,都完全排除在分析之外。因此,高的Cluster count是大细胞团聚体的良好指示,需要在培养处理或样品制备方面进行额外优化,以获得准确的细胞计数结果。最终,在优化Cell Type设置时,Vi-CELL BLU 软件还提供了增加Aspiration和Mixing cycles的可能性。增加Aspiration和Mixing的影响评估,是使用默认的Mammalian Cell Type,将其中的Aspiration和Mixing cycles都设为10,每天对 HEK 293-F 细胞样品进行采样,并一式三份测定细胞密度。之后,使用表1所述的High Decluster degree重新分析所有测量值。将结果与使用Vi-CELL XR细胞计数和活率分析仪及手动计数获得的值进行比较(图3)。图3: Vi-CELL BLU用4种不同Cell Types检测的总细胞密度和活率(蓝-灰色),Vi-CELL XR(红色)和手动细胞计数(绿色)。误差线表示标准差。图 3 显示了 Vi-CELL XR细胞计数和活率分析仪、血球计数板、Vi-CELL BLU 细胞计数和活率分析仪(使用默认Mammalian Cell Type)测试6天得到的细胞密度和活率具有可比性。此外,Mixing增加和/或High declustering的Cell Type会导致更高的细胞密度。在第3天,测量的平均 TCD 介于 2.81 – 4.12 百万个细胞/mL 之间,分别使用默认的 Mammalian 和 Mammalian A10M10 High decluster。因此,与默认设置相比,更改两个参数后结果增加了 47%。然而,在第6天存活率下降到~70%,而且手动计数的TCD明显比自动细胞计数仪的TCD更高。表 3 中的图像(通过显微镜显示 Neubauer 分析室)为这种偏差提供了清晰地解释,因为与第 3 天相比,第 6 天的细胞样品中显示有更多的细胞聚集体。这些细胞聚集体很难计数,在分析过程中将完全忽略大的团聚细胞。表3: 第3和第6天HEK 293-F细胞计数显微镜下的照片。第6天可以看到更多的细胞团聚体,细胞活率降低。专注于培养的前 3 天(图 4)可以进一步研究不同的Cell Type设置如何影响计数结果。第 3 天血球计数板图像(表 3)显示,到目前为止,细胞主要以小聚集体或单细胞形式生长。仔细观察Cluster count可以发现,Clusters的平均数量从第 1 天的 0.7 个增加到第 2 天的 3.7 个和第 3 天的 8.7 个。同时,更高的Mixing和Aspiration cycles的效果似乎有所增加,第 1 天的 TCD 增加了 4%,而第 2 天和第 3 天分别增加了 17% 和 25%。在Mammalian A10M10 High decluster设置下的结果一直是最高浓度。图4: HEK培养的前3天。在 Vi-CELL BLU 上以蓝灰色以及 Vi-CELL XR(红色)和手动计数(绿色)测定四种不同的细胞密度和活率。误差线表示标准差。总之,每日采样结果进一步证明了正确Cell Type设置的重要性。仅改变三个参数就导致 TCD 增加 47%。测量团聚的HEK细胞时,调整Decluster degree和Mixing/Aspiration cycles可以得到更高的TCD。然而,第6天的数据(图3)表明,应避免过度团聚的细胞样品,因为与手动计数相比,所有Cell Type的结果都明显较低。讨论本文讨论了使用 Vi-CELL BLU 细胞计数和活率分析仪优化细胞计数结果的几种选择。除了优化一般的培养处理 - 这将改善细胞健康、通量和产率 – 可以通过调整样品处理和分析来改进。通过演示使用不同Cell Type设置的影响,可以清楚地看出针对所用细胞系和应用优化这些设置对于获得好的分析结果至关重要。在处理倾向于形成聚集体的细胞系时,对Decluster degree、Aspiration cycles和Mixing cycles的拟议更改是优化计数性能的良好起点。但是,当可能需要进一步优化时,请随时向贝克曼库尔特生命科学的相关技术人员寻求支持。 ● 参考资料: 1. Cell Culture Problems: Cell Clumping – Causes, How to Unclump Cells & How to Avoid Cell Clumping. akadeum.com. [Online] Akadeum Life Sciences, February 2021. [Cited: 25 July 2023.] https://www.akadeum.com/blog/cell-clumping/.2. Cell Clumping Troubleshooting. Sigma Aldrich. [Online] Merck KGaA. [Cited: 25 July 2023.] https://www.sigmaaldrich.com/US/en/technical-documents/technical-article/cell-culture-and-cellculture-analysis/mammalian-cell-culture/cell-clumping-troubleshooting. 3. Biomass and Aggregation Analysis of Human Embryonic Kidney 293 Suspension Cell Cultures by Particle Size Measurement. Yung-Shyeng Tsao, Russell G. G. Condon, Eugene J. Schaefer, David A. Lindsay, and Zhong Liu. s.l. : Biotechnology progress, 2000, Bd. 16(5). 809-814.4. ISO 20391-1. Biotechnology — Cell counting — Part 1: General guidance on cell counting methods. s.l. : ISO/TC 276, Biotechnology, 2018-01. First edition. ISO 20391-1:2018(E). 5. Cluster Count Analysis and Sample Preparation Considerations for the Vi-CELL BLU Cell Viability Analyzer. Wu, Andrew. s.l. : Beckman Coulter Life Sciences, 2023. 2023-GBL-EN-101754.5. Cluster Count Analysis and Sample Preparation Considerations for the Vi-CELL BLU Cell Viability Analyzer. Wu, Andrew. s.l. : Beckman Coulter Life Sciences, 2023. 2023-GBL-EN-101754.
应用实例
2024.07.26
流式细胞样本前处理新品:贝克曼库尔特CellMek SPS
2024年上半年,贝克曼库尔特发布了一款全自动样本制备系统CellMek SPS自动加样系统。自 1986 年以来,贝克曼库尔特一直致力于自动化和创新工具,以支持全球实验室的流程优化。现在,通过引入 CellMek SPS 系统进入了精益处理的下一个阶段,该系统旨在实现端到端流式细胞术样品制备工作流程的自动化,无需用户干预。减轻压力。提高灵活性。CellMek SPS 系统能够执行与流式细胞样本前处理相关的多种液体操作,包括自动化细胞清洗,红细胞裂解及抗体染色孵育,支持的标本类型包括全血、骨髓或其他单细胞悬浮液,旨在实现端到端流式细胞仪样品制备工作流程的自动化,进一步帮助用户解决临床流式细胞术实验室中与样品制备相关的主要工艺浪费,从而释放精益的力量,主要实现以下: 通过自动化提高效率。 标准化流程并减少发生错误的可能性。 通过用户定义的协议确保灵活性。 通过完整的审计跟踪确保结果的可信度。 让实验室工作人员能够腾出时间来处理更多增值任务。贝克曼库尔特CellMek SPS自动加样系统
媒体关注
2024.07.26
灭活减毒类疫苗的秘密
在现代医学中,疫苗的研发和生产是保护人类健康的重要环节。灭活减毒类疫苗作为其中的一大类,发挥着不可或缺的作用。那么,什么是灭活减毒类疫苗?它们是如何生产的?在这个过程中,离心技术又扮演着怎样的角色呢?让我们一探究竟。Q什么是灭活减毒类疫苗?灭活减毒类疫苗是指通过物理或化学方法,将病原体(如病毒或细菌)灭活或减毒,使其失去致病性,但仍保留刺激免疫系统产生免疫应答的能力。这类疫苗通过激发人体的免疫系统,形成记忆细胞,从而在真正的病原体入侵时,能够迅速识别并消灭它们。常见的灭活疫苗包括狂犬疫苗、甲肝疫苗,减毒疫苗如黄热病疫苗、麻疹减毒疫苗和百日咳减毒疫苗。工艺流程:从病原体到疫苗灭活和减毒疫苗的生产工艺大致可分为以下几个步骤:01病原体培养在特定的细胞系或培养基中培养大量病毒或细菌。例如,新冠病毒的培养多采用Vero细胞。02灭活/减毒处理通过化学(如甲醛、乙醇)或物理方法(如热处理、紫外线)灭活病毒或细菌,或通过基因工程减弱其毒性。以狂犬疫苗为例,常使用β-丙内酯进行灭活处理。03纯化去除培养基、细胞碎片和其他杂质,获得高纯度的病毒或细菌成分。常用的纯化技术包括离心、层析和过滤。04配制与检测将纯化后的疫苗成分按一定比例配制,并进行质量检测,确保其安全性和有效性。05灌装与包装将合格的疫苗产品进行无菌灌装和包装,准备上市。离心技术在纯化中的应用纯化是疫苗生产中的关键步骤,直接关系到疫苗的安全性和有效性。离心技术在这一过程中具有重要应用,通过高速旋转产生的离心力,将混合物中的不同成分分离开来。01初步分离离心技术首先用于去除大部分细胞碎片和杂质。例如,在甲肝疫苗的生产中,通过低速离心去除细胞碎片。02浓缩和纯化通过超速离心进一步纯化目标成分,去除微小杂质并浓缩疫苗成分。例如,新冠灭活疫苗的纯化过程中,常使用梯度离心技术,提高病毒颗粒的纯度。03质量控制在生产过程中,离心技术还用于质量检测,确保纯化效果和产品质量。例如,分析型超速离心技术AUC检测疫苗中的残留杂质和病毒含量。案例分享01狂犬疫苗生产工艺:使用Vero细胞培养狂犬病毒,随后使用β-丙内酯进行灭活。低速离心去除细胞碎片,然后通过梯度离心和高速离心进行纯化,以提高病毒颗粒的纯度。疫苗随后配制并进行效力和纯度测试。离心技术应用:低速离心用于初步去除细胞碎片;梯度离心和高速离心用于病毒颗粒的纯化。代表性公司:Sanofi Pasteur02甲肝疫苗生产工艺:培养甲肝病毒,然后使用甲醛进行灭活。初步离心分离细胞碎片,随后采用高速离心和色谱技术浓缩和纯化病毒颗粒。最终的疫苗配制并经过质量测试。离心技术应用:低速离心用于初步去除细胞碎片;高速离心用于病毒浓缩和纯化。代表性公司:GSK03COVID-19灭活疫苗生产工艺:COVID-19病毒在Vero细胞中培养,并使用β-丙内酯进行灭活。低速离心去除细胞碎片,随后采用梯度离心进行病毒纯化。疫苗配制并进行效力测试。离心技术应用:低速离心用于去除细胞碎片;梯度离心用于病毒纯化。代表性公司:Sinovac Biotech04麻疹疫苗(麻疹减毒活疫苗)工艺流程:麻疹病毒在特定培养基中培养,然后通过温度敏感的突变体(例如,埃德蒙森株)进行减毒处理,以降低其致病性。离心应用:在去除培养基和细胞碎片阶段使用差速离心技术,纯化阶段使用梯度离心技术,从而提高疫苗的纯度和浓缩度。代表性公司:MSD05乙型流感疫苗工艺流程:使用鸡胚进行病毒培养,然后经过化学处理(如使用甲醛)灭活病毒。离心应用:超速离心用于去除细胞碎片和其他杂质,提高疫苗的纯度,精纯阶段使用密度梯度离心技术,分离杂蛋白。代表性公司:康明斯(CombiMatrix Corporation)拥有相关的生产技术专利,例如用于灭活病毒的化学处理方法。06黄热病减毒疫苗工艺流程:使用鸡胚进行病毒培养,然后经过减毒处理(例如,乙醇处理)。离心应用:用于从培养物中分离和纯化黄热病病毒颗粒。代表性公司:巴西生物制品研究所(Bio-Manguinhos)生产的黄热病疫苗利用了相关的减毒和纯化技术。07百日咳减毒疫苗工艺流程:细菌(百日咳杆菌)在特定培养基中培养,然后经过化学处理(如使用甲醛)灭活。离心应用:用于从培养物中分离和纯化百日咳病毒颗粒。代表性公司:赛诺菲巴斯德公司(Sanofi Pasteur)在百日咳疫苗生产过程中使用了相关的化学处理和离心技术。这些案例展示了不同类型减毒或灭活疫苗的生产工艺及离心技术在其中的应用。每种疫苗的生产流程和应用技术会根据病原体的特性和制造商的具体需求而有所不同。总结灭活和减毒疫苗作为传统疫苗技术的重要代表,凭借其成熟的研发、生产和质量控制流程,依然在疫苗产业中占据重要地位。离心技术等先进纯化方法的应用,不仅提升了疫苗的纯度和安全性,也为大规模生产提供了可靠保障。希望这篇文章能帮助您更好地了解灭活减毒疫苗的生产工艺和纯化技术。如果您对疫苗生产有更多的兴趣或疑问,欢迎在评论区留言与我们互动!让我们共同关注疫苗的发展,守护人类健康的每一天!贝克曼库尔特生命科学离心机助力疫苗生产与研发过程Avanti JXN-26 落地式大容量高速离心机+JCFZ连续流转头•可进行高通量去除细胞碎片,培养基,用于料液澄清,病毒与细胞的分离等•单次处理量高至100L**1%固液比前提下Optima XPN 落地式超速离心机+Ti-15区带转头•可进行高通量密度梯度离心,进行病毒及蛋白颗粒的精纯步骤•单次上样量高至1LOptima AUC 分析型超速离心机•可以在任意选定的溶液中检测蛋白质的构象(折叠或伸展)、聚集的可逆性(相互作用)、化学计量学(解离状态)和异质性(聚合状态);•活性成分分析 •药物配方研究 •API 和药品释放度试验 •API 和药品稳定性 •标准品评价
应用实例
2024.07.26
纳米流式的解析:探索EV“指纹”新视界
在现代生物医学研究中,流式细胞术(Flow Cytometry)已经成为不可或缺的分析工具。它能够通过分析单细胞的多参数特性,揭示细胞间的复杂异质性。而在这一领域,流式细胞指纹(Flow Cytometry Fingerprint)作为一种前沿技术,正在为我们揭示细胞微观世界的更多奥秘。特别是在纳米流式领域,CytoFLEX nano凭借其独特的技术优势,正在引领这一领域的进展。什么是流式细胞指纹?流式细胞指纹是指通过流式细胞术获得的细胞或颗粒的特定光学特征,这些特征包括散射光和荧光信号。每一种细胞或颗粒都有其独特的指纹图谱,这些图谱反映了它们的物理和生物化学特性。通过对这些指纹图谱的分析,研究人员能够识别并分类不同类型的细胞,甚至可以在同一细胞群体中发现不同的亚群。传统纳米流式在细胞外囊泡(Extracellular Vesicles, EVs)领域的挑战尽管流式细胞术在细胞分析中取得了巨大进展,但在传统纳米流式领域仍面临一些独特的挑战。一个主要问题是缺乏免疫分型的共识,并且同时检测的荧光信号非常有限。目前,细胞外囊泡(Extracellular Vesicles, EVs)亚群的研究还在起步阶段,并没有像免疫学中那样成熟。免疫细胞可以通过多色免疫分析,利用不同的CD分子的表达谱型(指纹)去定义其亚群,但在EV的研究中,类似的标记和分类标准尚未建立,并且相较于免疫细胞,EV有着更丰富的多样性,可供标记的潜在靶点也更多。CytoFLEX nano的突破CytoFLEX nano作为一款先进的纳米流式细胞仪,通过结合散射光和荧光信号的综合分析,显著提高了检测的准确性和灵敏度。6荧光通道检测能力,实现精准指纹描述:CytoFLEX nano能够同时检测6 个荧光通道,提供更加全面和详细的EV荧光指纹信息。5散射光通道检测能力,释放无限潜力:CytoFLEX nano分析仪通过提供5个侧向散射通道扩展了您的研究可能性。通过分析不同散射的比率来研究新群体,而无需依赖染料进行鉴定或分离。这种创新方法不仅提高了实验的灵活性和精度,还为细胞外囊泡研究提供了新的可能性和洞察力。CytoFLEX nano分析仪无疑是未来EV多样性研究的重要工具。高灵敏度,确保捕捉每一个潜在的实验现象与信号在一个细胞外囊泡(EV)上,可能只有10个抗原的拷贝,而目前的流式细胞仪无法测量如此少量的抗原。CytoFLEX nano流式细胞仪的主要优势在于其改进的散射和荧光灵敏度,使得可以测量更小的颗粒并检测低密度的抗原。高阶算法应用:利用Cytobank解析EV“指纹”高阶算法的引入为细胞外囊泡(EV)研究带来了一定的变化。Cytobank平台提供了一系列强大的高阶数据分析工具,如ViSNE、FlowSOM、SPADE和CITRUS,这些工具能够高效解析流式细胞数据,揭示复杂的生物学特征。这些高阶算法在解析EV“指纹”中的应用,使得研究人员能够更精准地解析流式细胞数据,发现传统方法难以识别的细微差异。例如:癌症诊断:利用ViSNE分析癌症患者血液中的EV,发现特定的EV亚群与癌症类型和阶段相关联,为早期诊断和个性化治疗提供了新的生物标志物。心血管疾病研究:通过FlowSOM聚类分析心血管疾病患者的EV数据,识别出与疾病进展相关的特定EV亚群,为疾病机制研究提供了重要线索。免疫监测:利用SPADE分析免疫治疗前后患者的EV变化,揭示免疫反应的动态过程,为评估治疗效果提供了新的视角。差异分析:使用CITRUS对不同病理状态下的EV进行差异分析,发现与疾病相关的特定细胞亚群,帮助识别潜在的生物标志物。von Lersner, Ariana K., et al. "Multiparametric single-vesicle flow cytometry resolves extracellular vesicle heterogeneity and reveals selective regulation of biogenesis and cargo distribution." ACS nano 18.15 (2024):10464-10484.所见即所得,利用CytoFLEX SRT实现分选与分析的相互验证。CytoFLEX nano不仅让研究人员能够在EV分析阶段实现“所见”,更通过CytoFLEX SRT的精确分选功能,将这些识别出的EV亚群进行进一步的分选和深入分析,实现“所得”。这种协同工作流程,确保了数据的准确性和可靠性。CytoFLEX nano与CytoFLEX SRT的结合,为EV研究提供了一个强大的工具组合。前者通过高灵敏度的多通道检测,实现对细胞群体的初步识别;后者则通过精准的分选功能,对这些群体进行进一步的验证和分析。这一协同工作流程,使研究人员能够在分子水平上揭示EV的复杂特征和生物学功能,开拓新的研究领域和应用前景。通过这种多种方法的联动,科学家们能够更全面地理解EV的特性,从而在疾病诊断、治疗和预防中发挥更大的作用。CytoFLEX nano和CytoFLEX SRT的完美结合,真正实现了分选与分析的相互验证,尽可能捕捉到每一个潜在的EV亚群。John Tigges, DirectorFlow Cytometry Core Facility and Center for Extracellular Vesicle Detection, Beth lsrael Deaconess Medical Center“Having all these scatters at hand together with the greater sensitivity gives you the power to ask, what could I do now?lt opens up new research possibilities.“拥有这些散射通道以及更高的灵敏度,让你可以问自己,我现在还能做些什么?这开启了新的研究可能性。”数据示例:通过流式分选验证散射光流式细胞指纹的真实性 在细胞外囊泡(EVs)的研究中,准确识别和表征其特性是至关重要的。使用CytoFLEX Nano流式细胞仪,我们能够通过高灵敏度的散射光检测捕捉到EVs的初步指纹信号。然而,为了验证这些散射光指纹的真实性,我们进一步利用CytoFLEX SRT进行精确分选。通过分选前后的对比分析,并使用标准微球验证散射光信号的差异,我们确保了这些指纹的准确性和可靠性。使用CytoFLEX SRT对在CytoFLEX Nano上观察到的不同散射差异信号进行分选,并通过回测确认这些差异的真实存在。同时,CytoFLEX SRT的精确分选功能也得到了验证。结语CytoFLEX家族和Cytobank的结合,为细胞外囊泡(EVs)研究提供了一个强大且全面的分析工具组合。通过纳米流式细胞术,研究人员能够捕捉到EVs的复杂指纹信号,并通过精确分选技术,进一步验证和深入分析这些信号的真实性。这种多方法学联动,不仅提高了数据的准确性和可靠性,还揭示了EVs在不同生理和病理状态下的潜在作用。高灵敏度的散射光和荧光检测能力,加上Cytobank平台的高阶算法,使得研究人员能够更全面地理解EVs的特性,从而在疾病诊断、治疗和预防中发挥更大的作用。通过这些先进技术的应用,EVs研究已经进入了一个新的纪元,开创了更多的研究领域和应用前景。CytoFLEX nano和CytoFLEX SRT的完美结合,为现代生物医学研究带来了前所未有的便利和创新。未来,我们有理由相信,随着技术的不断进步和应用的不断深入,流式细胞术将继续在EVs研究中发挥关键作用,为生命科学的探索开辟更多可能性。如果您对CytoFLEX nano、CytoFLEX SRT和Cytobank有任何疑问或需要进一步了解,欢迎随时联系我们。
应用实例
2024.07.10
新版指南解读 | TBNK性能验证及室内质控怎么做?
淋巴细胞亚群中的T细胞、B细胞和自然杀伤(NK)细胞,即TBNK 淋巴细胞是机体重要的免疫细胞,检测其水平变化能提示机体免疫状态的改变。TBNK 淋巴细胞检测已全面应用于艾滋病、严重急性呼吸综合征(SARS)、慢性乙型肝炎、手足口病、Epstein-Barr 病毒(EBV)感染、流行性出血热等多种感染性疾病患者的免疫评估及诊治,也逐渐成为自身免疫病、肿瘤、器官移植、血液系统疾病、重症监护医疗、老年医学及保健等学科的免疫监测辅助工具。国家卫健委于今年4月更新的《流式细胞术检测外周血淋巴细胞亚群指南》在仪器和项目检测的性能验证及质量控制这块做了大篇幅的更新,从而让TBNK的检测更加规范。而质量控制是结果准确发布的前提,因此做好TBNK的性能验证及质控为临床结果的准确发布保驾护航。今天我们一起来看一看指南的介绍。仪器性能验证01验证时机 新仪器启用前仪器搬移后仪器发生重大维修后(如更换激光、光纤、光电倍增管或流动室等)仪器软件系统更新后仪器性能出现问题或环境严重失控时02验证项目灵敏度散射光灵敏度:采用已知大小的校准微球检测仪器的FSC和SSC。在散射光FSC/SSC散点图上,应检测出直径0.5mm 或更小的微球,或满足仪器出厂声明的要求。荧光灵敏度:流式细胞仪能检测到标准荧光微球上的最少荧光分子数, 可用MESF表示,常用荧光通道应为FITC≤ 200 MESF、PE≤100 MESF 、APC≤200 MESF,或满足仪器出厂声明的要求。以8峰微球检测MESF举例,每个荧光通道获取8峰微球的MFI,根据微球说明书提供的软件,计算相对应荧光通道的MESF。分辨率散射光分辨率:采用EDTA盐或肝素抗凝全血,取适量样品稀释后直接上机测定,标本在FSC/SSC散点图可将红细胞和血小板清晰地区分开;取适量样品裂解红细胞后上机测定,标本在FSC/SSC散点图可将淋巴细胞、单核细胞、粒细胞清晰地区分开,即认为散射光分辨率符合要求。荧光通道分辨率:采用校准微球上机测定,各荧光通道的分辨率CV值应符合制造商声明的要求。荧光通道线性可采用含有不同荧光强度的校准微球(已知其相应荧光素的MESF)进行检测,计算每 一种荧光微球的MFI,以MEFL数(y)和平均荧光强度(x)的线性回归,计算相关系数(r)。相关系数r应≥0.98,此方法适用于校准微球上的荧光素可被定量检测的荧光通道。以FITC/PE通道8峰微球举例仪器稳定性将标准微球充分混匀后上机进行试验,测试完成后利用直方图分析实验结果,计算标准微球的平均荧光强度FL1,连续8小时开机后,再通道条件下重复检测,得到标准微球的平均荧光强度FL2,根据两次检测结果计算偏差,公式见下,每一通道的平均荧光强度变化范围均应在基线值±10%范围内。B=FL1-FL2FL2x 100 %携带污染率使用浓度为5000个/µL~10000个/µL的校准微球上机进行测定,获取至少100000个颗粒,连续测定3 次,计算检测通道内设定区域的颗粒数,分别记为H1、H2、H3;再使用空白溶液上机测定,获取颗粒30s,连续测试3次,计算该检测通道内设定区域的颗粒数,分别记为L1、L2、L3。按照此步骤重复循环3 次。携带污染率=L1-L3H3-L3x 100 %取上述公式计算最大值。携带污染率应≤0.5%。TBNK 性能验证01验证时机项目开展初期更换试剂品牌后更换检测系统后仪器的重大部件维修后02验证项目精密度批内精密度:选取至少5个新鲜全血样品,样品的淋巴细胞亚群细胞计数应覆盖低中高水平。每个标品从荧光染 色到上机检测重复3次,并确保所有测试都在同一台仪器的同一批内测定,整个操作过程由同一个操作 人员完成。先计算每个样品重复3次后检测结果的CV,然后计算所有样品的平均CV,所有样品的平均CV 宜<10%,最大不超过20%。实验室可根据不同水平的淋巴细胞亚群细胞计数设定不同程度的可接受CV 标准。日间精密度:宜使用正常和异常两个浓度水平的全血质控品,每天从荧光染色到上机测定重复操作3次, 至少重 复4天,整个操作过程可由不同操作人员完成。先计算每天每个全血质控品重复3次检测结果的CV值,然 后据此计算每个全血质控品4天的平均CV,最后得出两个全血质控品检测结果的平均CV。判定标准同上。稳定性样品稳定性:验证样品在确定的抗凝及处置条件下的稳定性。采集健康人或患者的样品至少 5 份,即刻染色-裂 解-固定并上机测定,以此结果作为基线参考水平,按照实验室的具体环境温度控制条件和预期的样品待检时间,在抗凝剂保存时间内,设置不同的时间点对上述样品进行重复处理和上机测定,获取检测结果,并与基线水平结果进行比较,以相对偏差或绝对偏差表示,检测结果应符合实验室制定的验证要求。淋巴细胞亚群计数过低者,宜以绝对偏差进行验证;亦可对试剂说明书声明的稳定性条件进行验证。处理后标本稳定性:旨在明确处理后标本的最长待检时间。采集健康人或患者的样品至少5份,对完成染色-裂解-固定 后的标本即刻上机检测结果作为基线水平。按实验室获得检测结果的最长可接受时间为期限,设置不同 的时间点对固定后标本进行上机检测。结果判定同上一条。亦可对试剂说明书声明的稳 定性条件进行验证。线性范围适用于淋巴细胞亚群绝对细胞计数。根据试剂说明书声明的线性范围,取一份淋巴细胞计数或亚群 计数接近线性范围上限的临床样品,采用样品稀释液按照比例制备 5~9 个不同浓度的标本,浓度范围应覆盖临床医学决定水平;通过染色-裂解-固定后,上机测定, 每个标本重复测定 4 次,取均值。分析实际测定的亚群细胞数量均值与理论值之间的相关性,相关系数 r 应≥0.975。可比性抗体试剂批次变更前后的可比性验证:宜使用至少3份健康人的新鲜全血样品和2份不同浓度质控品,采用新批号抗体试剂和当前批号抗体 试剂进行荧光染色、上机检测,以当前批号试剂检测结果为参考,计算相对偏差或绝对偏差。检测结果 应符合实验室制定的验证要求。验证要求的制定应考虑不同水平的淋巴细胞亚群计数设定不同程度的偏 差值,淋巴细胞亚群计数过低者,宜以绝对偏差进行验证。不同检测系统间的可比性验证:宜使用至少 5 份新鲜全血样品(样品的淋巴细胞亚群细胞计数应覆盖低中高水平)和 2 份不同浓度 水平的全血质控品,完成染色-裂解-固定后,分别采用待评价检测系统和比对检测系统进行检测。比对 检测系统应为仪器性能良好、规范开展室内质量控制、室间质量评价成绩合格的淋巴细胞亚群常规检测 系统,以比对检测系统的测定结果为参考,计算相对偏差或绝对偏差。检测结果应符合实验室制定的验 证要求。验证要求的制定应考虑不同水平的淋巴细胞亚群计数设定不同程度的偏差值,淋巴细胞亚群计 数过低者,宜以绝对偏差进行验证。不同检测人员间的可比性验证:宜使用至少5份新鲜全血样品和2份不同浓度水平的全血质控品,分别由实验室内淋巴细胞亚群检测 培训合格的不同检测人员完成染色-裂解-固定、上机检测和数据分析,计算不同检测人员间检测结果的 相对偏差或绝对偏差。验证结果应符合实验室制定的验证要求。准确度可使用室间质评回报结果验证淋巴细胞亚群项目的准确度。TBNK 室内质控01质控品选择应首选商品化全血质控品进行室内质控,并至少包括两个浓度水平,CD4+T细胞的绝对细胞计数应包括低值浓度水平质控。02检测时间检测当日至少做一次质控,质控品应和患者样品同时进行免疫荧光染色,并在患者标本检测前进行上机测定和数据分析。检测完成后做好相应质控记录。03靶值建立实验室应建立每一批次质控品的靶值和可接受范围,不可直接引用说明书提供的质控范围。更换新批号质控品前,可通过每日检测4次质控品(不同时间点),连续5天收集20次数据,计算均值。均值作为新批次靶值,结合既往累计CV值推算SD。04失控判断标准应至少选择13S和22S作为失控判断标准,应有相应的失控纠正措施。以CD3+T细胞质控曲线举例随着TBNK项目开展的普及,结果的准确与患者免疫状态的评估和治疗方案的制订是否能够正常进行的前提与保障。因此TBNK室内质控尤为重要,可以确保TBNK检测结果的准确性和可靠性。如需进一步了解性能验证的内容以及质控品的介绍,可与贝克曼库尔特生命科学的技术支持和销售联系。 ● 参考文献: 1.中华医学会健康管理学分会,TBNK淋巴细胞检测在健康管理中的应用专家共识.中华健康管理学杂志,2023,17(02):85-952.WS/T360—2024,流式细胞术检测外周血淋巴细胞亚群指南3.WS/T 406-2012 临床血液学检验常规项目分析质量要求4. YY/T0588-2017 流式细胞仪
操作维护
2024.07.09
自动化助力蛋白质组学样本高质量制备
蛋白质组学研究是一项涵盖蛋白质表达、蛋白间相互作用、蛋白功能、蛋白结构和翻译后修饰的综合科学研究。蛋白质组学的研究具有重大的潜力,可以解开疾病复杂机制,寻找疾病早期诊断的分子标志物和解决方案,促进疾病研究发展。蛋白质组学的研究在各个领域都具有广泛的应用,如临床与健康学研究、食品技术、生物标志物的发现,以及药物靶标的鉴定。蛋白质组学实验流程复杂,有较高的操作和实验技能的要求。完整的实验步骤一般包括实验设计、样品前处理、LC-MS/MS分析、数据库检索、生物信息学分析等多重步骤。其中蛋白质组样品前处理是确保数据重现性、一致性的关键,对于稳定的下游分析至关重要。质谱检测多肽质荷比,盐类以及其他离子化的物质都可能对结果产生干扰。同时,手工实验需要投入大量人工操作时间,压缩了分析时间。此外,劳动密集型步骤导致人为误差比率增大,不同个人和实验室间的准确性和重现性差异大,特别是在高通量条件下。自动化样本制备的方法可减少手动操作时间,提高蛋白质覆盖率,帮助获得高重现、高质量的结果。贝克曼库尔特生命科学利用功能强大的自动化设备和丰富的自动化经验,开发了一套标准的自动化实验流程包括变性、还原、烷基化、淬灭、稀释、消化和脱盐,应用于LC-MS/MS分析全血,血浆,干血斑等样品中产生的多种血浆蛋白,为不同类型样本用于疾病诊断、生物标志物发现和常规临床分析提供可靠的实验数据依据。图1:蛋白质组学样本自动化处理实验流程Biomek i7 Hybrid自动化样品前处理系统成功的蛋白质组学分析实验始于精心设计的样品前处理方法和自动化解决方案,对于自动化样品前处理,Biomek i7 Hybrid自动化样品前处理系统为双机械臂系统,每个机械臂同时配备移液系统和抓板手,2个抓板手可同时运行。拥有45个有效标准板位的台面容量,台面通过简单配备温控和震荡功能模块以及整合正压固相萃取模块,即可完成包括蛋白变性、还原、烷基化、蛋白酶解、脱盐和肽段纯化所有前处理流程。图2:系统示意图使用该系统实现自动化蛋白质样品前处理,可大大减少操作差异、样品处理错误,并节省人力。预先优化验证的方案支持无人值守,每个人只需通过简单的培训即可实现自动化操作。下图为系统使用集成的正压模块进行自动化固相萃取,完成脱盐流程。图3:正压过滤模块(PPA)应用案例本实验开发了一种更高效、稳定、适用性强的标准蛋白质组样本制备流程,将样品分为中等通量(20样本/天)和高通量(57个样品/天)通过自动化的样本处理流程产生高质量的肽段,然后利用液相色谱和质谱联用平台(LC-MS/MS)对肽段进行分析,获得3日内、日间不同样本的CV和不同数量的肽段。图4:Biomek 自动化标准实验流程和桌面布局(附带正压模块PPA照片)结果展示图5:总蛋白组学工作流CV=工作站CV + LC-MS/MS CV图6:总蛋白组学工作流CV自动化样品制备的日内重现性CV:4%-20%,结果表明自动化流程对高通量样本处理的稳定性满足需求。图7:A)中通量样品分析和肽段鉴定 B)高通量样本分析和肽段鉴定每个样本做5次重复,一共重复3日,并且利用LC-MS/MS平台对中通量数据和高通量数据进行了分析,对于中通量样本的研究发现全血样本可鉴定出最大数量为365的肽段,对于高通量样本的研究发现干血斑可鉴定出最大数量为324的肽段。总而言之:自动化蛋白质组样本前处理系统对于不同类型的血液样本(血浆,全血,血斑等),都可以获得重现性高,质量高的肽段,用于下游的定量和分析。(备注:该自动化平台不仅可用于蛋白质组学样本研究,而且可进一步扩展适用于代谢组学和脂质体的研究。)优势总结综上,小贝为您总结了自动化蛋白质组样本前处理的优势:参考文献1. Wright, I. & Van Eyk, J. E. A Roadmap to Successful Clinical Proteomics. Clinical Chemistry 63,245–247 (2017).2. Malsagova, K. et al. Dried Blood Spot in Laboratory: Directions and Prospects. Diagnostics(Basel, Switzerland) 10, (2020). 3. Fu Q, Kowalski MP, Mastali M, et al. Highly Reproducible Automated Proteomics Sample Preparation Workflow for Quantitative Mass Spectrometry. Journal of Proteome Research. 2018;17(1):420-428.doi:10.1021/acs.jproteome.7b00623.4. Mc Ardle A, Binek A, Moradian A, Chazarin Orgel B, Rivas A. et al. Standardized Workflow for Precise Mid- and High-Throughput Proteomics of Blood Biofluids. Clinical Chemistry. 2021 Oct 23: hvab202. doi: 10.1093/clinchem/hvab202. Epub ahead of print.5. Casey W Coutelin Johnson et al. Fully Automated Peptide Desalting for Liquid Chromatography–Tandem Mass Spectrometry Analysis Using Beckman Coulter Biomek i7 Hybrid Workstation.Beckman Coulter Life Sciences.
应用实例
2024.07.09
如何科学延长超速离心机的使用寿命?
随着机器使用年限的增加,仪器各个系统存在老化的迹象从而仪器故障率会增加,保养趋之重要。何为保养?保养即对离心机的各个系统进行检查及维护,能够及时发现仪器存在的潜在问题(如橡胶件老化等),定期更换易损耗材,缓解恶劣环境(潮湿、灰尘)对离心机造成影响,保养,可以避免因这些问题导致离心事故情况的发生。每年均必须保养一次,仪器运行的准确性、稳定性和使用的安全性均得到保障,从而降低离心机损坏风险和维护成本,保证仪器能处于良好的工作状态。保养可给您带来哪些帮助 ?提高操作人员的操作技巧保证仪器的稳定性和准确度延长真空系统、驱动系统的使用寿命延长马达的使用寿命延长仪器的使用寿命降低扩散泵出故障的风险降低仪器的维护成本仪器保养清洁、除尘检查调整机器水平离心机常见故障检查门锁检查保养,检查更换密封圈重要部件检查保养( 真空管道、转头识别传感器,测速环等)检查更换真空泵油和马达驱动油检查保养离心机各个系统(供电情况、真空系统、制冷系统、马达驱动系统等)离心机运行安全性检查转头保养检查清洁外观和测速环转头螺纹涂抹润滑油检查密封圈、密封圈涂抹真空脂检查转头、运行次数和使用寿命耗材检查检查离心瓶的使用状态检查离心机适配器的使用状态检查离心机附带工具的状态淘汰破损耗材离心机服务产品介绍1.正常使用范围内的零件,不包含耗材 2.保内人为造成零部件的损坏,按原价的50%收费 3.不包括节假日或非工作时间的人工费 4.每年一次保养(含标准保养包) 5.每年一次的转子检查,不含维修(如果维修则另外收费,客户须提供转子进口的报关文件) 6.电脑系统优化整理,不包括操作系统升级 7.服务工程师一次现场操作培训 8.工作日(周一至周五,早9点-晚5点) 9.工作日(周一至周五,早9点-晚5点); 非工作时间: 在线记录,优先处理 10.应用工程师一次现场应用培训 11.合同期内一次免费移机服务(含拆机,安装和调试),不含物流及相关费用* 以上产品仅用于工业及科研,不用于临床诊断,禁忌内容或注意事项详见说明书。* 未经授权,不得对原有的文字图片等内容进行变动、重新编排或者增加新的内容,贝克曼库尔特保留在不告知前提下随时更新版本的权利。* 商标中Life Sciences为整体商标的一部分,意为 “生命科学” 。
操作维护
2024.05.31
【超离应用】快速密度梯度形成技术,优化病毒载体纯化流程!
01技术背景随着现代生物医学研究的不断深入,病毒载体作为一种强大的工具,在基因治疗和基因编辑等领域发挥着至关重要的作用。然而,病毒载体的纯化过程往往耗时且复杂,这在一定程度上限制了相关研究的进展。今天,我们就来探讨一种全新的方法——利用VTi 90垂直转子与CsCl(氯化铯)密度梯度离心技术,来加速病毒载体的纯化过程,提高实验效率。02方法介绍研究团队通过使用VTi 90垂直转子和Optima XPN超速离心机,结合CsCl密度梯度离心技术,对病毒载体纯化过程进行了优化。通过多段离心,调整离心速度和离心时间,实现了在更短时间内达到密度梯度平衡的目标。03实验过程在实验中,研究团队首先将病毒载体样品与CsCl溶液混合,然后将其加入Quick-Seal热封管中。再使用VTi 90转子进行离心,通过调整离心速度和离心时间,使样品在离心管内形成稳定的密度梯度。离心结束后,通过分馏的方式收集不同密度的样品组分,并使用折射仪测量各组分并绘制密度梯度曲线。通过比较不同实验步骤的密度梯度曲线,找到与旧步骤密度梯度曲线相同的实验条件,确保了样品条带位于相同位置。离心结果示意图:04实验结果基于 Optima XPN超速离心机对于分段离心步骤设置的支持(在一次运行中运行多个转速步骤),研究团队最终找到了一种能够在80分钟(50+30分钟)内达到密度梯度平衡的优化方案,较之前16小时的旧步骤提升了近12倍效率。以更高的速度开始分离可以帮助更快地形成密度梯度。将运行速度降低足够长的时间可以:与现有的(较慢的)步骤获得相同的效果,将目标条带保留在完全相同的位置。平坦化密度梯度曲线,可提供更高的条带分辨率。05结语加速密度梯度形成、优化病毒载体纯化效率是一项具有重要意义的研究工作,不仅为病毒载体纯化领域带来了新的突破,也为广大科研工作者提供了更高效、更便捷的实验方法,从而降低了实验成本和时间成本,为相关领域的研究提供了有力支持!如果您对以上方案感兴趣,不妨看看相关离心产品,以下组合搭配即助您轻松实现病毒载体纯化流程:Optima X系列智能型超速离心机Optima XPN系列配备益于初学者操作的 eXpert 智能软件程序,同时为密度梯度离心等方法提供强大支持。产品还具有增强型数据管理功能,完美支持客户 GMP 流程。主要型号:Optima XPN-100 / 90 / 80基础型号:Optima XE-100 / 90最大转速(rpm):100,000 / 90,000 / 80,000最大相对离心力(xg):802,000 / 694,000 / 548,300Vti 90垂直转子Vti 90垂直转子,最大相对离心力可达到645,000xg,最大转速下K因子低至6。分离沉降系数约为60s的空壳AAV颗粒,仅需80min,为分离病毒颗粒的理想选择。最大RPM:90 ,000最大RCF:645,000 xgK因子:6离心管数量/体积/大小/尺寸: ▪ 8 x 5.1mL ▪ ½ x 2 in ▪ 13 x 51 mm转头容量:40.8mL更多产品信息请咨询:400-821-8935或点击进入:小贝学习中心—产品指南
应用实例
2024.05.30
超全! 宿主细胞蛋白残留检测的法规要求和检测方法宝典来了!
宿主细胞蛋白(HCP)的法规要求对于确保生物制药产品的质量和安全性至关重要。经测试,残留的HCP可能引起不良反应,如免疫反应,也需要关注到的是残留的HCP可能影响药物的活性,导致药物效果降低,影响治疗效果。这些负面影响会直接导致药物的安全性问题,甚至可能对患者的健康产生威胁。例如,某些研究表明,ECP(大肠杆菌多肽)的存在与抗ECP抗体和抗rhGH抗体的产生相关,可能导致免疫反应等。HCP残留含量也被认为是生物制品的关键质量属性(CQA),是工艺稳健性监测的重要评价指标,也是产品的重要质控指标。对于HCP的法规要求是多层次、多方面的,旨在确保生物制药产品的安全性、有效性和质量。许多国家和地区的药品监管机构都要求生物药物在上市前必须进行HCP残留的检测。这是为了确保药物的安全性和有效性,满足法规要求。制药企业应严格遵守相关法规要求,采用合适的检测方法和控制策略,确保HCP残留量在可接受范围内。1.国际法规要求:ICH Q6B指南:国际人用药品注册技术协调会(ICH)的Q6B指南指出,需要根据ICH准则采用敏感且经过验证的有效方法来监控残留的HCP,其残留量通常要求小于100ppm。美国药典(USP):USP章节规定,用一种灵敏度较高的方法检测药品中的HCP,其含量应该低于检测限(通常小于100ppm,即1mg总蛋白中HCP含量应小于100ng,也即欧洲药典(EP):EP 2.6.34中规定,在生物制品中,HCP的含量应当小于0.1%。2.国家/地区药典要求:中国药典(2020版):针对CHO细胞,HCP残留需要针对E.coli,HCP残留需要其他国家:不同国家和地区的药典可能有各自的HCP残留标准,但都旨在确保生物制药产品的安全性和质量。而在实验室中常规的宿主细胞蛋白残留检测方法如下:1酶联免疫吸附试验(ELISA)原理:利用特异性抗体与宿主蛋白结合,通过测定抗原-抗体反应来定量宿主蛋白的残留水平。优点:灵敏度高,可用于定量检测。缺点:需要有针对特定HCPs的抗体,可能产生假阳性或假阴性的结果。自动化:可以使用自动化工作站,如Biomek i7,来提高准确性和检测通量。2二维电泳-质谱联用法(2D-PAGE-MS)原理:基于蛋白质分子量和等电点差异进行分离,通过质谱分析进行蛋白质鉴定。优点:可检测更广泛的HCPs,提供全面的蛋白质谱。缺点:操作复杂,需要较高的技术水平。3多肽映射法原理:通过蛋白质酶切、高效液相色谱、质谱等步骤,获得蛋白质的多肽图谱,进行结构鉴定和定量分析。优点:准确性高,适用于复杂样品的分析。缺点:操作步骤复杂,需要较高的技术水平和专业设备。4电泳法包括CIE(毛细管电泳)、SDS-PAGE(十二烷基硫酸钠聚丙烯酰胺凝胶电泳)等。优点:反应时间短、灵敏性高(如CIE)。SDS-PAGE简便、快速、重复性好。缺点:分辨率低(如CIE、SDS-PAGE)、不能精确定量(如SDS-PAGE)。5质谱法原理:直接检测蛋白质的质量和结构,通过比对目标蛋白和宿主蛋白的质谱图谱进行定量分析。优点:高灵敏度、高分辨率,可同时检测多个宿主蛋白。缺点:需要复杂的样品准备和数据分析过程。6生物活性测定法原理:通过测定宿主蛋白对生物活性的影响来验证残留。优点:提供宿主蛋白残留对药物活性的直接影响信息。缺点:可能在特定情况下不够敏感或特异性。在选择宿主细胞蛋白残留检测方法时,需要考虑多个因素,包括所需的灵敏度和准确性、样品的复杂性、以及可用的设备和技术水平。通常,结合多种方法可以确保最终药物产品的质量和安全性。今天小贝带来了基于ELISA的自动化检测宿主细胞蛋白残留标准化流程——标准化无人值守图1. 自动化HCP检测流程展示更高线性的标曲——高精度移液体现自动化人工图2. 使用CygnusTM CHO HCP ELISA 试剂盒对于自动化再现性的验证。手工和自动化的标曲比较结果如图二A和B所示,对比R2的数值自动化动化结果更好。稳定的结果保证——高重现性使用Biomek i7自动化工作站完成对不同时间宿主细胞培养基和细胞裂解液的蛋白定量检测。贝克曼库尔特生命科学提供专业的软件硬件支持,以及客户应用开发来满足大家对于生命科学自动化的需求。关于贝克曼库尔特生命科学自动化整合部门介绍:1、贝克曼自动化整合部门位于美国Indianapolis,该部门位于Beckman质量管理系统下,并经过ISO9001认证,部门配备整合实验室,完成整合设备的研发。2、整合部门人员包含机械、电子、软件、系统工程师,和工程师支持、项目管理人员。3、人员配备齐全,售前售后响应快速。4、如有特殊功能开发,Beckman团队可协助客户在国内进行软硬件开发和测试。*以上内容涉及设备仅适用于科研和工业,不用于临床诊断。
应用实例
2024.05.30
把握方向盘,开好行车道的脂质体药物
年一月份恒瑞医药自主研发的盐酸伊立替康脂质体注射液(商标名:越优力)获批上市,公开资料显示,这是恒瑞医药在现有盐酸伊立替康注射液及其冻干粉针剂的基础上,通过改变剂型开发出的一种可靶向分布于瘤体的新制剂。脂质体制剂的设计可保护伊立替康不会被早期转化为活性代谢物SN-38,有助于伊立替康在体循环中保持更长时间,增加药物在肿瘤内的沉积和接触,增强对肿瘤生长的抑制作用。正是由于脂质体能够将毒副作用大、在血液中稳定性差、降解快的药物包裹,并将药物浓集于病灶部位达到缓释或靶向给药的目的,正作为药物载体被应用于小分子药物、蛋白质药物、核酸药物和显像剂等。目前,全球共有14个脂质体产品获批上市,分别是:脂质体最早由英国学者于1965年发现,是脂质自组装形成的双层(单层)和/或同心多个双层(多层)封闭中心水腔的药物囊泡。脂质体的结构与细胞膜极其类似,使其具有高度的生物相容性和生物可降解性,将药物包裹,可以提高药物的稳定性,降低药物的毒性,提高给药剂量。同时,脂质体的双亲性磷脂形成的双分子层表面,可以通过物理或者化学手段,与配体或者其他功能基团进行结构修饰使其具有组织靶向性。另外,通过改变双分子层表面的电荷,可用于DNA和RNA药物的包载和递送。脂质体的结构(来源:医学百科)脂质体药物根据结构可将其分类为单室、多囊与多层。单室脂质体是目前最常见的一种结构,只具有一个可以载药的空腔。如盐酸阿霉素脂质体(Doxil),由于脂质体外壳的存在,盐酸阿霉素在体内的稳定性更高,药物浓度下降较慢,从而延长了其药效。此外,脂质体外壳还可以减少盐酸阿霉素对心脏和造血系统的毒性。多囊脂质体与多层脂质体可以分别比喻为“石榴”和“洋葱”,即多囊脂质体具有多个蜂巢状排列的空腔,而多层脂质体具有多个层累堆叠的空腔,均具有出色的缓释效果。如最早由美国Pacira公司研制的布比卡因脂质体注射液,采用多囊脂质体药物递送系统,可将镇痛效果延长至数天。由于脂质体药物的组成、结构、尺寸、表面性质、药物包封率、载药量、药物存在形式等可显著影响其稳定性、药物释放以及脂质体-生物膜之间的相互作用,进而影响药物的安全性和有效性。因此,需对脂质体药物的质量进行深入研究和有效控制。丹纳赫生命科学拥有一些列脂质体药物的表征方案,可对脂质体进行多方位的分析。对于脂质体药物的形态、粒径及其分布,常采用电镜、激光散射法或激光扫描法测定。丹纳赫生命科学旗下徕卡显微系统的EM GP2 自动投入冷冻仪,可对脂质体样本进行冷冻透射电镜前的载网冷冻处理,采用冷冻透射电镜对脂质体进行观察可以减少电子束对样品的损伤,降低样品的形变,获得更真实的样品形貌。EM GP2 的红外线传感器能够精确控制滤纸吸附,使样品分布均匀,结合单面平行吸附,能够在不破坏碳膜的情况下,获得更大面积的载网可用范围。徕卡显微系统的EM GP2全自动快速投入冷冻仪对脂质体药物进行载网冷冻处理(来源:电子显微学报2012)包封率是脂质体药物特有的质量属性,它是指被包裹物质(如某药物)在脂质体悬液中占药物总量的百分量。丹纳赫生命科学旗下贝克曼库尔特生命科学的分析型超速离心机AUC可通过离心沉降法进行脂质体药物包封率的检测。如对阿霉素脂质体的检测,AUC通过对阿霉素脂质体、游离阿霉素以及空脂质体的不同紫外吸收波长进行包封率的测定和计算。AUC作为一种遵循第一性原理、使用样品原始溶液的方法,通过检测脂质体药物沉降系数分布,还可得到样品的纯度信息。贝克曼库尔特生命科学的分析型超速离心机AUC对阿霉素脂质体的包封率检测正是由于脂质体药物特有的质量属性,它在注入血液后,会存在脂质体包封的药物、非包封的药物和空脂质体三种形式。根据2015年FDA指南草案,要批准具有持续释放功能的新脂质体制剂,必须考虑三个标准:脂质体载体本身的清除率,被包封的药物从脂质体载体中释放的速率以及自由药物释放后的清除和代谢。因此,检测脂质体相关药物和游离(或非脂质体)药物的血浆浓度,对于脂质体制剂的药代动力学研究和安全性评价是必要的。而且,需要一种合适且可靠的样品制备方法,将未包封药物与脂质体包封药物分开。 SPE法是常见的前处理方法,当样品加载到SPE柱中时,未封装的药物会保留在SPE柱上,脂质体成分会通过并收集在洗脱液中。然后用有机溶剂洗脱柱,以收集未包封的药物,洗脱液中的脂质体需要进一步处理以破坏脂质体并释放出药物用于后续分析。SPE法进行脂质体药物前处理的典型步骤丹纳赫生命科学旗下艾杰尔-飞诺美拥有多种不同类型的SPE柱及96孔微孔板,可用于脂质体药物的制剂以及生物学分析前处理。其中SPE微孔板最低只需要25µL的洗脱体积,比传统96孔板节省时间,并且能够减少热敏感型化合物回收率损失。艾杰尔-飞诺美的SPE产品由于理化结构带来的优越生物相容性和可编辑性带来的靶向给药潜力,脂质体递送受到广泛关注,并且在临床上有进一步的应用。但是其工艺流程、保存、安全性等方面还具有一定的挑战,企业需要不断创新,加强产品研发和质量控制,才能在市场中取得竞争优势。
参数原理
2024.05.28
请查收!您的全自动高通量蛋白纯化方案已发布!
在绿色生物制造和合成生物学等研究领域中,高质量的蛋白分离和纯化是研究目的蛋白结构和功能的重要步骤。传统的分离纯化方法通量低、耗时长、均一性差,全自动高通量蛋白纯化系统在生命科学研究和生物制药领域已开始广泛运用,从样本前处理工序,到不同类型的蛋白纯化流程,可实现多管线自动化平行实验,具有稳定的工艺流程,可极大提高实验效率,节约时间和人力成本;同时还可以进行数据交互,实现样本溯源和实验数据管理。今天小贝给大家整理了几种常见好用的蛋白纯化方案助力您的科学研究。磁珠捕获特异性标签蛋白,因其纯化步骤精简成熟被广泛应用,图1是磁珠纯化流程示意图。小贝为您量身定制蛋白纯化全流程自动化方案:使用Biomek i系列液体工作站,整合核酸/蛋白提取仪,实现高效高通量自动化蛋白纯化,极大节省实验时间和科研精力。图1 磁珠纯化流程图2 Biomek i系列液体处理工作站展示图Biomek i系列液体工作站配置96通道和灵活8通道加样器,适配各种商品化试剂盒和用户自配试剂,轻松实现试剂分装和高通量样本纯化。同时工作站支持多设备整合,可进行后期无限升级,添加离心机、酶标仪等设备助力全流程自动化实验。图3 磁珠纯化方法截图及纯化结果高通量磁珠法蛋白纯化模块可以通过结合核酸/蛋白提取仪实现极简快速蛋白纯化,也可以通过自动化液体工作站结合磁力架完成。使用该功能时仅需要通过软件的简易命令行即可完成,如图3所示,工作站机械抓手会根据纯化流程将Binding Buffer、Beads、Washing Buffer等试剂自动搬运到指定位置,使用磁套进行磁珠转运,单次可以完成96个样本纯化,浓度稳定在0.5-0.8mg/ml,96孔板纯化时间约60min,节省枪头成本,省时省力。图4 亲和层析柱蛋白纯化法实验流程RoboColumn是一种小型色谱柱,用于抗体、蛋白质、多肽等的全自动平行色谱分离,其纯化流程如图4所示。高通量的RoboColumn ALP 与Biomek i系列液体工作站相结合,配置Span8固定针,可实现多通道自动化的平行层析实验流程,显著缩短工艺开发时间;同时还可以进行数据追踪,实现样本溯源,减少重复工作。图5 RoboColumn ALP模块结构及Span8固定针示意图W1:废液槽;B1:收集板载架;C1:柱载架Biomek液体工作站可以实现台面整合RoboColumn ALP模块,通过软件流程式编辑方法,控制ALP板位自动位移,实现液体收集,轻松完成蛋白纯化,图6展示了软件控制ALP板位收集液体的方法以及RoboColumn纯化结果,实验中1.56mg蛋白上样,经0.1M Gly-HCl(pH2.7)洗脱回收得到蛋白含量1.31mg,纯化得率达到84%,8通道操作时间约为80min。图6 调用RoboColumn方法界面及纯化结果展示图7 PhyTip法自动化纯化关键流程PhyTip为枪头式分散固相亲和色谱柱,采用枪头式装置,纯化树脂被填充于枪头尖端,由自动化液体处理工作站加载PhyTip,可以实现单通道到96通道灵活样品数纯化,其纯化流程如图7所示,可对微克级到毫克级的蛋白进行纯化。图8 PhyTip实物图、PhyTip纯化方法及结果展示图Biomek液体工作站与枪头式纯化色谱柱相结合,利用工作站加载PhyTip让纯化流程变得如移液流程一样简单!如图8所示,加样器加载PhyTip,分别在平衡液、蛋白样品、洗杂液和洗脱液中混匀即可完成高通量蛋白纯化,单次可处理96个样品,收集10mL菌液使用PhyTip(40uL填料),纯化后经BCA蛋白定量测定蛋白含量稳定在400ug左右,优于手工对照实验340ug的结果,96孔板操作时间约为90min。小 结
应用实例
2024.05.27
细胞计数仪知识分享系列 I 鉴定识别篇
上一篇《细胞计数仪知识分享系列 I 性能检测篇》中,我们发现全自动细胞计数仪在检测细胞样品的重复性和梯度稀释的结果准确性上,都比半自动插板式细胞计数仪更有优势。那么大家可能会问:导致这样的性能差异原因是什么?目前市场上许多公司都自诩所卖的细胞计数仪是全自动的,那我们又如何区分哪个是全自动,哪个是半自动?本文我们将给大家介绍下全自动和半自动细胞计数仪性能差异的原因以及如何快速地鉴别全/半自动细胞计数仪PART 01全自动和半自动细胞计数仪性能差异的原因首先,我们对台盼蓝染色的图像法细胞计数仪的检测过程做下回顾,下面6个步骤是细胞计数和活率分析的基本流程。传统显微镜下手工细胞计数(如下所示),前面5步操作都要操作人员来手动完成。因为人为操作带来的误差不可避免,导致结果差异有时会很大,甚至超出通常可以接受的±10%偏差范围。并且随着样品数越多,操作人员容易造成眼疲劳,无法继续进行有效并准确地计数。手工显微镜法细胞计数的照片和计算方法因此,插板式半自动细胞计数仪应运而生,它省去了操作人员肉眼观察和统计死活细胞数的步骤,但剩下几个步骤还需要手动完成,包括吸液加样、台盼蓝染色和上样分析(有时还要手动对焦),测试结束后需更换新的细胞计数板做下一批样品。半自动细胞计数仪的三种计数板手动加样照片相比全自动细胞计数仪,半自动细胞计数仪存在以下问题导致计数结果重复性和准确性要差:细胞样品和台盼蓝的体积需要移液枪手动定量,而且混匀也是手动来完成,因此不可避免地产生人为操作误差。从摇瓶培养的几十毫升或生物反应器几十到上百升的细胞样品中,吸取20-30uL体积的样品进行检测,由于取样量少,容易引起取样代表性差,结果不准确的问题。仪器一般只拍1-3张照片,分析统计的细胞数量相对少,结果的代表性相对较差。同时,染色后的细胞样品通过移液枪加到计数板上,有时会操作不当产生气泡,特别是细胞培养液中含有较多易产生气泡的蛋白,这种问题更容易发生。另外,废弃的细胞计数板还会产生二次固体污染,这些问题目前都没有好的解决方法。那有没可能细胞的混悬和染色,以及细胞的计数和分析过程全部实现自动化,同时不用手动更换新的细胞计数板而自动做下一个样品呢?答案是使用全自动细胞计数分析仪。PART 02如何快速鉴别全自动和半自动细胞计数仪?结合细胞计数和活率分析的检测过程,除了要放入待检测的样品外,全自动细胞计数仪可以让仪器自动完成样品的混悬、台盼蓝染色、细胞拍照和识别、测试结果的分析统计和显示。相比半自动细胞计数仪,全自动细胞计数仪有以下一些特点可供大家快速鉴别。1. 自动混悬和台盼蓝染色全自动细胞计数仪的一个显著特点是能够自动完成细胞的吹打混悬和台盼蓝染色。要拥有这个特点,仪器必须具备下面两个功能。首先,仪器内部要有步进马达,准确控制细胞样品和台盼蓝等体积混合。然后,仪器还要可以自动混匀染色,能将细胞样品和台盼蓝进行有效地染色处理。而这两步操作,对于半自动细胞计数仪而言,还只能通过手动操作来完成。2.自动管路清洗全自动细胞计数仪内部有一个流通池,可用于流过的细胞拍照成像,所以就不需要细胞计数板这个耗材。当样品检测结束后,仪器需要自动对流通池进行清洗,并在清洗结束后将管路内液体切换到对细胞友好的磷酸缓冲液,等待下一个样品的检测。所以,除了对细胞拍照的光路系统和用于数据控制的电子系统外,相比半自动细胞计数仪,全自动细胞计数仪还有一个清洗管路的液路系统,并通过八通阀的切换完成细胞的染色和管路清洗。因此,一般大家看到的全自动细胞计数仪体积会相对大一些。3. 高通量和不间断检测全自动细胞计数仪的另一个特点是高通量和不间断检测。待测样品可以先放到转盘或96孔板上,根据软件中设置好的分析条件,仪器会自动按要求分别对这些细胞样品完成计数和活率分析。Vi-CELL BLU细胞计数仪的两种上样模块以贝克曼库尔特生命科学Vi-CELL BLU全自动细胞计数仪为例,使用转盘一次可以放21个样品,而使用孔板最多可以放96个样品进行分析测试。若使用24位转盘,在检测过程中还可以实现不间断上样测试,即样品测试过程中,还可以放入新的待测样品。所以,在操作便捷性上,全自动细胞计数仪也是优于半自动细胞计数仪。总之,全自动细胞计数仪在细胞样品混悬和染色方面避免了人为操作带来的误差,同时仪器能自动清洁管路和过夜清洗,而且可以高通量上样和不间断测试。因此,不管是细胞计数的重复性和准确性,还是仪器操作的便捷性上,全自动细胞计数仪都比半自动插板式细胞计数仪更有优势。希望大家可以通过此文介绍的以上这些特点,在面对琳琅满目的细胞计数仪时,能够快速有效地鉴别出细胞计数仪是“真”全自动还是“假”全自动。除了仪器测试结果的重复性和准确性,对于生物制药的质量控制和生产部门,仪器软件的法规符合度也是一个很重要的点。所以,下一期的细胞计数仪知识分享,我们将为您提供法规符合度方面的内容介绍。
参数原理
2024.05.27
Echo声波移液合成生物学的DBTL角色
✦•✦声学微滴喷射(AED)技术使用聚焦的声能实现高精度和准确度转移纳升级液滴。Echo这种非接触式、无需吸头、低体积加液技术将交叉污染的可能性降至最低,同时极大程度降低试剂和耗材的成本。迄今为止,Echo除了广泛应用于高通量化合物筛选之外,还有另一个强大的技术应用方向——快速发展的合成生物学领域,如DNA合成和连接,Echo声波移液使得PCR以及Golden Gate 和 Gibson两种一步法DNA连接方法成功地缩小至纳升级规模,极大地提高DNA合成和连接效率并有效将试剂成本降低20至100倍。大部分DNA组装的费用成本是酶,包括DNA聚合酶,因此,将反应体积从微升缩小到纳升级,同时保持高装配效率,将使合成生物学家更容易完成DNA合成和组装。这也使Echo声波移液成为DNA生物铸造厂时代的合成生物学中的一项工具性技术。比如在常规终点法PCR实验中,Echo可将PCR反应体系降低至250nL,成功扩增出1.3kb的片段。图1 通过 Echo进行PCR体系构建。Gibson DNA连接方法是合成生物学中使用最多的技术,它可以组装从DNA序列至小基因组重叠DNA片段大小,优点是它与序列无关并生成无痕DNA连接产物。Golden Gate DNA连接方法利用TypeIIS限制性内切酶和连接酶组合来组装DNA片段。正如我们先前所介绍的一样,使用Echo声波移液,能够实现这两种一步式DNA连接反应的降本增效,可在250 nL、500nL和1000 nL反应体积下实现Gibson的正确组装,效率可与手工实验相媲美或优于20 μL反应,这使试剂成本降低20倍以上;Golden Gate可实现50 nL 、250 nL和500 nL规模反应体积的DNA(手工实验时通常为 15 μL反应)成功组装,效率同样高于手工实验对照,使试剂用量至少降低30倍。生物合成途径的阐明和重构以及调控回路和网络的工程设计,都需要蛋白质功能的知识。植物一直被用作生物活性和高价值天然产物的来源,但由于植物之中大型基因家族的普遍存在,使得将特定功能与单个蛋白质联系起来具有挑战性,同时也面临需要付出大量努力来优化表达和纯化方案进行蛋白质表征这一技术瓶颈。Biofoundry的独特优势能够加速“设计-构建-测试-学习”周期的能力,可加速优化并实现酶活性的快速筛选;无细胞蛋白质合成(CFPS)结合了DNA模板、能量源、氨基酸、核苷酸三磷酸 (NTP) 和过量辅因子,以及含有翻译机制的粗裂解物,是一种成熟的体外快速蛋白质生产工具,显著优势是能够直接进行功能分析,而无需耗时的细胞破碎和纯化方案,同时还适用于自动化和小型化,减少操作错误和CFPS反应中的可变性,促进主动学习引导的反应条件优化,并普遍增加实验的通量,最大限度地减少DBTL循环中的“构建”时间。SynTrack是一个基于web的工作流程驱动的bioCAM平台,用于管理和跟踪DNA制造过程。SynTrack导入boost指定的构建过程信息,其中包括操作人员(利用机器人平台)执行所有“构建”操作的分步说明。SynTrack可以为液体处理机器人(如Biomek FX和Echo平台)生成移液指令,自动将接收到的DNA片段重新排列到孔板中。通过Echo自动化平台构建2μL反应体积(手动为20μL)进行一步法Golden Gate DNA组装反应,随后构建2μL CFPS反应体系进行蛋白表达,通过荧光素酶(该标签可轻松去除)快速定量蛋白表达水平,随后无需蛋白纯化即可使用游离蛋白质合成反应产物进行多种功能表征。图2 Biofoundry辅助DNA组装和植物蛋白游离蛋白合成(CFPS)的工作流程。编码目的蛋白的0级DNA部分(模块)可以组装成用于CFPS或在植物中表达的功能表达质粒。使用Echo筛选蛋白质变体的文库,使用 HiBiTLgBiT荧光素酶发光实验定量确定最佳表达构型。使用Echo声波移液配合无细胞蛋白合成(CFPS)技术也可在96和384孔板中进行代谢工程检测,通过Wood-Ljungdahl通路耦合的反向β氧化(r-BOX)通路,实现如C4-C6酸和醇生化产物的负碳合成,具有降低全球CO2排放的巨大应用潜能。正是由于模式生物大肠杆菌无细胞转录-翻译(TXTL)在DNA定向体外蛋白质合成的应用范围越来越大,一些实验室也开发了全大肠杆菌TXTL工具箱,并通过Echo实现了流程自动化。另一个无细胞合成生物应用方向是非模式生物体外原型设计和快速表征代谢途径,加速体内生物合成途径测试,使例如梭状芽胞杆菌等非模式生物能够利用可再生资源(木质纤维素生物质或CO和H2合成气)生产更多高价值产品。使用DNA组装设计自动化软件J5进行结构设计和生成实验运行worklist,发送至Echo自动化平台以2 μL体积进行Golden Gate DNA组装,可同时进行多达6个部分(三个独特启动子和终止子序列的开放阅读框)的组装,效率高达90%;这一质粒系统将为非模式生物提供体外和体内生物合成途径的简单测试框架,从而缩短开发周期。非模式生物巨双歧杆菌的天然无细胞(NCF)转录翻译平台的快速建立也借助了Echo,并和贝叶斯模型参数推断方法相结合,可以在数小时内对基因表达工具进行严格的表征,并且这个平台还有望扩展到一系列其他重要的底盘微生物的合成生物学应用。图3 使用兼容的无细胞载体系统组装三基因构建体的Golden Gate。(a)Golden Gate组装工作流程的示意图,包括自动化组装,包括质粒的计算设计、Echo自动化液体处理操作指令、质粒组装和质粒确认。(b)含有构建的梭状芽孢杆菌表达载体的六个克隆中的质粒组装的PCR鉴定。图4 非模型微生物的无细胞原型设计。(A)在NCF中使用内源性能量再生和转录-翻译组分测试合成的基因表达质粒。(B)在B. megaterium NCF中使用MGapt(mRNA)适配体和GFP进行平行转录-翻译测定。(C)借助Echo液体处理工作站,用于快速筛选无细胞反应的半自动化工作流程。微生物系统中异源生产的特定高价值化学物质大多需要资源密集型分析过程(如HPLC和MS)进行定量,较低的分析通量使DBTL循环遇到了一定的瓶颈。而生物传感器通常与基因表达系统耦合,为此人们越来越关注开发荧光生物传感器用于合成生物学中,来检测小分子和物理信号。通过为Echo编写Python移液脚本,构建384或1536孔板的10μL或2μL荧光酶标检测体系,基于大肠杆菌双键还原酶(EcCurA)非特异性结合后荧光极大增强的特性,开发了一种荧光复合物直接蛋白质(DiPro)生物传感器,作为微生物异源姜黄素酶促合成的检测单元,且不需要任何额外的基因表达后步骤或特定的蛋白质成熟要求。同样,使用Echo进行小反应体系的荧光素酶化学发光体系构建,高通量筛选分析脯氨酰寡肽酶异源表达变异株,将金属响应开关整合到蛋白质中,也为精确调节蛋白质功能提供了新的机会。图5 Ni(II)依赖的开关随着合成生物学的发展,使得通过大肠杆菌或酿酒酵母等微生物用于筛选氢化烯烃的酶,成为克服石油精炼过程中烯烃加氢面临的催化剂中毒、传质限制、发热以及与氢气、储存和催化剂等相关的一个重要的解决方案。相比于LC/GC-MS复杂的工作流程和较长的分析时间,使用Echo声波移液和薄层色谱搭建的自动化96孔筛选平台极大地提高了检测速度,使并行多个样品检测即时可视化,读值结果更可靠,成为一种高效的筛选流程,用于确定与工程化GGR蛋白文库相关的酶活性和产物形成谱。使用Echo将环氧化反应产物“打印”涂覆在薄层二氧化硅上,根据环氧化程度进行色谱分离,并与发色团共价连接,从而可以检测具有独特产物分布或增强还原酶活性的酶变体。经过GC-MS验证,这种基于薄层色谱的筛选可以区分选定突变体酶活性的四倍差异。图6 靶向SaGGR(源自嗜酸热硫化叶菌的香叶基香叶基还原酶)中L377X(377位亮氨酸)的密码子饱和诱变文库高通量筛选方案图7 Echo声波喷射液滴的优化和时程分析中的应用。a,通过Echo转移到二氧化硅-TLC板上的考马斯染色剂。确定50 nL为同时进行48孔TLC分析的最佳体积。b, 30 μM WT SaGGR与2 mM法尼醇一起孵育的时程测定,每分钟用环氧化试剂淬灭,并在单独的泳道中点样。随着测定演化到其 48 分钟的终点,对应于H环氧化物衍生物的条带H0-, H2-和H4-FOH用Rf(1)、Rf(2)和 Rf(3)表示,并分别增加强度,而副产物带 Rf(s2)和Rf(S3)随时间保持相对恒定。c, 从b中描述的时间过程得出的气相色谱图描述了法呢醇(H0)、di-(H2)和四氢法尼醇(H4)Echo高通量DNA组装还被用于在酿酒酵母固氮基因组合文库中筛选功能性固氮酶异源表达基因,为固氮谷物开发并改变全球农业系统提供极大支撑。DNA组装和Echo自动化液体处理结合技术也入选了高校合成基因组暑期课程,这一培训课程旨在向研究人员传授合成生物学和合成基因组科学最新进展背后的理论和实践技能,通过软件研讨会、课程和该领域领先成员的研究讲座,与会者能够在了解相关原理和技术的同时,在基于实验室的实践课程中直接使用合成生物学平台开发的软件和载体进行验证。在课程具体实践中,Echo自动化DNA组装技术大大提高了用于设计β-胡萝卜素异源通路文库的表达检测的通量。同时,使用该平台进行的番茄红素代谢途径的自动化设计和构建成果也于2020年发表。图8 帝国理工学院暑期合成基因组培训课程。(a)实验室实践,(b)自动DNA组装编程,(c)合成基因组软件工具研讨会和(d)SCRaMbLE教程。通过以上案例我们可以发现,Echo声波移液在DBTL循环中起到承上启下的串联角色,既可接受“设计”流程中基于集成运算生成的脚本指令完成DNA组装,撑起“构建”阶段一众重要的应用方向;又可在“测试”过程中实现高通量自动化以及小体系精准检测,并传递数据为“学习”阶段提供支撑,因而是合成生物学和Biofoundry不可或缺的好帮手。✦•✦ ● 参考文献: 1、Kanigowska P, Shen Y, Zheng Y, Rosser S, Cai Y. Smart DNA Fabrication Using Sound Waves: Applying Acoustic Dispensing Technologies to Synthetic Biology. J Lab Autom. 2016 Feb;21(1):49-56. doi: 10.1177/2211068215593754. Epub 2015 Jul 10. PMID: 26163567; PMCID: PMC4814025.2、Dudley QM, Cai YM, Kallam K, Debreyne H, Carrasco Lopez JA, Patron NJ. Biofoundry-assisted expression and characterization of plant proteins. Synth Biol (Oxf). 2021 Sep 11;6(1):ysab029. doi: 10.1093/synbio/ysab029. PMID: 34693026; PMCID: PMC8529701.3、Cai YM, Carrasco Lopez JA, Patron NJ. Phytobricks: Manual and Automated Assembly of Constructs for Engineering Plants. Methods Mol Biol. 2020;2205:179-199. doi: 10.1007/978-1-0716-0908-8_11. PMID: 32809200.4、Vögeli B, Schulz L, Garg S, Tarasava K, Clomburg JM, Lee SH, Gonnot A, Moully EH, Kimmel BR, Tran L, Zeleznik H, Brown SD, Simpson SD, Mrksich M, Karim AS, Gonzalez R, Köpke M, Jewett MC. Cell-free prototyping enables implementation of optimized reverse β-oxidation pathways in heterotrophic and autotrophic bacteria. Nat Commun. 2022 Jun 1;13(1):3058. doi: 10.1038/s41467-022-30571-6. PMID: 35650184; PMCID: PMC9160091.5、Garenne D, Thompson S, Brisson A, Khakimzhan A, Noireaux V. The all-E. coliTXTL toolbox 3.0: new capabilities of a cell-free synthetic biology platform. Synth Biol (Oxf). 2021 Aug 4;6(1):ysab017. doi: 10.1093/synbio/ysab017. PMID: 34712841; PMCID: PMC8546610.6、Karim AS, Liew FE, Garg S, Vögeli B, Rasor BJ, Gonnot A, Pavan M, Juminaga A, Simpson SD, Köpke M, Jewett MC. Modular cell-free expression plasmids to accelerate biological design in cells. Synth Biol (Oxf). 2020 Oct 14;5(1):ysaa019. doi: 10.1093/synbio/ysaa019. PMID: 33344777; PMCID: PMC7737004.7、Moore SJ, MacDonald JT, Wienecke S, Ishwarbhai A, Tsipa A, Aw R, Kylilis N, Bell DJ, McClymont DW, Jensen K, Polizzi KM, Biedendieck R, Freemont PS. Rapid acquisition and model-based analysis of cell-free transcription-translation reactions from nonmodel bacteria. Proc Natl Acad Sci U S A. 2018 May 8;115(19):E4340-E4349. doi: 10.1073/pnas.1715806115. Epub 2018 Apr 17. PMID: 29666238; PMCID: PMC5948957.8、Kennedy A, Griffin G, Freemont PS, Polizzi KM, Moore SJ. A curcumin direct protein biosensor for cell-free prototyping. Eng Biol. 2022 Aug 18;6(2-3):62-68. doi: 10.1049/enb2.12024. PMID: 36969103; PMCID: PMC9996706.9、Zubi YS, Seki K, Li Y, Hunt AC, Liu B, Roux B, Jewett MC, Lewis JC. Metal-responsive regulation of enzyme catalysis using genetically encoded chemical switches. Nat Commun. 2022 Apr 6;13(1):1864. doi: 10.1038/s41467-022-29239-y. PMID: 35387988; PMCID: PMC8987029.10、Garabedian BM, Meadows CW, Mingardon F, Guenther JM, de Rond T, Abourjeily R, Lee TS. An automated workflow to screen alkene reductases using high-throughput thin layer chromatography. Biotechnol Biofuels. 2020 Nov 9;13(1):184. doi: 10.1186/s13068-020-01821-w. PMID: 33292503; PMCID: PMC7653764.11、Burén S, Young EM, Sweeny EA, Lopez-Torrejón G, Veldhuizen M, Voigt CA, Rubio LM. Formation of Nitrogenase NifDK Tetramers in the Mitochondria of Saccharomyces cerevisiae. ACS Synth Biol. 2017 Jun 16;6(6):1043-1055. doi: 10.1021/acssynbio.6b00371. Epub 2017 Mar 3. PMID: 28221768; PMCID: PMC5477005.12、Blount BA, Ellis T. The Synthetic Genome Summer Course. Synth Biol (Oxf). 2018 Nov 27;3(1):ysy020. doi: 10.1093/synbio/ysy020. PMID: 32995526; PMCID: PMC7445779.13、Haines MC, Carling B, Marshall J, Shenshin VA, Baldwin GS, Freemont P, Storch M. basicsynbio and the BASIC SEVA collection: software and vectors for an established DNA assembly method. Synth Biol (Oxf). 2022 Oct 11;7(1):ysac023. doi: 10.1093/synbio/ysac023. PMID: 36381610; PMCID: PMC9664905.14、Exley K, Reynolds CR, Suckling L, Chee SM, Tsipa A, Freemont PS, McClymont D, Kitney RI. Utilising datasheets for the informed automated design and build of a synthetic metabolic pathway. J Biol Eng. 2019 Jan 18;13:8. doi: 10.1186/s13036-019-0141-z. PMID: 30675181; PMCID: PMC6339355.
新品
2024.05.11
【离心课堂】离心机的前世今生——离心技术发展简史
“ 采用离心技术进行血液分离的历史可以追溯到十九世纪;电动低速台式离心机的商品化始于1912年;实验离心技术工作始于上世纪20年代;随后高速、超速离心机的商品化生产、实验离心技术的普遍应用则是从上世纪五十年代起始的。”现代生物医学研究的进展和对研究、诊断手段的大量需求促进了离心设备的开发,也有利于各种样品(特别是生物体组份)离心分离方法的迅速推广和应用。二十世纪70年代以后,低速、高速、超速离心机产品几经更新换代。目前,先进的超速离心机已经能够产生相当于重力加速度100多万倍的离心场并能保持此离心场连续运转数十小时以上;新一代的超速离心机还能对各种生物样品离心方法进行智能模拟,以拟定最佳的离心分离方案。综观实验离心技术的进步里程,一些重要事件简述如下:1911~1912年:开始生产和使用低速(3,000rpm以下)的商品化台式离心机;1923~1926年:瑞典UPPSALA大学Svedberg等科学家试制了世界上第一台试验型超速离心机(45,000rpm);1926年:T.斯韦德贝里和R.法劳斯测定了马血红蛋白的分子量,获得诺贝尔化学奖;1929年:Lamn完成了沉降方程、计算了沉降速度、定义了沉降系数;点击查看【离心课堂】常用术语之沉降系数1932年:细胞核的离心纯化(Behrens);1933年:Beams,Pickels研制成试验型空气透平驱动超速机;1947年:美国Beckman Coulter公司的Model E全球首台分析型超速离心机和Model L制备型超速离心机供应市场;1951年:Brakke在差速离心的基础上发展了速率区带离心法。Kahler研制成功水平转头;点击查看【速率区带离心法 | 你的分离纯化方法选对了吗?1955年:Anderson研制出区带转头,并用区带离心法首次证明了DNA双螺旋结构半保留复制假说;1957~1959年:Meselson、Duve等开发了等密度离心法;1963年:美国Beckman Coulter公司推出全球首个Type 50 Ti钛金属转头;点击查看【离心课堂】转头效率K因子与离心时1974年:美国Beckman Coulter公司推出全球首台Microfuge B全球首台微量离心机;1975年:垂直管转头转头被开发并用于Dupont-Sorvall油透平驱动的超速离心机1981年:美国Beckman Coulter公司开发的用于细胞离心纯化的“淘洗”转头供应市场;1998年:美国Beckman Coulter公司推出全球首台超过一百万离心力的OptimaTMMAX台式超速离心机;1998年:美国Beckman Coulter公司开发出ARIES可以自我修正平衡的转头;2002年:美国Beckman Coulter公司开发了采用触幕式操作的OptimaTML-XP超速离心机,其离心专家软件可对各种生物样品的离心方法进行本机实验模拟,以找到最佳的离心分离方案,并可进行诸如分子量、沉降系数等的计算;2012年:美国Beckman Coulter公司开发了全球首台智能化超速离心机OptimaTMX系列,从此离心机进入智能化时代;2014和2015年:智能化离心技术被引入落地式高速离心机领域,相继推出JXN-26和JXN-30系列智能化高效离心机。点击查看贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn),查看更多精彩资料!
参数原理
2024.05.08
【离心课堂】等密度梯度离心法 | 你的分离纯化方法选得对吗?
离心方法——等密度梯度离心法等密度梯度离心也称为平衡密度梯度离心。等密度梯度离心是根据样品中各组分的浮力密度差不同进行分离。在离心立场中,溶液中颗粒浮力密度小则上浮,浮力密度大则下沉,上浮和下沉的颗粒会一直延梯度液移动到与其浮力密度恰好相等的位置上,该位置也称颗粒的等密度点,离心时样品各组分颗粒将按其密度大小分别移至等密度点形成区带,形成的区带不会因离心时间长而发生变化。离心后收集所需区带颗粒即为纯化组分。离心前后样品的状态如图1所示。图 1 等密度区带离心因此,在离心前,样品可置于梯度液的任意位置,一般是均匀分布在梯度液中。等密度区带离心法的离心效果取决于样品颗粒的浮力密度差,密度差越大,分离效果越显著,与样品颗粒的大小与形状无关。速率区带离心和等密度区带离心都需预准备梯度液。速率区带离心的梯度液密度必须小于待分离组分中小颗粒的浮力密度。利用颗粒形状和大小差异而形成的沉降速率不同达到分离目的。等密度区带离心是一种平衡离心方法,利用颗粒密度差进行分离,与颗粒形状和大小无关,处理量比差速离心法大。等密度梯度离心经常使用的梯度液包括氯化铯(CsCI)、溴化钠等,典型的应用包括质粒DNA(或者其他DNA、RNA核酸片段)的大规模高纯度纯化,脂蛋白的分离纯化等。质粒DNA的氯化铯等密度梯度离心分离纯化流程如下:脂蛋白溴化钠等密度梯度离心分离纯化流程如下:人全血1000g离心10分钟去除各种血细胞,上清为血清。血清加入NaBr密度梯度液(不连续梯度)的底部,往上依次铺浓度变小的梯度液。然后在水平转头中,260,000g离心力14℃下离心24小时,各种密度的脂蛋白从管底浮向它们自己的等密度区形成了纯的各种密度脂蛋白区。而离心管底部保留着各种血清蛋白。用上排法从离心管中抽出各层液体,经DU核酸蛋白分析仪测定,定位各种不同密度血清脂蛋白。点击查看贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn),查看更多精彩资料!
参数原理
2024.05.08
【离心课堂】差速离心方法
“ 在实验过程中,由于样品的各种性质差异,只有选择了正确的离心方法,才能获得预期的分离纯化结果。常用的离心方法主要有差速离心法、密度梯度离心法。其中密度梯度离心法又可细分为速率区带离心和等密度梯度离心法。本期向大家具体介绍离心方法之差速离心。”离心方法之差速离心差速离心法(differential velocity centrifugation method)又称离心力差分离法。差速离心法原理利用样品中各组分沉降系数的差异,对不同的微粒施以不同的离心力,经过多次离心,离心速度逐步加大,将不同的微粒依次沉降,从而实现离心分离。差速离心原理可用离心力表达式说明:F=ma, 其中 a=ω²R。由于小粒径的微粒质量小,分离时所需离心力大。为满足大离心力的需要,必需提高其旋转速度,方可分离。以不同的离心力分离不同粒径的微粒是动力学的分离方法,特别是沉降速度差别较大的微粒多采用此种分离方法。如果分离样品中有大中小三种不同粒径的微粒,对它们施以不同的离心力,大粒径的微粒,其质量较大,将会首先沉降;分离上清液,以更大转速对上清液进行第二次离心,中颗粒被分离出来;再取上清以更大离心力,更高的转速,最后沉降小颗粒,以达到不同颗粒的分离,如图1所示。图1差速离心由于在每种颗粒的沉淀物中总含有部分次级颗粒,如想将某种颗粒提纯,需对该颗粒的沉淀物进行稀释后再离心沉淀,最终可制备出理想纯度的颗粒。差速离心法之优劣势差速离心主要用于分离直径和密度差异较大的颗粒,其优势在于分离时间短、重复性高,样品处理量大,可用于大量样品的初分离。但是在使用差速离心法分离复杂样品时,或分离纯度要求较高时,会需要多次进行离心,操作繁杂;其次,由于沉淀的多次清洗、溶解及再沉淀,容易引起中间损失,会造成离心分辨力差的问题;此外,实际分离时由于离心时的对流、扩散和收取沉淀时的污染,对于一些沉降系数相差不大的组分无法进行完全的分离提纯。由于差速离心法在样品的纯度和回收率方面的限制,它主要用于用于大量样品的初步分离提纯,为下一步检测或实验做准备。例如,我们可以对动物肝组织匀浆液进行多次的不同相对离心力和时间的离心和沉淀/上清分步收集,得到样品的细胞核、线粒体、溶酶体和核糖体等的初步分离富集沉淀,用于下一步的其他检测或者精细纯化实验。具体的处理流程如下:离心课堂正在连载,持续关注了解更多离心方法!点击进入贝克曼库尔特官网:贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn)了解更多产品信息!
参数原理
2024.05.08
【离心课堂】速率区带离心法 |你的分离纯化方法选对了吗?
密度梯度离心(isodensity centrifugation method)又称为区带离心。01离心时先将样品溶液置于一个由惰性梯度材料形成的密度梯度液体柱中02离心后被分离组分以区带层分布于梯度柱中该方法的优点是可以同时使样品中几种或全部组分分离,具有良好的分辨率,分离效果好,可一次获得较纯组分。缺点是离心时间较长,需制备梯度液,操作要求高。按照离心分离原理,密度梯度离心又可分为速率区带离心法(rate zonal centrifugation method,R-Z)和等密度离心法 (isopycnic centrifugation method)。速率区带离心也可称为等区密度离心,是根据样品中不同组分粒子所具有的不同的体积大小和不同的沉降系数将混合样品进行离心分离提纯。离心时将需要分离的样品溶液置于由密度梯度材料(如蔗糖、氯化铯 (CsCI)、溴化钠等)形成的梯度液柱上面,样品粒子的密度必须大于梯度液柱中任一点的密度,否则无法得到理想的区带离心效果。离心时,混合样品中不同的组分将在梯度液柱的不同位置分别形成各自的区带,选择适合的转速和时间进行离心,当各组分区带距离拉得远时,结束离心,然后将区带取出。这样只需通过一次离心就可以把混合样品中的各组分分离提纯,其纯度和回收率均可满足要求。优点是一次分离纯化,组分的沉降系数相差 20% 以上的即可选用此法,分辨力高,操作熟练可以将组分沉降系数相差 5%~10% 的样品很好的分离。缺点是材料的条件限制,样品液浓度不能太高,否则操作条件很难控制,同时此法与差速离心法相比,处理样品的量要小的多。图 1 速率区带离心速率区带离心的时间必须严格控制,不能太短,否则样品区带不清,时间也不能太长,否则待分离组分可能沉底。需要分离的样品颗粒的沉降速度取决于颗粒形状、大小、密度及离心力等因素。离心前后样品的状态如图 1 所示。速率区带离心经典的应用就是通过蔗糖密度梯度离心,进行各种亚细胞器(核糖体、线粒体、Exosome 等)和病毒颗粒(病毒载体、疫苗等)的纯化。例如,我们在上一期中得到的 70S 核糖体沉淀,经过水解后,可利用蔗糖密度梯度离心,进一步分离纯化得到 50S 和 30S 的两个亚基。具体的实验流程如下:点击进入贝克曼库尔特官网:贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn)了解更多离心信息!
参数原理
2024.05.08
【离心课堂】转头效率K因子与离心时间
转头的k值转头的k值(又称k因子或k系数)用以衡量转头的沉淀效率。所有的离心机厂家在转头出厂时都计算了制备型转头的k值,转头k值通过在转头运行至最高转速、离心管装满样品时计算得到的,其计算公式如下:k 转头的k值rmax 最大半径,指旋转轴到离心管底端的垂直距离rmin最小半径,指旋转轴到离心管顶端的垂直距离ω角速度由于将公式(2)代入公式(1)可得到以下转头k 值的计算公式:由上得出转头k值是与转头的最高转速和形状有关。最高转速完全一样的转头,离心管与轴的角度越小,也就是rmax/rmin 越小,k值就越小。所以制备型超速离心机的四类转头的k值如下:水平转头k值 > 定角转头k值 > 近垂直转头k值 > 垂直转头k值。如果在离心时,转头没有运行到最高转速,那么rpm就不能使用最高转速的k值,必须将转头实际运行转速代入公式(3)来计算实际的k值。离心时间已知某转头k值和颗粒的沉降系数,可以计算出用该转头分离颗粒时所需要的时间。其公式如下:t 沉淀时间(单位:小时)k指实际运行状态下的转头k值s颗粒的沉降系数由公式(5)可以看出,转头k值是评估转头离心效率的一个指标,对于沉淀同一颗粒,转头k值越小,颗粒沉淀所需要的时间就越短,也就是离心效率越高;反之,转头k值越大,颗粒沉淀所需要的时间就越长,转头的离心效率越低。举例分离沉降系数为15S的蛋白,如果用的转头k值是15,那么沉降该蛋白颗粒所需要的时间是:t = k/s = 15/15 = 1 小时如果用的转头k值是18,那么沉降所需的时间是:t = k/s = 18/15 = 1.2 小时已知一个转头k值和沉淀所需要的时间,如果用另一个转头来沉淀同样的颗粒,可以用以下公式来计算需要沉淀的时间:kaa转头的k值kbb转头的k值taa转头沉降样品所需要的时间tbb转头沉降样品所需要的时间如果该转头不是在最高转速下运行,或者样品没有装满,又或者换用了其他更小的离心管(例如g-MAX 管等),相应k值都会发生改变,相应离心所需的时间也需要重新计算。综上所述k因子已经综合考虑了离心的转速、相对离心力以及样品在最小半径和最大半径等位置的受力改变情况,还有颗粒沉降的行程等因素,是计算离心时间、评价转头离心效率的最准确和最重要指标。关注小贝离心课堂,了解更多离心信息!点击查看贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn),查看更多精彩资料!
参数原理
2024.05.08
【离心课堂】常用术语 – 沉降系数
沉降系数迄今为止,离心工作的重点的就是生物颗粒的制备,所以了解颗粒的沉降特性是至关重要的。沉降系数是生物大分子极其重要的物理参数,通过它可以了解生物大分子的相对分子量、分子形状和水化程度等。早在1940 年,Svedberg 和Pedersen 发展了用分析超速离心技术来测量生物大分子的沉降系数和分子量,直至目前分析超速离心方法仍然是测定生物大分子沉降系数的金标准。Svedberg 在实验过程中定义了沉降系数(S,Svedberg):s 就是单位离心加速度的作用下颗粒移动的速度。用以下公式表示:dr/dt:颗粒移动速度ω2r : 离心加速度d: 平均粒径𝜎: 颗粒密度𝜌: 溶剂密度 𝜂: 溶剂粘度 由于大部分的生物大分子的沉降系数都在10-11-10-13s(秒)范围内,故定义了沉降系数的单位S,1 S = 1 x 10-13s(秒)。s 值经常被用来描述生物大分子(如核酸、蛋白)和一些大分子复合物(如核糖体、核糖体亚基),参见图3。蛋白的沉降系数在1-20S之间,核酸的沉降系数在5-100S 之间,亚细胞器的沉降系数则更大,基本在几百S 到几千S之间。图1:生物颗粒的沉降系数精彩内容后续不断,敬请关注!点击查看贝克曼库尔特官网贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn),查看更多精彩资料!
参数原理
2024.05.08
【离心课堂】离心常用术语 – 离心力和相对离心力
在生命科学研究中,离心是一种必不可少的技术手段,更是实验室中最常见的实验项目。但是你真的了解这门技术吗?你是否知道离心的原理,了解如何选择合适的转头、离心管和离心方法呢?小贝离心课堂重新开课,带你玩转离心机,快来加入我们吧!离心原理学习一门技术势必要先从了解其原理开始。我们可以通过简单的实验来理解离心的基本原理。首先我们来观察在重力作用下颗粒的沉降:抓一把沙子和泥土的混合物放到装有水的容器里摇匀,然后把容器置于桌上,观察到在地球引力作用下大量的颗粒立即沉淀到容器的底部。一段时间后,又看到容器中的混合物分成数层,每层都由大小相同的颗粒组成,颗粒在容器的分布从上到下逐渐增大。不过,仍然会有一些细小的颗粒在水中缓慢的向容器底部移动,由于移动得非常缓慢,我们不一定能观察到这些颗粒的运动。另外还有一些颗粒则漂浮在水面上。通过实验中观察到的结果,我们可以得出大颗粒比小颗粒更快地沉降到底部,而更小的颗粒则沉降得更慢。不过,一些密度比较重的小颗粒反而比密度比较轻的大颗粒沉降得更快。我们还可以看到有些小颗粒在水中是不沉降的,漂浮在水面。图1 重力作用下混合颗粒的沉降:颗粒沉降的速度依赖于颗粒的大小,大颗粒则先沉降到底部,而小颗粒则停留在容器的上部。以上即是离心的主要原理,液体中的颗粒在重力的作用下以一定的速率向下移动,颗粒移动的速率往往与颗粒的大小与密度相关,这样就出现了颗粒的沉降运动。当然前提是颗粒的密度必须大于液体的密度。总结来说,离心技术是利用离心机旋转运动产生离心力,将具有沉降系数差别的样品进行分离、分析、浓缩和提纯的一种技术。离心常用术语离心力和相对离心力尽管有些生物颗粒可以在重力场(1×g)作用下实现分离,如人血细胞,将处理过的血细胞置于桌上1-2 小时,由于不同细胞的大小不一样,白细胞和红细胞能自动分层。但若需分离更小的生物颗粒,远大于重力的力则是必须的,这可以通过沿轴旋转装有悬浮颗粒的离心管来实现。颗粒在放射状的离心力下从轴心向外运动,使离心管旋转的机器就是离心机,而装载了离心管并带动离心管沿轴旋转的即是转头。不管是细胞还是生物大分子受到离心力都可以用以下公式计算: (1)F离心力– 颗粒受到的离心力m – 颗粒的质量ω – 角速度r – 旋转轴到颗粒的距离但是通常情况下,旋转的转头受到的放射状的力都是由相对离心力(RCF:Relative centrifugation force)来衡量的。而所谓的相对离心力即是离心力与重力之比,用以下公式表示: (2)RCF – 相对离心力;F离心力– 颗粒受到的离心力;F重力– 颗粒受到的重力;m – 颗粒的质量;ω – 角速度;g –重力加速度;r – 旋转轴到颗粒的距离。ω 是转头的角速度,指转头每秒钟转过的弧度数,其值就是: (3)RPM (Revolution per minute) – 转头每分钟转过的转数结合公式(2)和公式(3)可得到同一转头的转速与相对离心力之间的关系: (4)r – 旋转轴到颗粒的距离(单位:毫米mm)由上可以看出转头的相对离心力与转头的转速的平方成正比,而且与转头的半径成正比。对于同一转头而言,由于半径不变,增加转速也就相当于提高了相对离心力。为便于进行转速和相对离心力之间的换算,Dole 和Cotzias 利用RCF 的计算公式,制作了转速“rpm”、相对离心力“RCF”和旋转半径“r”三者关系的列线图,图式法比公式计算法方便,且一目了然。换算时,先在r 标尺上取已知的半径和在rpm 标尺上取已知的离心机转数,然后将这两点间划一条直线,与图中RCF 标尺上的交叉点即为相应的相对离心力数值。上图转速与半径相对应的离心力列线图,左列为半径标尺,右列为转速标尺,连接半径与转速的直线与中间RCF 表尺的交汇点,就可得到相对离心力。注意,若已知的转数值处于rpm 标尺的右边,则应读取RCF 标尺右边的数值,转数值处于rpm 标尺左边,则应读取RCF 标尺左边的数值。在重力场的沉降中,重力场通常被看作恒定值,而离心管中的离心力场却不是一个恒定值。由于转头的形状及设计,离心管中从管顶至管底各点到旋转中心的距离是不同的,为了计算相对离心力的数值可用平均相对离心力来表示,即同一离心转头部和底部所受离心力的平均值。科技文献中离心力的数据通常是指其平均值(RCFav),即离心管中点的离心力。而各厂家在标注离心机和转头等的最大相对离心力(RCF)时,一般用最高转速下、最大半径处(Rmax)的相对离心力。请注意区分这个参数与平均离心力(RCFav)的差异。离心机常有多种不同形状的转头,其各自所反映的离心力场的大小和离心沉降距离也不一样,在实际工作中应根据分离要求正确选择使用。下一期小贝讲堂将具体介绍沉降系数,精彩不断,敬请关注!点击查看贝克曼库尔特生命科学官网及电商平台 (mybeckman.cn),查看更多精彩资料!
参数原理
2024.05.08
细胞计数仪知识分享系列 | 性能检测篇
细胞计数仪对于做动物细胞培养的老师而言,可以算是最简单又常用的分析仪器之一了。但看似简单的细胞计数仪,也可能让使用者为之抓狂。曾收到一位做工艺开发的老师反馈,他使用的一款细胞计数仪三次检测同一个样品,每次分析结果和平均值的偏差都超出正常可接受范围。这么简单的仪器为何会出现这种问题是否是仪器本身的性能问题在此,我们希望通过本文对细胞计数结果的重复性和准确性介绍,以及如何检测来帮助老师排查使用的仪器性能。对于性能不达标的老仪器,就可以考虑设备的更新了。关于重复性和准确性,我们可以通过下图所示的Precision和Accuracy来理解。如果重复性好,那连续几次测试结果比较集中,与平均值相比的偏差都比较小。而准确性则是和真实值进行比较,多次测试结果和真实值的偏差越小,说明测试准确性越好。1如果您手头已有细胞计数仪在使用,如何来判定这款细胞计数仪的重复性和准确性呢?根据《定量细胞计数方法性能的实验设计和统计分析(ISO20391-2:2019)》一文中,关于细胞计数方法性能判定的实验设计,建议至少做4个浓度梯度,每个浓度梯度至少做3次重复性测试。我们可以考虑使用该方法来评判手上细胞计数仪的性能好坏,具体的细胞选择和样品制备上可以参考ISO20391-2:2019里面的具体描述。在此,我们拿Vi-CELL BLU全自动细胞计数仪和另一款半自动插板式细胞计数仪分别进行细胞计数的重复性和准确性的性能评估。这里检测用到的是一种肿瘤细胞,按4个浓度梯度稀释(原液,2倍,5倍和10倍稀释),并且每个浓度做3组重复性检测,以下是测试得到的结果和统计数据。针对同一个样品的4个不同稀释倍数和3组重复性检测,同时使用半自动细胞计数仪(通常需要使用细胞计数板作为载体,同时台盼蓝染色需要手动完成)检测是怎样的效果呢?如下表所示是一款半自动细胞计数仪上检测得到的数据。由于半自动细胞计数仪装机后很久未做过标样的验证和校准,所以和全自动细胞计数仪的测试结果之间的差异在此不做比较分析。为了能比较得出这两台细胞计数仪的重复性和准确性的性能水平,我们将每台仪器3次原液检测(编号:S3-原液)得到的活细胞密度平均值作为“真值”。那么Vi-CELL BLU得到的“真值”是3.44M,而半自动细胞计数仪得到的“真值”是3.06M。而其他3个稀释倍数下计算得到的平均结果,都分别和这个“真值”进行比较,并且计算得到相对偏差。通过分析我们可以看到随着S3样品的稀释倍数不断增加,Vi-CELL BLU的活细胞密度平均值偏差也逐渐变大,但都在±10%的偏差范围内。同时每个稀释倍数下的3次重复性检测RSD都小于5%,显示出良好的测试结果重复性。而半自动细胞计数仪对5倍和10倍稀释的样品检测,3次测试结果的相对标准偏差已经大于10%,并且稀释10倍的活细胞密度平均值和原液“真值”结果比较,偏差达到了15.03%。所以,半自动细胞计数仪的重复性检测上相对要差很多,并且随着稀释倍数增加,检测得到的结果和原液结果之间的偏差加大。通过以上这种性能检测方法,我们可以得出无论是在3次测试的重复性,还是梯度稀释结果的准确性,Vi-CELL BLU全自动细胞计数仪都比半自动细胞计数仪更有优势。如果您对自己使用的细胞计数仪性能感兴趣,也可以尝试用这个方法来检测判断。至于为何Vi-CELL BLU全自动细胞计数仪在重复性检测和梯度稀释的测试准确性上,都比半自动插片式细胞计数仪更有优势?下一期的内容,我们将针对这个问题为您做具体的介绍。
操作维护
2024.04.30
重磅!全自动、高通量CE-SDS样品前处理及分离分析流程来了!
Beckman Biomek i5自动化移液工作站与SCIEX高通量毛细管电泳BioPhase™ 8800系统联合用于单抗CE-SDS纯度分析。CE-SDS是广泛用于药物纯度、完整性和稳定性分析的金标准方法。从抗体药物筛选,到生产工艺研究再到产品上市放行等不同阶段均需要进行大量的CE-SDS纯度实验。高通量毛细管电泳BioPhase™ 8800系统,采用8通道毛细管并行处理样品,大大提高样品采集速度。Biomek i5自动化移液工作站全自动完成样品前处理及缓冲液添加过程,省去大量人工操作时间,同时消除潜在的误差。两者的联合,必将迎来蛋白药物纯度高速分析的时代。近期,由两大生命科学仪器品牌贝克曼库尔特生命科学与SCIEX联合开发的Biomek i5自动化移液工作站与高通量毛细管电泳BioPhase™ 8800系统联用的流程,完成项目落地。图1. Biomek i5 span8自动化移液工作站 (左),高通量毛细管电泳BioPhase™ 8800系统 (中),BioPhase CE-SDS蛋白分子量&纯度分析试剂盒 (右)。自动化前处理流程展示图2. Biomek i5自动化移液工作站处理样品及缓冲液的过程示意图图3. Biomek i5工作站台面示意图(A:BioPhase™ 8800 系统样品盘;B:1.5 ml EP管架,用于放置10 kD内标、β-巯基乙醇和样品溶液;C:试剂槽,第一列放置样品缓冲液,其他位置空置;D:BioPhase 8800系统 样品出口盘;E-H:90 mL自动化移液枪头;I:1070 mL自动化移液枪头;J:BioPhase 8800系统缓冲液盘;K:试剂槽,从左到右分别为碱洗液、酸洗液、SDS分离胶及超纯水;L:BioPhase 8800系统缓冲液出口盘)部分结果展示图4. 96份还原单抗的CE-SDS电泳图。8个通道毛细管编号用A-H表示,A01-H01表示样品盘第一列的8份样品在8通道毛细管A-H的电泳图结果。主要优势提高效率贝克曼库尔特Biomek i5自动化移液工作站配备高通量移液器,同时完成样品前处理及多个试剂的添加,无需人工参与,缩短前处理时间,明显提升效率。减少误差通过自动化移液工作站,所有试剂添加过程及加热、混匀等动作完全自动化进行,增加操作的一致性,消除人工操作带来潜在的误差。稳定性好,重复性高SCIEX高通量毛细管电泳BioPhase™ 8800系统6.9 小时可完成96个还原单抗的CE-SDS纯度分析。8个毛细管和单根毛细管运行12针均获得高度的重复性。主峰(LC和HC) 相对迁移时间 (RMT)的RSD值小于0.14% (n=96) ,校准峰面积百分比的RSD值小于0.35% (n=96) ,说明该工作流程稳定、结果可靠。
企业动态
2024.04.30
大规模设备更新,不断升级的Vi-CELL细胞计数仪来助力
早在2002年贝克曼库尔特生命科学便在全球推出了第一款Vi-CELL细胞计数仪,当时一次只能测试一个样品,但仪器是全自动的,相比同期大家经常使用的显微镜+血球计数板的计数方法,操作更加简便,并且避免了样品混匀和染色方面的人为操作误差,因此测试结果的重复性更好。 血球计数板手动数细胞单通道Vi-CELL细胞计数仪随着生物医药的蓬勃发展,越来越多的细胞培养用于研发和生产各类生物制品,包括:各类疫苗、重组蛋白药物、单克隆抗体、基因治疗和细胞治疗药物等。因此,各个生物医药企业和研究机构对高通量细胞计数仪的需求也在不断增加。所以,带有12位上样转盘的Vi-CELL XR全自动细胞计数仪也应运而生(如下图所示)Vi-CELL XR计数仪保留了自动检测功能,同时上样通量从1位扩大到了12位,针对实验室中多位老师需要同时检测细胞样品的情况,12位转盘可以实现无需在旁等待的不间断上样检测。相比插板/片式半自动细胞计数仪,节省了老师在旁等待的时间,大大提高工作效率。因此,Vi-CELL XR细胞计数仪推出后受到广大使用客户的好评。随后的十几年间,生物制药的研发和生产各项技术日趋完善和成熟,对细胞计数仪的要求也越来越高。譬如工艺开发和细胞株开发部门需要更高的上样通量,更快的检测速度和更少的检测样品体积,而质量控制和生产部门则更看重仪器的重复性、稳定性和法规的符合度。根据Vi-CELL XR客户反馈的这些新需求,2019年新一代Vi-CELL BLU全自动细胞计数仪诞生。这款新型的Vi-CELL细胞计数仪,相比老款Vi-CELL XR在客户所提的需求,以及其他多个方面都做了较大的升级。具体可参照以下Vi-CELL新老仪器各项性能对比表(一些相同功能未列其中)。若将新老仪器间的主要升级点做个小结,可以概括为下面这张在设计和测试性能方面的对比图。如您希望了解更多新品Vi-CELL BLU细胞计数仪信息,请联系我们。
企业动态
2024.04.30
持续改进-助力焕新 贝克曼库尔特生命科学整体解决方案
应用实例
2024.04.19